
ЁОЬтФПЁПCЁЂNЁЂSЕФбѕЛЏЮяГЃЛсдьГЩвЛаЉЛЗОГЮЪЬтЃЌПЦбаЙЄзїепе§дкбаОПгУИїжжЛЏбЇЗНЗЈРДЯћГ§етаЉЮяжЪЖдЛЗОГЕФВЛРћгАЯьЁЃ
ЃЈ1ЃЉФПЧАЙЄвЕЩЯгавЛжжЗНЗЈЪЧгУCO2КЭH2дк230ЁцЃЌДпЛЏМСЬѕМўЯТзЊЛЏЩњГЩМзДМеєЦћКЭЫЎеєЦјЁЃШчЭМБэЪОКубЙШнЦїжа![]() КЭ
КЭ![]() ЦНвЦзЊЛЏТЪДя
ЦНвЦзЊЛЏТЪДя![]() ЪБЕФФмСПБфЛЏЪОвтЭМЁЃаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪН______________________ЁЃ
ЪБЕФФмСПБфЛЏЪОвтЭМЁЃаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪН______________________ЁЃ

ЃЈ2ЃЉвЛЖЈЮТЖШЯТЃЌЯђ2LКуШнУмБеШнЦїжаЭЈШы![]() КЭ
КЭ![]() ЃЌЗЂЩњЗДгІ
ЃЌЗЂЩњЗДгІ![]() ЃЌПЩгУгкЛиЪеШМЩебЬЦјжаЕФСђЁЃШєЗДгІНјааЕН
ЃЌПЩгУгкЛиЪеШМЩебЬЦјжаЕФСђЁЃШєЗДгІНјааЕН![]() ЪБДяЦНКтЃЌВтЕУ
ЪБДяЦНКтЃЌВтЕУ![]() ЕФЬхЛ§ЗжЪ§ЮЊ0.5ЃЌдђЧА20minЕФЗДгІЫйТЪ
ЕФЬхЛ§ЗжЪ§ЮЊ0.5ЃЌдђЧА20minЕФЗДгІЫйТЪ![]() _______
_______![]() ЃЌИУЮТЖШЯТЗДгІЛЏбЇЦНКтГЃЪ§K=________ЁЃЃЈБЃСєСНЮЛаЁЪ§ЃЉ
ЃЌИУЮТЖШЯТЗДгІЛЏбЇЦНКтГЃЪ§K=________ЁЃЃЈБЃСєСНЮЛаЁЪ§ЃЉ
ЃЈ3ЃЉЙЄвЕЩЯгаЖржжЗНЗЈгУгк![]() ЕФЭбГ§ЁЃ
ЕФЭбГ§ЁЃ
Ђй ПЩгУNaClOМюадШмвКЮќЪе![]() ЁЃЮЊСЫЬсИпЮќЪеаЇТЪЃЌГЃМгШы
ЁЃЮЊСЫЬсИпЮќЪеаЇТЪЃЌГЃМгШы![]() ЃЌЗДгІЙ§ГЬЕФЪОвтЭМШчЭМЫљЪОЃЌВњЩњЕФЫФМлФјКЭбѕдзгОпгаМЋЧПЕФбѕЛЏФмСІЃЌвђДЫПЩМгПьЖд
ЃЌЗДгІЙ§ГЬЕФЪОвтЭМШчЭМЫљЪОЃЌВњЩњЕФЫФМлФјКЭбѕдзгОпгаМЋЧПЕФбѕЛЏФмСІЃЌвђДЫПЩМгПьЖд![]() ЕФЮќЪеЁЃ
ЕФЮќЪеЁЃ
a. ![]() ЕФзїгУЪЧ____________________ЁЃ
ЕФзїгУЪЧ____________________ЁЃ
b. Й§ГЬ2ЕФРызгЗНГЬЪН___________________________________ЁЃ
c. Ca(ClO)2вВПЩгУгкЭбСђЃЌЧвЭбСђаЇЙћБШNaClOИќКУЃЌдвђЪЧ_______________ЁЃ

ЂкЁАбЧСђЫсбЮЗЈЁБЮќЪебЬЦјжаЕФ![]() ЁЃЪвЮТЬѕМўЯТЃЌНЋбЬЦјЭЈШы
ЁЃЪвЮТЬѕМўЯТЃЌНЋбЬЦјЭЈШы![]() ШмвКжаЃЌВтЕУШмвК
ШмвКжаЃЌВтЕУШмвК![]() гыКЌСђзщЗжЮяжЪЕФСПЗжЪ§ЕФБфЛЏЙиЯЕШчЭМЫљЪОЃЌ
гыКЌСђзщЗжЮяжЪЕФСПЗжЪ§ЕФБфЛЏЙиЯЕШчЭМЫљЪОЃЌ![]() ЕуЪБШмвКpH=7ЃЌдђ
ЕуЪБШмвКpH=7ЃЌдђ![]() _____________ЁЃ
_____________ЁЃ

ЃЈ4ЃЉгУЪЏФЋзіЕчМЋЃЌЪГбЮЫЎзіЕчНтвКЕчНтбЬЦјЭбЕЊЕФдРэШчЭМ1ЃЌ![]() БЛбєМЋВњЩњЕФбѕЛЏадЮяжЪбѕЛЏ
БЛбєМЋВњЩњЕФбѕЛЏадЮяжЪбѕЛЏ![]() ЃЌЮВЦјОЧтбѕЛЏФЦШмвКЮќЪеКѓХХШыПеЦјЁЃЕчСїУмЖШЖдШмвК
ЃЌЮВЦјОЧтбѕЛЏФЦШмвКЮќЪеКѓХХШыПеЦјЁЃЕчСїУмЖШЖдШмвК![]() КЭЖдбЬЦјЭбЯѕЕФгАЯьШчЭМ2ЫљЪОЃК
КЭЖдбЬЦјЭбЯѕЕФгАЯьШчЭМ2ЫљЪОЃК


ЭМ1 ЭМ2
Ђй NOБЛбєМЋВњЩњЕФбѕЛЏадЮяжЪбѕЛЏЮЊNO3-ЗДгІЕФРызгЗНГЬЪН__________________ЁЃХХШыПеЦјЕФЮВЦјЃЌвЛЖЈКЌгаЕФЦјЬхЕЅжЪЪЧ_________________ЃЈЬюЛЏбЇЪНЃЉЁЃ
Ђк ШмвКЕФpHЖдNOШЅГ§ТЪДцдкЯрЙиЙиЯЕЕФдвђЪЧ___________________________ЁЃ
ЁОД№АИЁПCO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ЁїH=-49kJ/mol 0.03 11.25 ДпЛЏМС 2NiO2+ClO-= Ni2O3+Cl-+2O Ca2+гыSO42-НсКЯЩњГЩФбШмЕФCaSO4ЃЌгаРћгкЗДгІЕФНјаа 3:1 3Cl2+8OH-+2NO=2NO3-+6Cl-+4H2O H2 ДЮТШЫсФЦдкЫсадЬѕМўЯТбѕЛЏаддіЧП
CH3OH(g)+H2O(g)ЁїH=-49kJ/mol 0.03 11.25 ДпЛЏМС 2NiO2+ClO-= Ni2O3+Cl-+2O Ca2+гыSO42-НсКЯЩњГЩФбШмЕФCaSO4ЃЌгаРћгкЗДгІЕФНјаа 3:1 3Cl2+8OH-+2NO=2NO3-+6Cl-+4H2O H2 ДЮТШЫсФЦдкЫсадЬѕМўЯТбѕЛЏаддіЧП
ЁОНтЮіЁП
ЃЈ1ЃЉИљОнЭМЪОЃЌПЩжЊ0.5molCO2КЭ1.5molH2зЊЛЏТЪДя80%ЪБЗХШШ23-3.4=19.6kJЃЌШЛКѓАДБШР§МЦЫуЃКCO2ЃЈgЃЉ+3H2ЃЈgЃЉ![]() CH3OHЃЈgЃЉ+H2OЃЈgЃЉЕФЁїHЕУГіИУЗДгІЕФШШЛЏбЇЗНГЬЪНЃЛ
CH3OHЃЈgЃЉ+H2OЃЈgЃЉЕФЁїHЕУГіИУЗДгІЕФШШЛЏбЇЗНГЬЪНЃЛ
ЃЈ2ЃЉСаГіШ§ааЪНЃЌРћгУвбжЊЙиЯЕевГізЊЛЏСПКЭЦНКтСПЃЌДњШыМЦЫуЙЋЪНМЦЫуЫйТЪКЭЦНКтГЃЪ§ЃЛ
ЃЈ3ЃЉЂйa. гЩЙ§ГЬ1КЭЙ§ГЬ2ЕФЗДгІПЩжЊЃЌNi2O3ЕФзїгУЪЧзїЮЊДпЛЏМСЃЛ
b. ИљОнДпЛЏЙ§ГЬЕФЪОвтЭМПЩжЊЃЌЙ§ГЬ2жаNiO2КЭClO-ЗДгІЩњГЩNi2O3ЁЂCl-ЁЂOЃЌОнДЫаДГіРызгЗНГЬЪНЃЛ
c. Ca2+гыSO42-НсКЯЩњГЩФбШмЕФCaSO4ЃЌгаРћгкЗДгІЕФНјааЃЛ
ЂкbЕуЪБШмвКЕФpH=7ЃЌИљОнЕчКЩЪиКуЗжЮіНтД№ЃЛ
ЃЈ4ЃЉЂйгЩЭМ1ПЩжЊЃЌгУЪЏФЋзіЕчМЋЃЌЕчНтЪГбЮЫЎдкбєМЋВњЩњCl2ЃЌНЋNOбѕЛЏЮЊNO3-ЁЃЕчНтЪБвѕМЋВњЩњH2ЁЃ
ЂкгЩЭМ2ПЩжЊЃЌШмвКЕФpHдНаЁЃЌNOЕФШЅГ§ТЪдНИпЁЃ
ЃЈ1ЃЉИљОнЭМжаЪ§ОнЃЌКубЙШнЦїжа0.5molCO2КЭ1.5molH2зЊЛЏТЪДя80ЃЅЪБЕФФмСПБфЛЏЃЌ23kJ-3.4kJ=19.6kJЃЌЁїH =![]() =-49 kJ/molЃЌИУЗДгІЕФШШЛЏбЇЗНГЬЪНЃКCO2(g)+3H2(g)
=-49 kJ/molЃЌИУЗДгІЕФШШЛЏбЇЗНГЬЪНЃКCO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ЁїH=-49kJ/molЃЌ
CH3OH(g)+H2O(g)ЁїH=-49kJ/molЃЌ
вђДЫЃЌБОЬте§ШЗД№АИЪЧЃКCO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ЁїH=-49kJ/molЃЛ
CH3OH(g)+H2O(g)ЁїH=-49kJ/molЃЛ
ЃЈ2ЃЉЩшНјааЕН![]() ЪБДяЦНКтЃЌзЊЛЏЕФCOЕФЮяжЪЕФСПЮЊ2xЃЌдђЃК
ЪБДяЦНКтЃЌзЊЛЏЕФCOЕФЮяжЪЕФСПЮЊ2xЃЌдђЃК
2CO(g)+SO2(g)![]() 2CO2(g)+S(s)
2CO2(g)+S(s)
Ц№ЪМСПЃЈmolЃЉ 2 1 0
зЊЛЏСПЃЈmolЃЉ 2x x 2x
ЦНКтСПЃЈmolЃЉ 2-2x 1-x 2x
ИљОнЦНКтЪБCO2ЕФЬхЛ§ЗжЪ§ЮЊ0.5ЃЌгаЃК![]() =0.5ЃЌНтЕУx=0.6ЃЌ
=0.5ЃЌНтЕУx=0.6ЃЌ
дђЧА20minЕФЗДгІЫйТЪ![]()
![]() =0.03
=0.03![]() ЃЌ
ЃЌ
ЦНКтЪБЃЌCOЁЂSO2КЭCO2ХЈЖШЗжБ№ЮЊ0.4mol/LЁЂ0.2mol/LЁЂ0.6mol/LЃЌдђ
ЦНКтГЃЪ§K=![]() =
=![]() =11.25ЁЃ
=11.25ЁЃ
вђДЫЃЌБОЬте§ШЗД№АИЪЧЃК0.03ЃЛ11.25ЃЛ
ЃЈ3ЃЉЂйa. гЩЙ§ГЬ1КЭЙ§ГЬ2ЕФЗДгІПЩжЊЃЌNi2O3ЕФзїгУЪЧзїЮЊДпЛЏМСЃЛ
b.ИљОнДпЛЏЙ§ГЬЕФЪОвтЭМПЩжЊЃЌЙ§ГЬ2жаNiO2КЭClO-ЗДгІЩњГЩNi2O3ЁЂCl-ЁЂOЃЌРызгЗНГЬЪНЮЊ2NiO2+ClO-= Ni2O3+Cl-+2OЃЛ
c. Ca(ClO)2вВПЩгУгкЭбСђЃЌЧвЭбСђаЇЙћБШNaClOИќКУЃЌЪЧвђЮЊCa2+гыSO42-НсКЯЩњГЩФбШмЕФCaSO4ЃЌгаРћгкЗДгІЕФНјааЃЌ
вђДЫЃЌБОЬте§ШЗД№АИЪЧЃКДпЛЏМСЃЛ2NiO2+ClO-= Ni2O3+Cl-+2OЃЛCa2+гыSO42-НсКЯЩњГЩФбШмЕФCaSO4ЃЌгаРћгкЗДгІЕФНјааЃЛ
ЂкbЕуЪБШмвКЕФpH=7ЃЌИљОнЕчКЩЪиКуЃКn(NH4+)= n(HSO3-)+2n(SO32-)ЃЌгжИљОнЭМПЩжЊЃКn(HSO3-)= n(SO32-)ЃЌn(NH4+)ЃКn(SO32-)=ЃЈ1+2ЃЉ:1=3:1ЃЌ
вђДЫЃЌБОЬте§ШЗД№АИЪЧЃК3:1ЃЛ
ЃЈ4ЃЉЂйгЩЭМ1ПЩжЊЃЌгУЪЏФЋзіЕчМЋЃЌЕчНтЪГбЮЫЎдкбєМЋВњЩњCl2ЃЌНЋNOбѕЛЏЮЊNO3-ЃЌЗДгІЕФРызгЗНГЬЪН3Cl2+8OH-+2NO=2NO3-+6Cl-+4H2OЁЃЕчНтЪБвѕМЋВњЩњH2ЃЌЙЪХХШыПеЦјЕФЮВЦјЃЌвЛЖЈКЌгаЕФЦјЬхЕЅжЪЪЧH2ЁЃ
вђДЫЃЌБОЬте§ШЗД№АИЪЧЃК3Cl2+8OH-+2NO=2NO3-+6Cl-+4H2OЃЛH2ЃЛ
ЂкгЩЭМ2ПЩжЊЃЌШмвКЕФpHдНаЁЃЌNOЕФШЅГ§ТЪдНИпЃЌШмвКЕФpHЖдNOШЅГ§ТЪДцдкЯрЙиЙиЯЕЕФдвђЪЧДЮТШЫсФЦдкЫсадЬѕМўЯТбѕЛЏаддіЧПЁЃ
вђДЫЃЌБОЬте§ШЗД№АИЪЧЃКДЮТШЫсФЦдкЫсадЬѕМўЯТбѕЛЏаддіЧПЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕШЬхЛ§ЕФNaSO4ЁЂKAlЃЈSO4ЃЉ2ЁЂAl2ЃЈSO4ЃЉ3ЃЌШ§жжШмвКЗжБ№гыЕШЬхЛ§ЁЂЕШХЈЖШЕФBaCl2ШмвКЭъШЋЗДгІЃЌдђШ§ШмвКЕФЮяжЪЕФСПХЈЖШжЎБШЮЊ
AЃЎ1:2:3
BЃЎ3:2:1
CЃЎ6:3:2
DЃЎ2:3:6
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАЂдњЮїТЁ(azasetron)ЪЪгУгкжЮСЦгЩЗўгУвЉЮяв§Ц№ЕФЖёаФЁЂХЛЭТЕШЯћЛЏЕРжЂзДЁЃЫќПЩгЩЫЎбюЫсМзѕЅ(a)ЮЊдСЯКЯГЩЃЌВПЗжКЯГЩТЗЯпШчЯТЃК


ЪдЛиД№ЯТСаЮЪЬтЃК
(1)АЂдњЮїТЁЕФЗжзгЪНЮЊ________ЃЛcЮяжЪжаКЌбѕЙйФмЭХЕФУћГЦЪЧ________ЁЃ
(2)ЗДгІЂкЫљгУЪдМСЪЧ________ЁЃ
(3)1 mol bЮяжЪгызуСПNaOHШмвКЗДгІЃЌзюЖрЯћКФ________mol NaOHЁЃ
(4)ЫЎбюЫсМзѕЅ(a)ЕФЭЌЗжвьЙЙЬхжаЃЌТњзуЯТСаЬѕМўЕФЙВга________жжЁЃ
AЃЎгыЬМЫсЧтФЦШмвКЗДгІЗХГіЖўбѕЛЏЬМ
BЃЎгыТШЛЏЬњШмвКЗДгІЯдзЯЩЋ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГСђЫсУОКЭСђЫсТСЕФЛьКЯШмвКжаЃЌc(Mg2+ )ЃН2 molЁЄLЃ1ЃЌc(SO42-)ЃН6.5 molЁЄLЃ1ЃЌШєНЋ200 mLДЫЛьКЯвКжаЕФMg2ЃЋКЭAl3ЃЋЗжРыЃЌжСЩйгІМгШы1.6 molЁЄLЃ1ЧтбѕЛЏФЦШмвКЕФЬхЛ§ЪЧ
AЃЎ0.5 L BЃЎ1.625 LCЃЎ1.8 LDЃЎ2 L
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГШмвКжаПЩФмКЌгаH+ЃЌNa+ЃЌ![]() ЃЌMg2+ЃЌFe3+ЃЌAl3+ЃЌ
ЃЌMg2+ЃЌFe3+ЃЌAl3+ЃЌ![]() ЃЌ
ЃЌ![]() ЕШРызгЃЎЕБЯђИУШмвКжаМгШывЛЖЈЮяжЪЕФСПХЈЖШЕФNaOHШмвКЪБЃЌЗЂЯжЩњГЩГСЕэЕФЮяжЪЕФСПЫцNaOHШмвКЕФЬхЛ§БфЛЏЕФЭМЯёШчЭМЫљЪОЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ( )
ЕШРызгЃЎЕБЯђИУШмвКжаМгШывЛЖЈЮяжЪЕФСПХЈЖШЕФNaOHШмвКЪБЃЌЗЂЯжЩњГЩГСЕэЕФЮяжЪЕФСПЫцNaOHШмвКЕФЬхЛ§БфЛЏЕФЭМЯёШчЭМЫљЪОЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ( )
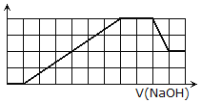
A.дШмвКжаКЌгаЕФбєРызгЪЧH+ЃЌ![]() ЃЌMg2+ЃЌAl3+
ЃЌMg2+ЃЌAl3+
B.дШмвКжавЛЖЈКЌга![]() ЃЌвЛЖЈВЛКЌ
ЃЌвЛЖЈВЛКЌ![]()
C.дШмвКжаКЌгаЕФFe3+КЭAl3+ЕФЮяжЪЕФСПжЎБШЮЊ1ЃК1
D.ЗДгІзюКѓаЮГЩЕФШмвКжаКЌгаЕФШмжЪГ§СЫNa2SO4ЭтЛЙгаЦфЫќЮяжЪ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЫсЪНбЮNaHYЕФЫЎШмвКЯдМюадЃЌЯТСаа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
A.H2YЕФЕчРыЗНГЬЪНЮЊЃКH2Y![]() 2HЃЋЃЋY2Ѓ
2HЃЋЃЋY2Ѓ
B.HYЃЕФЫЎНтЗНГЬЪНЮЊЃКHYЃЃЋH2O![]() H3OЃЋЃЋY2Ѓ
H3OЃЋЃЋY2Ѓ
C.ИУЫсЪНбЮШмвКжаРызгХЈЖШЙиЯЕЮЊЃКc(NaЃЋ)ЃОc(HYЃ)ЃОc(OHЃ)ЃОc(HЃЋ)ЃОc(Y2Ѓ)
D.ИУЫсЪНбЮШмвКжаРызгХЈЖШЙиЯЕЮЊЃКc(NaЃЋ)ЃОc(Y2Ѓ)ЃОc(HYЃ)ЃОc(OHЃ)ЃОc(HЃЋ)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪЧЬНОПЛЏбЇЙ§ГЬЕФживЊЭООЖЃЌгаЙиЯТСаИїЪЕбщзАжУЭМЕФа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ

![]()
A. ЭМIПЩгУгкЬНОП NaHCO3ЙЬЬхЕФШШЮШЖЈад
B. ЭМЂђгУгкДгТШЛЏФЦШмвКжаЛёЕУОЇЬх
C. ЭМIIIжаbПкНјЦјПЩЪеМЏCl2ЁЂCO2ЕШЦјЬх
D. ЭМЂєжаШєXЮЊNaOHШмвКЃЌдђПЩЭъГЩSO2ЕФХчШЊЪЕбщ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСабЁЯюжаЕФдвђЛђНсТлгыЯжЯѓВЛЖдгІЕФЪЧ
бЁЯю | ЯжЯѓ | двђЛђНсТл |
A | дкH2O2жаМгШыMnO2ЃЌФмМгЫйH2O2ЕФЗжНтЫйТЪ | MnO2НЕЕЭСЫЗДгІЫљашЕФЛюЛЏФм |
B | НЋЪЂгаNO2ЦјЬхЕФУмБеШнЦїНўХндкШШЫЎжаЃЌШнЦїФкЦјЬхбеЩЋБфЩю | 2NO2(g) |
C | дкУмБеШнЦїжагаЗДгІЃКA+xB(g) | AЮЊЗЧЦјЬхЁЂxЃН1 |
D | Яђ5mL 0.005molЁЄL-1FeCl3ШмвКжаМгШы5mL 0.015molЁЄL-1 KSCNШмвКЃЌШмвКГЪКьЩЋЃЌдйЕЮМгМИЕЮ1molЁЄL-1 KSCNШмвКЃЌШмвКбеЩЋМгЩю | діДѓЗДгІЮяХЈЖШЃЌЦНКтЯђе§ЗДгІЗНЯђвЦЖЏ |
A. A B. B C. C D. D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЮТЖШЯТЃЌХЈЖШЖМЪЧ1molЁЄL-1ЕФСНжжЦјЬхX2КЭY2дкУмБеШнЦїжаЗДгІЃЌОЙ§tminКѓЃЌВтЕУЮяжЪЕФХЈЖШЗжБ№ЮЊЃКcЃЈX2ЃЉЃН0ЃЎ4molЁЄL-1ЃЌcЃЈY2ЃЉЃН0ЃЎ8molЁЄL-1ЃЌдђИУЗДгІЕФЗНГЬЪНПЩБэЪОЮЊЃЈЃЉ
A. X2+2Y2![]() 2XY2B. 2X2+Y2
2XY2B. 2X2+Y2![]() 2X2Y
2X2Y
C. X2+3Y2![]() 2XY3D. 3X2+Y2
2XY3D. 3X2+Y2![]() 2X3Y
2X3Y
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com