
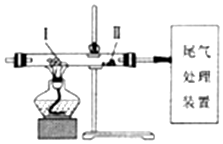
| A. | 缓慢通入N2,再加热Ⅰ处的碳酸氢钠,可观察到Ⅱ处过氧化钠粉末由浅黄色变成白色 | |
| B. | 缓慢通入N2,加热Ⅰ处KClO3和MnO2的混合物,可观察到Ⅱ处干燥KI淀粉试纸变成蓝色 | |
| C. | 先对Ⅰ处的氯化铵加热,再缓慢通入N2,可看到Ⅰ处固体减少,Ⅱ处无固体沉积 | |
| D. | 先缓慢通入CO2,再加热Ⅰ处炭粉,可观察到Ⅱ处氧化铁粉末由红色变成黑色 |
分析 A.碳酸氢钠加热分解生成二氧化碳,二氧化碳能够与过氧化钠反应生成碳酸钠和氧气;
B.应该用湿润的碘化钾淀粉试纸,否则试纸不会变蓝;
C.氯化铵加热分解生成氨气和氯化氢,冷却后氨气与氯化氢结合生成氯化铵;
D.氧化铁与CO的反应必须在高温下进行.
解答 解:A.缓慢通入N2,再加热Ⅰ处的碳酸氢钠,分解生成的二氧化碳与过氧化钠反应生成无色的碳酸钠,则可观察到Ⅱ处过氧化钠粉末由浅黄色变成白色,故A正确;
B.加热Ⅰ处KClO3和MnO2的混合物会生成氧气,氧气不与干燥的碘化钾反应,则试纸不会变蓝,故B错误;
C.先对Ⅰ处的氯化铵加热,氯化铵分解生成氨气和HCl,可看到Ⅰ处固体减少,但是氨气与HCl遇冷又会反应生成氯化铵,在Ⅱ处会出现固体沉积,故C错误;
D.Ⅱ处缺少加热装置,则CO无法还原氧化铁,所以氧化铁粉末不会由红色变成黑色,故D错误;
故选A.
点评 本题考查化学实验方案的评价,题目难度不大,明确装置特点及实验目的为解答关键,注意掌握常见元素及其化合物性质,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:解答题

 ,E
,E .
. ;②CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O;⑥
;②CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O;⑥ .H→I
.H→I $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| KMnO4酸性溶液 的浓度/mol•L-1 | 溶液褪色所需时间t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
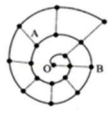 某同学在研究前 18 号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧 线上的“.”代表一种元素,其中 O 点代表氢元素.下列说法中错误的是( )
某同学在研究前 18 号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧 线上的“.”代表一种元素,其中 O 点代表氢元素.下列说法中错误的是( )| A. | B 元素是图中金属性最强的元素 | |
| B. | 虚线相连的元素处于同一族 | |
| C. | 离 O 点越远的元素原子半径越大 | |
| D. | A、B 两种元素组成的化合物中可能含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO3的电离方程式:H2SO3?2H++SO${\;}_{3}^{2-}$ | |
| B. | Cl-的结构示意图: | |
| C. | 乙醇的结构式:C2H5OH | |
| D. | HOCH2COOH缩聚产物的结构简式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①②④⑤ | C. | ①②③④ | D. | ②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com