
| A. | 9g甲基(-CH3)所含有的电子数是10NA个 | |
| B. | 4.2gC3H6中含有的碳碳双键数一定为0.1NA | |
| C. | 常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 | |
| D. | 22.4L乙烷中含有的共价键数为7NA个 |
分析 A、求出甲基的物质的量,然后根据甲基中含9个电子来分析;
B、C3H6不一定是丙烯,还可能是环丙烷;
C、乙烯和丙烯的最简式均为CH2;
D、乙烷所处的状态不明确.
解答 解:A、9g甲基的物质的量为0.6mol,而甲基中含9个电子,故0.6mol甲基中含5.4NA个电子,故A错误;
B、C3H6不一定是丙烯,还可能是环丙烷,故结构中不一定含碳碳双键,故B错误;
C、乙烯和丙烯的最简式均为CH2,故14g混合物中含有的CH2的物质的量为1mol,故含3NA个原子,故C正确;
D、乙烷所处的状态不明确,故乙烷的物质的量无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu→CuSO4 | B. | Fe→FeCl2 | C. | Al2O3→Al(OH)3 | D. | Fe(OH)2→Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
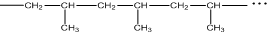 合成该高分子化合物的单体是( )
合成该高分子化合物的单体是( )| A. | CH2=CH2 | B. | CH2=CH-CH3 | C. | CH3CH2CH3 | D. | CH3CH(CH3)CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
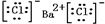 ,⑤的电子式是
,⑤的电子式是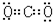 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com