
| A. | ①③⑤⑥ | B. | ③⑤ | C. | ①②⑤ | D. | ①③④⑥ |
分析 ①化学变化的实质:分子的分裂,原子的重新组合;
②焰色反应为物理反应;
③碱性氧化物一定是金属氧化物;
④纯净物是由一种物质组成的;
⑤同素异形体的化学性质相似;
⑥酸性氧化物可能和酸反应.
解答 解:①化学变化的特征是有新物质生成,通过化学变化不能实现16O与18O间的相互转化,故①错误;
②焰色反应不属于化学反应,故②错误;
③碱性氧化物一定是金属氧化物,故③正确;
④只由一种元素可以组成不同单质,如氧气和臭氧的混合气体只含一种元素,所以只由一种元素组成的物质不一定为纯净物,故④错误;
⑤同素异形体是指同种元素形成的不同单质,石墨和C60是同素异形体,故⑤正确;
⑥酸性氧化物可能和酸反应,如二氧化硫与硝酸反应,故⑥错误;
故选B.
点评 本题考查了基本化学概念,注意理解化学概念的含义,也可采用列举法解答.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | K | 0.6 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4的摩尔质量是98 | |
| B. | 等质量的O2和O3中所含的氧原子数相同 | |
| C. | 等体积的CO与CO2中所含碳原子数之比为1:1 | |
| D. | 将98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
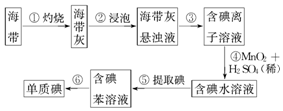
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | pH=4 时,醋酸的电离常数Ka≈1.8×10-5 | |
| B. | B点时,c(CH3COOˉ)=c(CH3COOH) | |
| C. | B点时,在溶液中滴入酚酞试剂,溶液显红色 | |
| D. | C点时,c(CH3COOˉ)>c(Na+)>c(H+)>c(OHˉ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
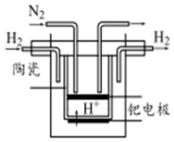 氮的固定对工农业及人类生存具有重大意义.
氮的固定对工农业及人类生存具有重大意义.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.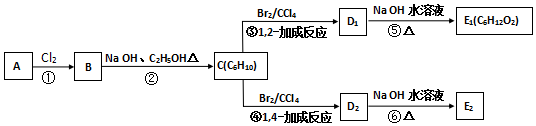
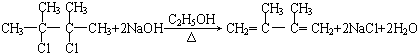 ,C的化学名称为2,3-二甲基-1,3-丁二烯,E2的结构简式是
,C的化学名称为2,3-二甲基-1,3-丁二烯,E2的结构简式是 ,②的反应类型是消去反应.
,②的反应类型是消去反应. +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$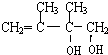 +2NaBr.
+2NaBr.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com