
【题目】部分中学化学常见元素原子结构及性质如表所示
元素 | 结构及性质 |
A | A在第三周期中简单离子半径最小 |
B | B原子最外层电子数是内层电子数的 |
C | 使用最广泛的金属元素C能形成两种氯化物,其相对分子质量之差为35.5 |
D | D与B同主族,且通常状况下D没有正化合价 |
E | E在周期表中位于IA族,有人认为将其排在VIIA族也有一定道理 |
F | F与B同周期,其最高价氧化物的水化物与A或B的最高价氧化物的水化物均能反应 |
(1)C元素在周期表中的位置_____________;E形成的一种简单离子能支持“将E排在VIIA族”这一观点,该离子的结构示意图为_______________________。
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方法为________________________________。
E与B形成的一种化合物Z与X、Y中的一种电子总数相同且能发生化学反应,写出该反应的化学方程式__________________________(用相应化学式表示)
(3)请画出化合物F2B2的电子式__________,该化合物中含有的化学键类型是_______。
(4)将A、C的单质用导线连接后插入F的最高价氧化物的水化物溶液中可形成原电池,该原电池中阴离子移向_________(填“A”或“C”),写出该原电池总反应的离子方程式____________________。
【答案】第四周期第VIII族 ![]() 分别取两种液体少量于试管中,加入少量二氧化锰,有大量气泡冒出的是H2O2 H2O2+H2S=S↓+2H2O
分别取两种液体少量于试管中,加入少量二氧化锰,有大量气泡冒出的是H2O2 H2O2+H2S=S↓+2H2O ![]() 离子键、共价键 A 2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ (或2Al+2OH-+2H2O=2AlO2-+3H2↑)
离子键、共价键 A 2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ (或2Al+2OH-+2H2O=2AlO2-+3H2↑)
【解析】
A在第三周期中简单离子半径最小,则A是Al元素;B原子最外层电子数是内层电子数的![]() ,则B是S元素;使用最广泛的金属元素C能形成两种氯化物,其相对分子质量之差为35.5,则C是Fe元素;D与B同主族,且通常状况下D没有正化合价,则D是O元素;E在周期表中位于IA族,有人认为将其排在VIIA族也有一定道理,则E最外层只有1个电子,E是H元素;F与B同周期,其最高价氧化物的水化物与A或B的最高价氧化物的水化物均能反应,则F是Na元素。
,则B是S元素;使用最广泛的金属元素C能形成两种氯化物,其相对分子质量之差为35.5,则C是Fe元素;D与B同主族,且通常状况下D没有正化合价,则D是O元素;E在周期表中位于IA族,有人认为将其排在VIIA族也有一定道理,则E最外层只有1个电子,E是H元素;F与B同周期,其最高价氧化物的水化物与A或B的最高价氧化物的水化物均能反应,则F是Na元素。
(1) C元素是Fe元素,在周期表中的位置是第四周期第VIII族;E是H元素,形成的一种简单离子能支持“将E排在VIIA族”这一观点,是因为H原子获得一个电子变为K层2个电子的稳定结构,该离子的结构示意图为![]() ;
;
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y分别是H2O、H2O2,可利用H2O2的不稳定性来区别X、Y这两种物质,实验方法是分别取两种液体少量于试管中,加入少量二氧化锰,有大量气泡冒出的是H2O2;E与B形成的一种化合物Z是H2S,与X、Y中的一种电子总数相同的是H2O2,二者能发生氧化还原反应,该反应的化学方程式是H2O2+H2S=S↓+2H2O;
(3)化合物F2B2是Na2S2,该物质中含有非极性共价键和离子键,其电子式是![]() ;
;
(4)A是Al,C是Fe,F是Na,将A、C的单质用导线连接后插入F的最高价氧化物的水化物溶液中可形成原电池,由于Al可以与NaOH溶液反应,失去电子,所以Al为负极,Fe为正极。根据同种电荷互相排斥,异种电荷相互吸引,可知该原电池中阴离子移向正电荷较多的负极Al电极,即向A电极移动,该原电池总反应的离子方程式2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ ;或写为2Al+2OH-+2H2O=2AlO2-+3H2↑。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(夹持和净化装置省略)。仅用以下实验装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的液体 | b中的物质 | c中收集的气体 | d中的液体 |
A | 浓氨水 | 碱石灰 | NH3 | H2O |
B | 浓硝酸 | Cu | NO2 | H2O |
C | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
D | 稀硝酸 | Cu | NO | NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于反应K37ClO3+6H35Cl=KCl+3Cl2↑+3H2O的有关叙述中,正确的是( )
A. KCl中含有35ClB. KCl中含有37Cl
C. 生成物Cl2的相对分子质量大于71D. 该反应转移的电子数为6e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生产或实验事实引出的相应结论不正确的是( )
选项 | 事实 | 结论 |
A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间变短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
B | 工业制硫酸中,在SO3的吸收阶段,吸收塔里要装填瓷环 | 增大气液接触面积,使SO3的吸收速率增大 |
C | 在容积可变的密闭容器中发生反应:2NH3(g) | 正反应速率加快,逆反应速率减慢 |
D | A、B两支试管中分别加入等体积5%的H2O2,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中相关物质的信息都正确的一项是
选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
A | NaClO | 离子键、共价键 | 强氧化性 | 消毒液 |
B | H2O2 |
| 不稳定,易分解 | 医用消毒剂 |
C | NH3 | 共价键 | 水溶液呈弱碱性 | 工业制硝酸 |
D | NaHCO3 | 离子键 | 受热易分解 | 泡沫灭火器 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.久置的氯水也能使有色布条迅速褪色
B.氯气、液氯和氯水是同一种物质
C.碘化钾溶液中加淀粉溶液变蓝色
D.二氧化硅是制备光导纤维的材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)![]() CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是

A. 反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的ΔH>0
CO2(g)+H2(g)的ΔH>0
B. 在T2时,若反应处于状态D,则一定有ν正<ν逆
C. 平衡状态A与C相比,平衡状态A的c(CO)小
D. 若T1、T2时的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解Na2SO4溶液产生H2SO4和烧碱的装置如下图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1∶2。以下说法正确的是(说明:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)
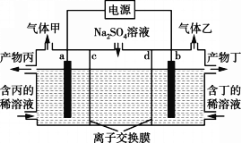
A. 产物丁为H2SO4
B. a电极反应式:2H2O+2e-=H2↑+2OH-
C. 离子交换膜d为阳离子交换膜
D. 每转移0.2 mol电子,产生1.12 L气体甲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com