
A、 分液 |
B、 过滤 |
C、 转移溶液 |
D、 蒸馏 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、电化学反应不一定是氧化还原反应 |
| B、pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
| C、根据某反应的△H<0,判断该反应在此条件下一定能自发进行 |
| D、已知BaSO4和BaCO3的Ksp相近.用饱和Na2CO3溶液处理BaSO4沉淀,可将BaSO4转化为BaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
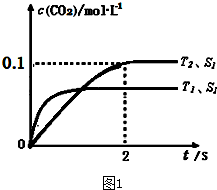
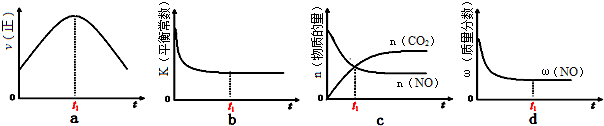
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中AgCl不再溶解 |
| B、AgCl难溶于水,溶液中没有Ag+和Cl- |
| C、升高温度,AgCl沉淀的溶解度增大 |
| D、向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解的量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)0.4molNH4ClO4含有氧原子数为
(1)0.4molNH4ClO4含有氧原子数为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、降低体系温度 |
| B、恒容,充入N2 |
| C、恒容,充入He |
| D、恒压,充入He |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Cu2+)增大 |
| B、c(Cu2+)减小 |
| C、c(Cu2+)不变 |
| D、无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com