
分析 根据平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积,书写平衡常数,固体物质的浓度看作1,据此答题.
解答 解:平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积,
反应①C(s)+H2O(g)?CO(g)+H2(g)平衡常数K=$\frac{c({H}_{2})c(CO)}{c({H}_{2}O)}$,
反应②2SO2(g)+O2?2SO3(g) 平衡常数K1=$\frac{{c}^{2}(S{O}_{3})}{c({O}_{2}){c}^{2}(S{O}_{2})}$,
反应③SO2(g)+$\frac{1}{2}$O2?SO3(g) 平衡常数K2=$\frac{c(S{O}_{3})}{c(S{O}_{2}){c}^{\frac{1}{2}}({O}_{2})}$,
反应②×$\frac{1}{2}$=反应③,所以K1=K22,
故答案为:$\frac{c({H}_{2})c(CO)}{c({H}_{2}O)}$;$\frac{{c}^{2}(S{O}_{3})}{c({O}_{2}){c}^{2}(S{O}_{2})}$;$\frac{c(S{O}_{3})}{c(S{O}_{2}){c}^{\frac{1}{2}}({O}_{2})}$;K1=K22.
点评 本题考查化学平衡常数的意义,和平衡常数的书写、及综合应用,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c=$\frac{1000W}{aV}$mol/L | B. | c(Cl-)=$\frac{10dW}{a}$mol/L | C. | ω%=$\frac{100W}{dV}$% | D. | S=$\frac{100W}{dV-W}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
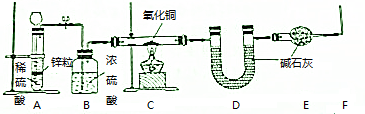
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷(解析版) 题型:填空题
在一定温度下,向一固定容积的密闭容器中加入 1mol A和 2mol B,发生下述反应:A(g)+2B(g) 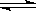 3C(g)+2D(s) △H>0。达到平衡时生成
3C(g)+2D(s) △H>0。达到平衡时生成 了1.8 mol C。
了1.8 mol C。
(1)在相同条件下,若向该容器中改为加入0.3mol A、0.6 mol B,要使平衡混合气体中C物质的体积分数与原平衡的相同,在D足量时,则还应加入 mol的物质C。
(2)若维持容器的体积和温度不变,反应从逆反应方向开始,按不同的配比作为起始物质,达到平衡时C仍为1.8 mol 。则D的起始物质的量n(D)应满足的条件是:n(D)___________。
当改变温度或压强时,有可能改变物质的聚集状态,对平衡产生影响。回答(3)(4)
(3)若升高平衡体系温度,当再次达到平衡后,测得两次平衡条件下混合气体的平均相对分子质量未发生改变,试解释形成这种结果的可能原因是:_________________;
(4)若将容器改为容积可变的容器,在一定温度和常压下,建立上述平衡之后,A的物质的量浓度为a mol/L。现持续增大压强,当:
①当压强为原来1.5倍时,A的平衡时物质的量浓度为m mol/L,测得m=1.5a;
②当压强为原来10倍时,A的平衡时物质的量浓度为n mol/L,测得n >10 a;
③当压强为原来100倍时,A的平衡时物质的量浓度为p mol/L,测得p<100a。
试解释形成这种结果的可能的原因:
①1.5倍时: ;
②10倍时: ;
③100倍时:  。
。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷(解析版) 题型:选择题
常温时,下列叙述正确的是
A.稀释pH=3的醋酸,溶液中所有离子的浓度均降低
B.一定浓度的CH3COOH和NaOH混合,溶液呈中性,则混合液中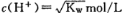
C.pH均为11的NaOH和NH3·H2O溶液中,水的电离程度不相同
D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
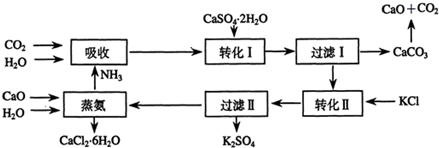
| 所含离子 | 检验方法 |
| K+ | 取少量滤液于试管中,通过焰色反应,火焰呈紫色(透过蓝色钴玻璃) |
| NH4+ | 取少量滤液于试管中,并向其中加入NaOH微热,有刺激性气味产生(该气体可使湿润红色石蕊试纸变蓝) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石转化成石墨是自发进行的过程 | |
| B. | 石墨转化成金刚石是自发进行的过程 | |
| C. | 石墨和金刚石能量一样高 | |
| D. | 金刚石比石墨能量低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com