
(14分)红磷P(s)和Cl2 (g)发生反应生成PCl3(g)和 PCl5(g),反应过程如下。
2P(s) + 3Cl2(g) = 2PCl3(g) △H=-612kJ/mol
2P(s) + 5Cl2(g) = 2PCl5(g) △H=-798kJ/mol
请回答下列问题。
(1)气态 PCl5生成气态PCl3和Cl2的热化学方程式为 。
(2)PC15生成 PCl3和Cl2是一个可逆反应,向5.0L密闭容器中充入0.1 md PCl5(g),反应在不同条件下进行,反应体系总压强随时间的变化关系如图所示。
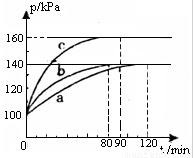
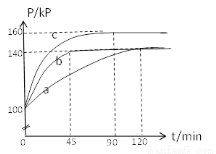
①实验b中PCl5的平衡分解率为 ,其他条件不变,在该实验中再加入 0.1 mol PCl5 (g) ,平衡分解率 (填“增大”、“减小”或“不变”)。
②与实验a相比,c改变的条件是 ,判断依据是 。
(3)PCl5露置于潮湿空气中,能水解生成两种中学化学常见酸,其化学方程式为 。
(4)人的牙齿表面有一层釉质,其组成为羟基磷灰石 Ca5( PO4)3OH(Ksp=6.8×10-37)。为了防止蛀牙,人们常使用含氟离子的牙膏,其中的氟化物可使轻基磷灰石转化为氟磷灰石Ca5( PO4)3F(Ksp=1.0×10-60)。写出该反应的离子方程式 ,该反应的平衡常数为 。
科目:高中化学 来源:2014-2015内蒙古北方重工业集团三中高一下学期第一次月考化学试卷(解析版) 题型:选择题
在标准状况下,mgA气体与ngB气体分子数相等,下列说法不正确的是
A.标准状况下,同体积的气体A和气体B的质量比m∶n
B.25℃时,1Kg气体A与1Kg气体B的分子数之比为n∶m
C.同温同压下,气体A与气体B的密度之比为n∶m
D.标准状况下,等质量的A与B的体积比为n∶m
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
一定条件下,分别对反应A(s)+B(g) 2C(g) (正反应吸热)进行如下操作(只改变该条件):
2C(g) (正反应吸热)进行如下操作(只改变该条件):
①增大A的用量 ②缩小容器的容积 ③升高体系温度 ④减小体系中C的量
上述措施中一定能使正反应速率加快的是
A.①③ B.②③ C.①②③ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省高一3月月考化学试卷(解析版) 题型:选择题
某学习小组进行了下图所示的实验,实验后组员之间的交流不合理的是

A.甲同学认为试管b中收集到的气体可点燃,且产生淡蓝色 火焰
B.乙同学认为试管a中生成的黑色固体可能为四氧化三铁
C.丙同学认为可用盐酸和KSCN溶液来验证产物中的三价铁
D.丁同学认为将少量还原性铁粉放入试管中,加适量的水,加热也可实现该反应
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省高一3月月考化学试卷(解析版) 题型:选择题
下列推断正确的是
选项 | 事实 | 结论 |
A | SiO2可用于制光导纤维 | SiO2有导电性 |
B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
C | Cl2的水溶液可以导电 | Cl2是电解质 |
D | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市高二3月月考化学试卷(解析版) 题型:选择题
一定温度下,向300 mL l mol/L的NaOH溶液中通入bmol CO2,下列说法正确的是
A.通入CO2过程中溶液中的Kw减小
B.b=0.3与b=0.15时,所得溶液中的微粒种类不相同
C.当b=0.2时,所得溶液中部分离子浓度关系为:c(HCO3一)>c(CO32-)>c(OH-)>c(H+)
D.当恰好生成NaHCO3时,溶液中存在:c(Na+ )+c(H十)=c(HCO3-)+c(OH一)
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市高二3月月考化学试卷(解析版) 题型:选择题
下列说法正确的是

A.钛和钾都采取图1的堆积方式
B.图2为金属原子在二维空间里的非密置层放置,此方式在三维空间里堆积,仅得简单立方堆积
C.图3是干冰晶体的晶胞,晶胞棱长为a cm,则在每个CO2 周围距离相等且为 的CO2有8个
的CO2有8个
D.图4这种金属晶体的晶胞,是金属原子在三维空间里以密置层采取ABCABC…堆积的结果
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省梅州市高三高三总复习质检理综化学试卷(解析版) 题型:选择题
能在水溶液中大量共存的一组离子是
A.H+、Ca2+、I-、NO3- B.Al3+、Mg2+、SO42-、CO32-
C.NH4+、Na+、Br-、SO42- D.K+、Fe2+、OH-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省郑州市高三第二次质量预测理综化学试卷(解析版) 题型:实验题
(14分)铜、铬都是用途广泛的金属。工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收金属铜和铬的流程如下图:

已知:部分物质沉淀的pH如下表:
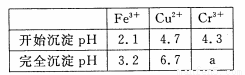
CaSO4的溶解度曲线如图:
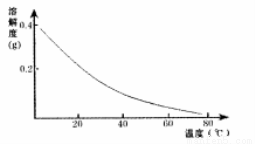
请回答下列问题:
(1)滤液I中所含溶质主要有 (填化学式)。
(2)第②步操作中,先加人Ca(OH)2调节溶液的pH,调节范围为____,然后将浊液加热至80 ℃ 趁热过滤,所得滤渣Ⅱ的成分为 。
(3)第③步操作中,发现除了生成砖红色沉淀外,还产生了无色刺激性气味的气体。写出该步骤中发生反应的离子方程式
(4)当离子浓度≤1× 10-5mol· L-1 l时,可以认为离子沉淀完全。第④步操作中,若要使Cr3+完全沉淀,则室温下溶液中a的最小值为 。(已知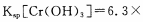
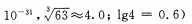
(5)Cr(OH)3受热分解为Cr2O3,用铝热法可以冶炼金属铬。写出铝热法炼铬的化学方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com