
| A、若M1>M2,平衡右移,△H<0 |
| B、若M1<M2,平衡右移,△H>0 |
| C、若M1>M2,平衡左移,△H>0 |
| D、若M1<M2,平衡左移,△H<0 |
| 气体质量总和 |
| 气体物质的量总和 |
| 气体质量总和 |
| 气体物质的量总和 |


科目:高中化学 来源: 题型:
| A、35g |
| B、30 g |
| C、20 g |
| D、15 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
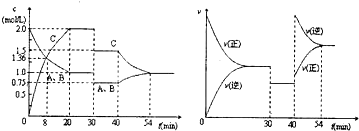
| A、该反应可以表示为A(g)+B(g)?2C(g),△H>0 |
| B、从反应开始到40min,反应物B的转化率为62.5% |
| C、30min后研究的是压强对反应速率和化学平衡的影响,40min后则是温度的影响 |
| D、在20min-30min,30min-40min的反应的平衡常数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )
可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )| A、m+n<p |
| B、m+n>p |
| C、增大压强平衡向正反应方向移动 |
| D、升高温度平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、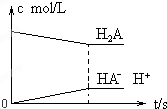 |
C、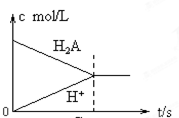 |
D、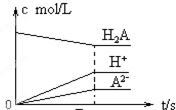 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH |
| B、NaHCO3 |
| C、CH3COOK |
| D、Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:
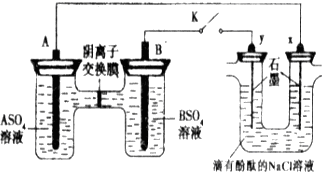
| A、A的金属活动性弱于B |
| B、Na+从y电极趋向x电极 |
| C、Y电极附近溶液先变红 |
| D、B的电极反应:B-2e-=B2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液态HCl不导电,所以HCl是非电解质 |
| B、NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质 |
| C、铜、石墨均导电,所以它们都是电解质 |
| D、蔗糖在水溶液中或熔融时均不导电,所以是非电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com