
某溶液,只可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、NO2-、CO32-、NO3-,现取两份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g;
②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体;
③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用50mL0.5mol·L-1的硫酸溶液恰好完全吸收,酸也不剩余。
根据上述实验,以下推测不正确的是
| A.原溶液一定不存在较大浓度的H+、Mg2+ |
| B.原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5︰2︰1 |
| C.不能确定原溶液是否含有K+、NO3- |
| D.实验中产生的棕色气体遇空气颜色会加深 |
C
解析试题分析:第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g,这说明该白色沉淀中一定含有亚硝酸银,亚硝酸银与盐酸反应生成氯化银与亚硝酸,亚硝酸不稳定分解生成NO、NO2和水。所以原溶液中一定含有NO2-,则氢离子一定不能大量共存。将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体,则该白色沉淀应该是碳酸钙,物质的量是0.01mol,所以气体中含有CO2,这说明反应①中生成的白色沉淀一定有碳酸银,则原溶液中一定含有CO32-。因此Mg2+就一定不能大量共存。根据碳原子守恒,CO32-的物质的量是0.01mol。5.84g沉淀中亚硝酸银沉淀的质量=5.84g-0.01mol×276g/mol=3.08g,因此亚硝酸银的物质的量=3.08g÷154g/mol=0.02mol,则原溶液中NO2-的物质的量是0.02mol。第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,该气体一定是氨气,因此原溶液中含有NH4+。用50mL0.5mol/L的硫酸溶液恰好完全吸收,酸也不剩余,硫酸的物质的量是0.025mol,则氨气的物质的量是0.025mol×2=0.05mol,则原溶液中NH4+的物质的量是0.05mol,所以原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5︰2︰1,因此选项A、B正确。根据电荷守恒可知,原溶液中一定还含有NO3-,但K+不能确定,C不正确;实验中产生的棕色气体中含有NO,遇空气生成红棕色NO2,所以颜色会加深,D正确,答案选C。
考点:考查考查离子共存、离子检验的有关判断


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:单选题
下列离子或分子在溶液中能大量共存,通入CO2后仍能大量共存的一组是
| A.K+、Ca2+、F-、NO3- | B.K+、Ba2+、Br-、NO3- |
| C.Na+、K+、CO32-、HCO3- | D.Na+、Ag+、NH3·H2O、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
能正确表示下列反应的离子方程式是
A.向0.1mol/L的Na2S溶液中加入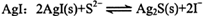 |
B.碳酸钠溶液显碱性的原因: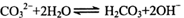 |
C.二氧化硫通入氯化铁溶液: |
D.用醋酸清洗盛放石灰水试剂瓶内壁出现的白色固体: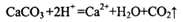 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列粒子一定能大量共存于指定的分散系中的是
A.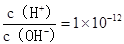 的溶液:K+、Cl-、SO32-、SiO32- 的溶液:K+、Cl-、SO32-、SiO32- |
| B.空气中:CO2、NO、SO2、CH4 |
| C.氢氧化铝胶体中:Cl-、HClO、Na+、SO32- |
| D.加入铝粉放出大量氢气的溶液:Fe2+、Na+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列各组离子或分子在指定溶液中能大量共存的是( )
| A.氨水中:NH4+、Fe2+、SO42-、HSO3- |
| B.pH=l的溶液中:、Mg2+、Fe3+、Cl-、NO3- |
| C.通入足量CO2的溶液中:Ca2+、Na+、SiO32-、CO32- |
| D.由水电离出的c(OH-)=1×10—12mol·L—1的溶液中:NH4+、HCO3-、Na+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式正确的是( )
A.小苏打溶液中加入少量石灰水:HCO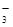 +Ca2++OH-=CaCO3↓+H2O +Ca2++OH-=CaCO3↓+H2O |
B.稀硝酸中加入过量铁粉: Fe+4H++NO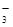 =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| C.溴化亚铁溶液中通入足量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
D.苯酚钠溶液中通入少量二氧化碳: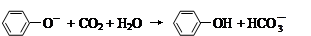 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有一瓶无色溶液,可能含有Na+、K+、Al3+、Mg2+、NH4+、Cl?、SO42?、HCO3?、MnO4?中的几种。为确定其成分,进行如下实验:①取少许溶液,逐渐加入过量的Na2O2固体,产生无色无味的气体和白色沉淀且白色沉淀逐渐增多而后又部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生;③用洁净的铂丝蘸取原溶液在酒精灯上灼烧,观察到黄色火焰。下列推断正确的是
| A.肯定有 Na+、Al3+、Mg2+、SO42? | B.肯定有 Na+、Al3+、Mg2+、Cl? |
| C.肯定没有K+、HCO3?、MnO4? | D.肯定没有K+、NH4+、Cl? |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com