
| 粒子代号 | A | B | C | D | E | F | G |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
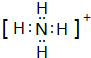 .
.分析 A、B、C、D、E、F、G都是由短周期元素构成的粒子,它们都有10个电子.A为单核,电荷为0,则A为Ne原子;B为单核,电荷为1+,则B为Na+;C为双核,电荷为1-,则C为OH-;D为多核,D是由极性键构成的4原子极性分子,电荷为0,则D为NH3;E为单核,电荷为2+,则E为 Mg2+;F为多核,电荷为1+,C常用作F的检验(加热),则F为NH4+;G为多核,电荷为0,则G为CH4,据此解答.
解答 解:A、B、C、D、E、F、G都是由短周期元素构成的粒子,它们都有10个电子.A为单核,电荷为0,则A为Ne原子;B为单核,电荷为1+,则B为Na+;C为双核,电荷为1-,则C为OH-;D为多核,D是由极性键构成的4原子极性分子,电荷为0,则D为NH3;E为单核,电荷为2+,则E为 Mg2+;F为多核,电荷为1+,C常用作F的检验(加热),则F为NH4+;G为多核,电荷为0,则G为CH4.
(1)F为NH4+,电子式为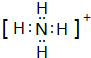 ,故答案为:
,故答案为: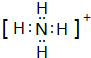 ;
;
A为Ne原子,核外电子数为10,有2个电子层,最外层电子数为8,结构示意图为其结构示意图为: ,故答案为:
,故答案为: ;
;
(2)BC为NaOH,EC2为Mg(OH)2,金属性Na>Mg,所以碱性NaOH>Mg(OH)2,故答案为:>;
(3)F为NH4+,C为OH-,NH4+与OH-在溶液中反应生成NH3.H2O,离子方程式为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,
故答案为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
点评 本题考查无机物推断,熟练掌握中学常见10电子、18电子微粒,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 它的中子数是175 | B. | 它是第七周期元素 | ||
| C. | 它是活泼的金属元素 | D. | 它的最外层电子数是8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++Al3++2 SO42-+4OH-═AlO2-+2BaSO4↓+2H2O | |
| C. | 在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | NH4HCO3溶液中加入过量NaOH溶液并加热:NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,K+、OH-、S2-、NO3-能大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,离子方程式为:2Fe2++ClO-+2H+→Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)>c(CN-)>c(H+)>c(OH-) | B. | c(HCN)+c(CN-)=0.04 mol•L-1 | ||
| C. | c(Na+)+c(H+)=c(CN-)+c(OH-) | D. | c(CN-)>c(HCN) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
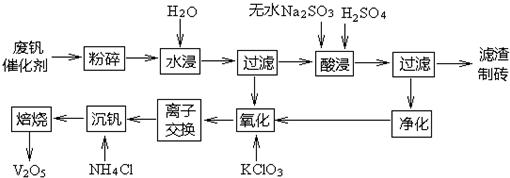
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人体不能缺碘,需要正常补碘.“加碘食盐”中的“碘”是指碘元素 | |
| B. | 进行焰色反应实验时,蘸取样品之前需要用稀硫酸溶液清洗铂丝 | |
| C. | “绿色化学”的理想在于不再使用有毒、有害的物质,不再产生废物 | |
| D. | 水壶中产生的水垢可用食醋清洗除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com