
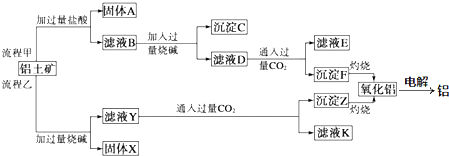
分析 根据工艺流程甲可知,铝土矿与盐酸反应时,SiO2和盐酸不反应,则固体A为SiO2,滤液B含有氯化铝、氯化铁等,滤液中加入过量的NaOH,可推知沉淀C为氢氧化铁,滤液D含有偏铝酸钠、氯化钠,向滤液D中通入过量二氧化碳,生成氢氧化铝沉淀与碳酸氢钠,沉淀F为Al(OH)3,滤液E中含有NaCl、NaHCO3,氢氧化铝分解得到氧化铝;
根据工艺流程乙可知,铝土矿中的Al2O3、SiO2能和氢氧化钠反应,可知固体X为Fe2O3,滤液Y为硅酸钠、偏铝酸钠,滤液中通入过量二氧化碳,沉淀Z为Al(OH)3、硅酸,滤液K中含有NaHCO3.
(1)加入过量盐酸后的实验操是将不溶的固体与溶液分离;
(2)固体A为二氧化硅,可以制光纤、饰品、制硅、制玻璃等;
(3)溶液在氯化铝与氢氧化钠反应生成偏铝酸钠与水;
(4)Al与氧化铁在高温下反应生成Fe与氧化铝;
(5)根据Al元素守恒计算.
解答 解:根据工艺流程甲可知,铝土矿与盐酸反应时,SiO2和盐酸不反应,则固体A为SiO2,滤液B含有氯化铝、氯化铁等,滤液中加入过量的NaOH,可推知沉淀C为氢氧化铁,滤液D含有偏铝酸钠、氯化钠,向滤液D中通入过量二氧化碳,生成氢氧化铝沉淀与碳酸氢钠,沉淀F为Al(OH)3,滤液E中含有NaCl、NaHCO3,氢氧化铝分解得到氧化铝;
根据工艺流程乙可知,铝土矿中的Al2O3、SiO2能和氢氧化钠反应,可知固体X为Fe2O3,滤液Y为硅酸钠、偏铝酸钠,滤液中通入过量二氧化碳,沉淀Z为Al(OH)3、硅酸,滤液K中含有NaHCO3.
(1)加入过量盐酸后的实验操是将不溶的固体与溶液分离,应采取过滤方法分离,
故答案为:过滤;
(2)由上述分析可知,A为SiO2,可以用于生产玻璃、制备光导纤维等,
故答案为:SiO2;生产玻璃、制备光导纤维等;
(3)溶液在氯化铝与氢氧化钠反应生成偏铝酸钠与水,反应离子方程式为:Al3++4OH-═AlO2-+2H2O,
故答案为:Al3++4OH-═AlO2-+2H2O;
(4)Al与氧化铁在高温下反应生成Fe与氧化铝,反应方程式为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,
故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;
(5)根据Al元素守恒,可以制得Al的质量为氧100吨×51%×$\frac{54}{102}$=27吨,
故答案为:27.
点评 本题以氧化铝提取工艺流程为载体,考查无机物推断、元素化合物性质及相互转化、除杂的方法、离子方程式、化学计算等,难度中等,熟练掌握元素化合物的性质.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | c(Z)=0.45mol/L | B. | c(X2)=0.3mol/L c(Z)=0.1 mol/L | ||
| C. | c(X2)=0.5mol/L | D. | c(Y2)=0.9mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 己二酸是合成高分子化合物尼龙-66的原料.某学习小组拟在实验室以环己醇为原料制备己二酸.反应原理如下:
己二酸是合成高分子化合物尼龙-66的原料.某学习小组拟在实验室以环己醇为原料制备己二酸.反应原理如下: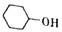 +8HNO3$\stackrel{一定条件}{→}$3HOOC(CH3)4COOH+8NO↑+7H2O
+8HNO3$\stackrel{一定条件}{→}$3HOOC(CH3)4COOH+8NO↑+7H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤燃烧时,化学能主要转化为热能 | |
| B. | 白炽灯工作时,电能转化为光能 | |
| C. | 电解水生成氢气和氧气时,化学能转化为电能 | |
| D. | 绿色植物进行光合作用时,太阳能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
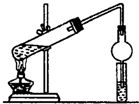 某同学用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图所示.
某同学用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com