
消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________ (填序号)。
A.Cl2 B.H2O2
C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O+H2O2===A+NH3↑,则生成物A的化学式为________,H2O2被称为“绿色氧化剂”的理由是_________________________________________。
(3)漂白剂亚氯酸钠(NaClO2)在常温下、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子数约为________。
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是__________________________________(用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:______________________________。
解析 (2)根据原子守恒原理,可知反应KCN+H2O2+H2O===A+NH3↑中的A为KHCO3。在反应中,H2O2是氧化剂,其产物H2O没有污染性。(3)该反应是歧化反应,HClO2中+3价的氯元素一部分升高到ClO2中的+4价,一部分降低到-1价。当有1 mol ClO2生成时,反应中转移1 mol电子,即转移的电子数约为6.02×1023。(4)ClO-与浓盐酸中的Cl-会发生归中反应生成有毒的Cl2。氯碱工业的产物是NaOH、H2和Cl2,NaOH溶液和Cl2发生歧化反应可以得到含有NaClO的溶液。
答案 (1)C
(2)KHCO3 H2O2是氧化剂,其产物是H2O,没有污染
(3)6.02×1023(或NA)
(4)ClO-+Cl-+2H+===Cl2↑+H2O Cl2+2NaOH===NaClO+NaCl+H2O


科目:高中化学 来源: 题型:
已知:C(s)+CO2(g)2CO(g) ΔH>0。该反应达到平衡后,下列条件有利于反应向正反应方向进行的是( )
A.升高温度和减小压强
B.降低温度和减小压强
C.降低温度和增大压强
D.升高温度和增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )。
A.食用白糖的主要成分是蔗糖
B.淀粉、纤维素和油脂都属于天然高分子化合物
C.植物油的主要成分是高级脂肪酸
D.蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖
查看答案和解析>>
科目:高中化学 来源: 题型:
水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O +O2+xOH-===Fe3O4+S4O
+O2+xOH-===Fe3O4+S4O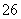 +2H2O,下列说法中错误的是 ( )。
+2H2O,下列说法中错误的是 ( )。
A.每生成1 mol Fe3O4,反应转移的电子总数为4 mol
B.Fe2+和S2O 都是还原剂
都是还原剂
C.1 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为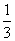 mol
mol
D.x=4
查看答案和解析>>
科目:高中化学 来源: 题型:
锑(Sb)在自然界一般以硫化物的形式存在。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:
2Sb2S3+3O2+6Fe===Sb4O6+6FeS ①
Sb4O6+6C===4Sb+6CO ②
关于反应①、反应②的说法正确的是 ( )。
A.反应①②中的氧化剂分别是Sb2S3、Sb4O6
B.反应①中每生成3 mol FeS时,共转移6 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成1 mol Sb时,反应①与反应②中氧化剂的物质的量之比为1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
金属原子在二维空间里的放置如图所示的两种方式,下列说法中正确的是 ( )。
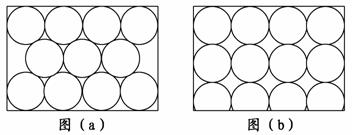
A.图(a)为非密置层,配位数为6
B.图(b)为密置层,配位数为4
C.图(a)在三维空间里堆积可得六方最密堆积和面心立方最密堆积
D.图(b)在三维空间里堆积仅得简单立方
查看答案和解析>>
科目:高中化学 来源: 题型:
 金晶体的最小重复单元(也称晶胞)是面心立方体,如图所示即在立方体的8个顶点各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞所共有。金原子的直径为d cm,用NA表示阿伏加德罗常数的值,M表示金的相对原子质量。
金晶体的最小重复单元(也称晶胞)是面心立方体,如图所示即在立方体的8个顶点各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞所共有。金原子的直径为d cm,用NA表示阿伏加德罗常数的值,M表示金的相对原子质量。
(1)金晶体每个晶胞中含有________个金原子。
(2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定________。
(3)一个金晶胞的体积是多少?
(4)金晶体的密度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家把药物连在高分子载体E上制成缓释长效药剂。阿司匹林
(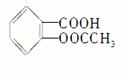 )可连接在某高分子聚合物上,形成缓释长效药剂,其中一种结构简式为:
)可连接在某高分子聚合物上,形成缓释长效药剂,其中一种结构简式为:
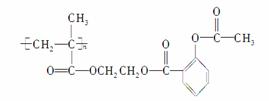
试回答下列问题:
(1)载体结构简式为________________________________。
(2)缓释反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(3)阿司匹林在碱性条件下(NaOH)发生水解反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(4)这种高分子载体是由单体发生聚合反应得到的,写出单体的结构简式:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨反应为:N2(g)+3H2(g)2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化。图2表示在2 L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。

下列说法正确的是 ( )。
A.该反应为自发反应,由图1可得加入适当的催化剂,E和ΔH都减小
B.图2中0~10 min内该反应的平均速率v(H2)=0.045 mol·L-1·min-1,从11 min起其他条件不变,压缩容器的体积为1 L,则n(N2)的变化曲线为d
C.图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点
D.图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com