(2013?盐城一模)多晶硅是太阳能光伏产业的重要原材料.
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
SiO
2(s)+C(s)═SiO(g)+CO(g),△H=akJ?mol
-12SiO(g)═Si(s)+SiO
2(s),△H=bkJ?mol
-1①反应SiO
2(s)+2C(s)═Si(s)+2CO(g)的△H=
2a+b
2a+b
kJ?mol
-1(用含a、b的代数式表示);
②SiO是反应过程中的中间产物,隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式为
SiO+2NaOH═Na2SiO3+H2
SiO+2NaOH═Na2SiO3+H2
.
(2)粗硅提纯常见方法之一是先用粗硅与HCl反应,制得SiHCl
3,经提纯后再用H
2还原:SiHCl
3(g)+H
2(g)?Si(s)+3HCl(g).不同温度及不同
时,反应物X的平衡转化率关系如图1.
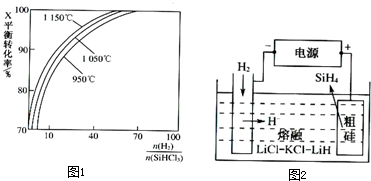
①X是
SiHCl3
SiHCl3
(填化学式);
②上述反应的平衡常数:K(1150℃)
>
>
K(950℃)(填“>”、“<”或“=”).
(3)SiH
4(硅烷)法生产高纯多晶硅是非常优异的方法.
①用粗硅做原料,熔盐电解法制取硅烷原理如图2所示,电解时阳极的电极反应式为
Si+4H+-4e-═SiH4↑
Si+4H+-4e-═SiH4↑
.
②硅基太阳能电池需用N、Si两种元素组成的化合物Y做钝化材料,它可由SiH
4与NH
3混合气体进行气相沉积得到.已知Y中Si的质量分数为60%,Y的化学式为
Si3N4
Si3N4
.



