
ŅŃÖŖ25”ęŹ±Ä³ČÜŅŗÖŠŗ¬ÓŠ“óĮæNa+”¢H+”¢Fe3+”¢HC03©”¢OH©”¢I©ÖŠµÄ¼øÖÖ£¬²¢ĒŅĖ® µēĄė³öµÄc£ØH+£©=1”ĮlO©13 mol/L£®µ±ĻņøĆČÜŅŗÖŠ»ŗĀżĶØČėŅ»¶ØĮæµÄCl2ŗó£¬ČÜŅŗÓÉĪŽÉ« ±äĪŖ»ĘÉ«£®ĻĀĮŠÓŠ¹Ų·ÖĪöÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | ČÜŅŗµÄpH=1»ņ13 | B£® | ČÜŅŗÖŠŅ»¶ØƻӊFe3+£¬Na+ |
| ”” | C£® | ČÜŅŗÖŠŅõĄė×ÓÓŠI©£¬²»ÄÜČ·¶ØHCO3© | D£® | µ±Cl2¹żĮ棬ĖłµĆČÜŅŗÖ»ŗ¬ÓŠĮ½ÖÖŃĪ |
| ³£¼ūĄė×ӵļģŃé·½·Ø£® | |
| ×ØĢā£ŗ | Ąė×Ó·“Ó¦×ØĢā£® |
| ·ÖĪö£ŗ | Ė®µēĄė³öµÄc£ØH+£©=1”ĮlO©13 mol/L£¬ČÜŅŗÖŠĒāĄė×Ó»ņĒāŃõøłĄė×ÓÅضČĪŖ0.1mol/L£¬øĆČÜŅŗĪŖĒæĖįŠŌ»ņ¼īŠŌČÜŅŗ£¬Ņ»¶Ø²»»į“ęŌŚĢ¼ĖįĒāøłĄė×Ó£»µ±ĻņøĆČÜŅŗÖŠ»ŗĀżĶØČėŅ»¶ØĮæµÄCl2ŗó£¬ČÜŅŗÓÉĪŽÉ«±äĪŖ»ĘÉ«£¬ĖµĆ÷ČÜŅŗÖŠŅ»¶Ø“ęŌŚµāĄė×Ó£¬Äܹ»ÓėµāĄė×Ó·“Ó¦µÄĢśĄė×ÓŅ»¶Ø²»»į“ęŌŚ£¬¾Ż“ĖĶź³É±¾Ģā£® |
| ½ā“š£ŗ | ½ā£ŗÓÉĖ®µēĄė³öµÄc£ØH+£©=1”ĮlO©13 mol/L£¬øĆČÜŅŗÖŠ“óĮæ“ęŌŚĒāĄė×Ó»ņÕßĒāŃõøłĄė×Ó£¬ĖłŅŌČÜŅŗÖŠŅ»¶Ø²»»į“ęŌŚĢ¼ĖįĒāøłĄė×Ó£»ĶØČėĀČĘųŗóČÜŅŗÓÉĪŽÉ« ±äĪŖ»ĘÉ«£¬ĖµĆ÷ČÜŅŗÖŠŅ»¶Ø²»»į“ęŌŚÓŠÉ«µÄĢśĄė×Ó£¬Ņ»¶Ø“ęŌŚµāĄė×Ó£¬ A”¢øł¾Ż·ÖĪöæÉÖŖ£¬Ė®µēĄė³öµÄc£ØH+£©=1”ĮlO©13 mol/L£¬ČōĪŖĖįŠŌČÜŅŗ£¬øĆČÜŅŗpH=1£»ČōĪŖ¼īŠŌČÜŅŗ£¬øĆČÜŅŗµÄpHĪŖ13£¬¹ŹAÕżČ·£» B”¢ČÜŅŗÖŠŅ»¶Ø²»»į“ęŌŚĢśĄė×Ó£¬ČōŹĒ¼īŠŌČÜŅŗ£¬Ņ»¶Ø“ęŌŚÄĘĄė×Ó£¬¹ŹB“ķĪó£» C”¢øĆČÜŅŗÖŠŅ»¶Ø“ęŌŚµāĄė×Ó£¬Ņ»¶Ø²»»į“ęŌŚĢ¼ĖįĒāøłĄė×Ó£¬¹ŹC“ķĪó£» D”¢ĀČĘų¹żĮ棬·“Ó¦ŗóÖ»ÓŠŅ»ÖÖŃĪ£¬¼“ĀČ»ÆÄĘ£¬¹ŹD“ķĪó£» ¹ŹŃ”A£® |
| µćĘĄ£ŗ | ±¾Ģāæ¼²éĮĖ³£¼ūĄė×ӵļģŃé·½·Ø£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāĆ÷Č·³£¼ūĄė×ӵķ“Ó¦ĻÖĻó¼°¼ģŃé·½·Ø£¬ŹŌĢāÓŠĄūÓŚÅąŃųѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°Įé»īÓ¦ÓĆĖłŃ§ÖŖŹ¶µÄÄÜĮ¦£® |
””


 ĆūŹ¦½šŹÖÖøĮģĻĪæĪŹ±ĻµĮŠ“š°ø
ĆūŹ¦½šŹÖÖøĮģĻĪæĪŹ±ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĶʶĻÕżČ·µÄŹĒ
A£®ÓÉH+(aq)+OH-(aq)=H20£Ø1£© ”÷H=-57£®3 kJ”¤mol-1£¬æÉÖŖŗ¬1 mo1 CH3COOHµÄČÜŅŗÓėŗ¬1 mol NaOHµÄČÜŅŗ»ģŗĻ£¬·Å³öČČĮæĪŖ57£®3 kJ
B£®ÓÉC(ŹÆÄ«)=C(½šøÕŹÆ) ”÷H=+1£®9 kJ”¤mol-1£¬æÉÖŖŹÆÄ«±Č½šøÕŹÆøüĪȶØ
C£®ÓÉN2(g)+3H2(g)=2NH3(g) ”÷H=-92£®4 kJ”¤mol-1£¬æÉÖŖ½«1 mol N2(g)ŗĶ3 mol H2(g)ÖĆÓŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ó¦ŗó·Å³öČČĮæĪŖ92£®4 kJ
D£®ÓÉ”÷G£½”÷H-T”÷SæÉÖŖ£¬ĖłÓŠµÄ·ÅČČ·“Ó¦¶¼ÄÜ×Ō·¢½ųŠŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | »Æѧ¼üµÄ¶ĻĮŃŗĶŠĪ³ÉŹĒ»Æѧ·“Ó¦µÄŹµÖŹ£¬»Æѧ·“Ó¦Ē°ŗóÄÜĮæ²»±ä |
| ”” | B£® | ·²ŹĒ·ÅČČ·“Ó¦¶¼ŹĒ×Ō·¢µÄ£¬ĪüČČ·“Ó¦¶¼ŹĒ·Ē×Ō·¢µÄ |
| ”” | C£® | ČōŅ»øö·“Ó¦µÄĘ½ŗā³£ŹżŌ½“ó£¬Ōņ±ķŹ¾øĆ·“Ó¦ĖŁĀŹŅ²Ō½“ó |
| ”” | D£® | ÉżøßĪĀ¶Č»Æѧ·“Ó¦ĖŁĀŹŌö“ó£¬Ö÷ŅŖŌŅņŹĒŌö¼ÓĮĖ·“Ó¦Īļ·Ö×ÓÖŠ»ī»Æ·Ö×Ó°Ł·ÖŹż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
»ÆѧÓėČÕ³£Éś»īĆÜĒŠĻą¹Ų£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
”” A£® µā¾ĘÖ»ŹĒÖøµāµ„ÖŹµÄŅŅ“¼ČÜŅŗ
”” B£® “æĖ®²»Ņ×µ¼µē£¬µ«ŹōÓŚµē½āÖŹ
”” C£® ÖŹĮæ·ÖŹż£ŗŅ½ÓĆ¾Ę¾«£¾ÉśĄķŃĪĖ®£¾Ź³“×
”” D£® Ć÷·ÆæÉÓĆÓŚĖ®µÄĻū¶¾”¢É±¾ś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ·“Ó¦ÖŠ£¬·“Ó¦ŗó¹ĢĢåĪļÖŹŌöÖŲµÄŹĒ£Ø””””£©
| ”” | A£® | ĒāĘųĶعż×ĘČȵÄCuO·ŪÄ© | B£® | ¶žŃõ»ÆĢ¼ĶعżNa2O2·ŪÄ© |
| ”” | C£® | ĀĮÓėFe2O3·¢ÉśĀĮČČ·“Ó¦ | D£® | ½«ŠæĮ£Ķ¶ČėCu£ØNO3£©2ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ķłŗ¬Fe3+”¢H+”¢NO3©µÄ»ģŗĻŅŗÖŠ¼ÓČėÉŁĮæŗ¬SO32©µÄijČÜŅŗ³ä·Ö·“Ó¦ŗó£ØÉčČÜŅŗÖŠµÄĘäĖū³É·Ö²»·“Ó¦£©£¬ĻĀĮŠ±ķŹ¾øĆ»ģŗĻČÜŅŗÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ÖŠÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | 2 Fe3++SO32©+H2O”ś2 Fe2++SO42©+2 H+ |
| ”” | B£® | 2 H++SO32©”śSO2”ü+H2O |
| ”” | C£® | 2 H++2 NO3©+3 SO32©”ś3 SO42©+2 NO+H2O |
| ”” | D£® | 2 Fe3++3 SO32©+3 H2O”ś2 Fe£ØOH£©3”ż+3 SO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŹµŃéŹŅ“Óŗ¬µā·ĻŅŗ£Ø³żH2OĶā£¬»¹ŗ¬ÓŠCCl4”¢I2”¢I©£©ÖŠ»ŲŹÕµā£¬Ę䏵Ńé¹ż³ĢČēĶ¼1£ŗ
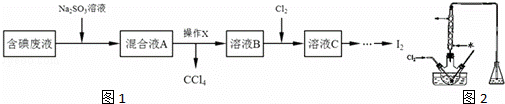
£Ø1£©Ļņŗ¬µā·ĻŅŗÖŠ¼ÓČėÉŌ¹żĮæµÄNa2SO3ČÜŅŗŹ±·¢ÉśµÄĄė×Ó·½³ĢŹ½ĪŖ””””£»øĆ²Ł×÷µÄÄæµÄŹĒ””””£®
£Ø2£©²Ł×÷XÓ¦ŌŚ””£ØĢīŠ“ŅĒĘ÷Ćū³ĘĶ¼2£©ÖŠ½ųŠŠ£¬¼ņŹöµĆµ½ČÜŅŗBµÄ¹ż³Ģ£ŗ½«»ģŗĻČÜŅŗ¾²ÖĆŗ󣬔”””
£Ø3£©ŌŚČż¾±ĘæÖŠ½«ČÜŅŗBÓĆŃĪĖįµ÷ÖĮpHŌ¼ĪŖ2£¬»ŗĀżĶØČėCl2£¬ŌŚ40˚C×óÓŅ·“Ó¦£ØŹµŃé×°ÖĆČēÓŅĶ¼ĖłŹ¾£©£®ŹµŃéæŲÖĘŌŚ½ĻµĶĪĀ¶ČĻĀ½ųŠŠµÄŌŅņŹĒ””£»×¶ŠĪĘæĄļŹ¢·ÅµÄČÜŅŗĪŖ””””£ØĢīČÜÖŹµÄ»ÆѧŹ½£©£®
£Ø4£©Ä³ŗ¬µā·ĻĖ®£ØpHŌ¼ĪŖ4£©ÖŠŅ»¶Ø“ęŌŚI2£¬æÉÄÜ“ęŌŚI©»ņIO3©£®æÉŅŌŹ¹ÓĆ””””£ØĢīČÜÖŹµÄ»ÆѧŹ½£¬ĻĀĶ¬£©ČÜŅŗ¼ģŃéæÉÄÜ“ęŌŚµÄI©»ņ””””ČÜŅŗ¼ģŃéæÉÄÜ“ęŌŚµÄIO3©£®ŌŚ¼ģŃéøĆŗ¬µā·ĻĖ®ÖŠŹĒ·ńŗ¬ÓŠI©»ņIO3©Ē°±ŲŠčŅŖ½ųŠŠµÄ²Ł×÷ŹĒ””””£ØĢīŠņŗÅ£©£®
a£®Č”ŹŹĮæŗ¬µā·ĻĖ®ÓĆCCl4¶ą“ĪŻĶČ””¢·ÖŅŗ
b£®ÓĆNaOHČÜŅŗ½«ČÜŅŗµ÷½Śµ½ÖŠŠŌ
c£®ĻņČÜŅŗÖŠµĪČėÉŁĮæµķ·ŪČÜŅŗ£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÉčNAĪŖ°¢·üŁ¤µĀĀŽ³£Źż£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ( )
A£®2.8gŅŅĻ©ŗĶ±ūĻ©µÄ»ģŗĻĪļÖŠĖłŗ¬µē×Ó×ÜŹżĪŖ1.6NA
B£®0.1L 0.1mol/LµÄ¼×Č©ČÜŅŗŗĶ×ćĮæµÄ¼īŠŌŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ·“Ó¦Ģį¹©µÄµē×ÓŹżĪŖ0.02NA
C£®0.1Ħ¶ūC10H22Ėłŗ¬¹²¼Ū¼üµÄŹżÄæĪŖ3.1NA
D£®1.7gōĒ»łĖłŗ¬µē×ÓŹżĪŖ0.9 NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijæĪĶāŠĖȤŠ”×é²ā¶ØÄ³Ę·ÅĘÅ£ÄĢÖŠøʵÄŗ¬Į棬·½·ØČēĻĀ£ŗČ”100mLÅ£ÄĢ£¬¼ÓČė×ćĮæµÄ²ŻĖįļ§[(NH4)2C2O4]ČÜŅŗ£¬Ź¹Å£ÄĢÖŠµÄøĘ×Ŗ»Æ³ÉÄŃČܵÄCaC2O4³Įµķ£»¹żĀĖ£¬ÓĆŹŹĮæµÄÕōĮóĖ®Ļ“µÓ³Įµķ±ķĆęĪüø½µÄÉŁĮæ(NH4)2C2O4”¢µ°°×ÖŹµČŌÓÖŹ£»½«³Įµķ×ŖŅĘÖĮ׶ŠĪĘæÖŠ£¬¼Ó×ćĮæµÄĻ”ĮņĖįČÜŅŗČܽāCaC2O4£»Č»ŗóŅŌ0.10mol・L£1µÄKMnO4ČÜŅŗµĪ¶ØÉś³ÉµÄH2C2O4ČÜŅŗ£¬¹²ĻūŗÄ12.00mLKMnO4ČÜŅŗ”£·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
5H2C2O4£«2KMnO4£«3H2SO4 = 5CO2”ü£«2MnSO4£«K2SO4£«8H2O
£Ø1£©KMnO4ČÜŅŗÓ¦Ź¢ŌŚ_________£ØĢī”°ĖįŹ½”±»ņ”°¼īŹ½”±£©µĪ¶Ø¹ÜÖŠ”£
£Ø2£©ČōµĪ¶Ø¹ÜµÄ¹ęøńĪŖ25mL£¬µĪ¶ØĒ°µĪ¶Ø¹ÜÖŠŅŗĆęµÄ¶ĮŹżĪŖ5.20 mL£¬ŌņµĪ¶Ø¹ÜÖŠŅŗĢåµÄĢå»żĪŖ______£ØĢī“śŗÅ£©”£
A£®5.20 mL B£®19.80 mL C£®“óÓŚ19.80 mL D£®Š”ÓŚ19.80 mL
£Ø3£©±¾ŹµŃéŹĒ·ńŠčŅŖĶā¼ÓÖøŹ¾¼Į£æ £ØĢī”°ŹĒ”±»ņÕß”°·ń”±£©”£ČēŗĪÅŠ¶ĻµĪ¶ØÖÕµć
£Ø4£©µĪ¶ØŹ±±ßµĪ±ßŅ”¶Æ׶ŠĪĘ棬ŃŪ¾¦Ó¦¹Ū²ģ
£Ø5£©øĆÅ£ÄĢÖŠøʵÄŗ¬ĮæĪŖ_________mg/100mL”£
£Ø6£©ĻĀĮŠ²Ł×÷»įŹ¹ŹµŃé½į¹ūĘ«µĶµÄŹĒ____________£ØĢī“śŗÅ£©”£
A£®µĪ¶Ø¹ÜĪ“ÓĆKMnO4ČÜŅŗČóĻ“¾ĶÖ±½ÓŹ¢×°KMnO4ČÜŅŗ
B£®Ļņ׶ŠĪĘæ×ŖŅĘ³ĮµķŹ±£¬ĖšŹ§²æ·Ö³Įµķ
C£®æŖŹ¼Ź±Ę½ŹÓ¶ĮŹż£¬µĪ¶ØĶź³ÉŹ±ø©ŹÓ¶ĮŹż
D£®CaC2O4µÄ±ķĆęƻӊĻ“µÓøɾ»£¬Īüø½ÉŁĮæC2O42£µČŌÓÖŹ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com