
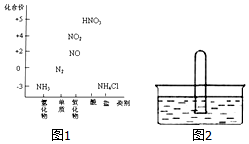
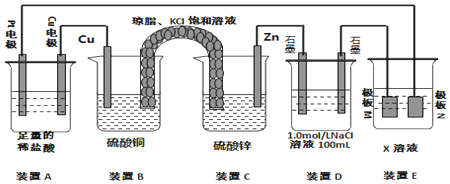
 Ķ¼1ĪŖµŖ¼°Ęä»ÆŗĻĪļµÄĄą±šÓė»ÆŗĻ¼Ū¶ŌÓ¦µÄ¹ŲĻµĶ¼£®
Ķ¼1ĪŖµŖ¼°Ęä»ÆŗĻĪļµÄĄą±šÓė»ÆŗĻ¼Ū¶ŌÓ¦µÄ¹ŲĻµĶ¼£®·ÖĪö £Ø1£©¢ŁŹµŃéŹŅÓĆ¹ĢĢåĀČ»Æļ§ŗĶ¹ĢĢåĒāŃõ»ÆøĘ·“Ó¦Öʱø°±Ęų£»
¢ŚŅĄ¾Ż°±Ęų¼«Ņ×ČÜÓŚĖ®µÄŠŌÖŹ½ā“š£»
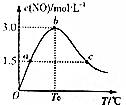
£Ø2£©b£®»ÆŗĻ¼ŪÉżøßµÄŌŖĖŲĢåĻÖ»¹ŌŠŌ£¬°±Ęų“ß»ÆŃõ»ÆÉś³ÉŅ»Ńõ»ÆµŖŗĶĖ®£¬·“Ó¦ÖŠĢåĻÖ°±ĘųµÄ»¹ŌŠŌ£»
£Ø3£©¢Ł¶žŃõ»ÆµŖŗĶĖ®·“Ӧɜ³ÉĻõĖįŗĶŅ»Ńõ»ÆµŖ£»
¢ŚĒó³öV mLNO2µÄĪļÖŹµÄĮ棬ÉčĻūŗĵÄŃõĘųµÄĪļÖŹµÄĮæĪŖxmol£¬Éś³ÉµÄĻõĖįµÄĪļÖŹµÄĮæĪŖymol£¬Č»ŗóøł¾Ż»Æѧ·½³ĢŹ½4NO2+O2+2H2O=4HNO3¼ĘĖć£»
¢ŪNO2ŗĶ°±Ęų·¢Éś¹éÖŠ·“Ӧɜ³ÉµŖĘų£®
£Ø4£©Fe2O3ŹĒ¼īŠŌŃõ»ÆĪļ£¬ÄÜŗĶĖį·“Ó¦£»¶ųSiO2ŹĒĖįŠŌŃõ»ÆĪļ£¬ÄÜŗĶ¼ī·“Ó¦£»
ĀČĘųŗĶĒāŃõ»ÆøĘ·“Ó¦ÖĘČ”ĘÆ°×·Ū£®
½ā“š ½ā£ŗ£Ø1£©¢Łļ§ŃĪŗĶ¼ī·“Ӧɜ³É°±Ęų£¬ŹµŃéŹŅÓĆ¹ĢĢåĀČ»Æļ§ŗĶ¹ĢĢåĒāŃõ»ÆøĘ·“Ó¦Öʱø°±Ęų£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ£ŗCa£ØOH£©2+2NH4Cl=CaCl2+2NH3”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗ2NH4Cl+Ca£ØOH£©2$\frac{\underline{\;\;”÷\;\;}}{\;}$CaCl2+2NH3”ü+2H2O£»
¢Ś°±ĘųŅ×ČÜÓŚĖ®£¬Ź¹×°ÖĆÖŠµÄŃ¹ĒæŠ”ÓŚĶā½ēµÄŃ¹Ē棬“Ó¶ųŅżĘšµ¹Īü£¬
¹Ź“š°øĪŖ£ŗ°±Ė®¼«Ņ×ČÜÓŚĖ®£»
£Ø2£©b£®°±Ęų“ß»ÆŃõ»ÆÉś³ÉŅ»Ńõ»ÆµŖŗĶĖ®£¬»Æѧ·½³ĢŹ½£ŗ4NH3+5O2$\frac{\underline{\;“߻ƼĮ\;}}{”÷}$4NO+6H2O£¬°±ĘųÖŠ-3¼ŪNÉżøßĪŖ+2¼Ū£¬ĢåĻÖ»¹ŌŠŌ£¬
¹Ź“š°øĪŖ£ŗ4NH3+5O2$\frac{\underline{\;“߻ƼĮ\;}}{”÷}$4NO+6H2O£»
£Ø3£©¢Ł¶žŃõ»ÆµŖæÉŅŌŗĶĖ®Ö®¼ä·“Ó¦£¬·“Ó¦ĪļNO2ÖŠNŌŖĖŲ»ÆŗĻ¼Ū½µµĶĪŖ+2¼Ū£¬ÉżøßĪŖ+5¼Ū£¬Éś³ÉĻõĖįŗĶŅ»Ńõ»ÆµŖ£¬·“Ó¦ĪŖ£ŗ3NO2+H2O=2HNO3+NO£¬
¹Ź“š°øĪŖ£ŗ3NO2+H2O=2NHO3+NO£»
¢Ś±źæöĻĀV mLNO2µÄĪļÖŹµÄĮæn=$\frac{V”Į1{0}^{-3}L}{22.4L/mol}$=$\frac{V}{22400}mol$£¬ÉčĻūŗĵÄŃõĘųµÄĪļÖŹµÄĮæĪŖxmol£¬Éś³ÉµÄĻõĖįµÄĪļÖŹµÄĮæĪŖymol£¬øł¾Ż»Æѧ·½³ĢŹ½4NO2+O2+2H2O=4HNO3æÉÖŖ£ŗ4NO2 +O2 +2H2O=4HNO3
4 1 4
$\frac{V}{22400}mol$ xmol ymol
ŌņÓŠ£ŗ$\frac{4}{\frac{V}{22400}mol}=\frac{1}{xmol}=\frac{4}{ymol}$
½āµĆx=$\frac{V}{22400}”Į\frac{1}{4}$mol
y=$\frac{V}{22400}$mol
¹ŹĖłĻūŗĵÄŃõĘųµÄĢå»żV£ØO2£©=$\frac{V}{22400}”Į\frac{1}{4}$mol”Į22.4L/mol=$\frac{V}{4000}$L=$\frac{V}{4}$mL£»
ÓÉÓŚ×īÖÕČÜŅŗ³äĀśÕūøöŹŌ¹Ü£¬¹ŹĖłµĆĻõĖįČÜŅŗµÄĢå»żĪŖVmL£¬ŌņĻõĖįČÜŅŗµÄÅضČC=$\frac{\frac{V}{22400}mol}{V”Į1{0}^{-3}L}$=$\frac{1}{22.4}$mol/L£®
¹Ź“š°øĪŖ£ŗ$\frac{V}{4}$mL£»$\frac{1}{22.4}$mol/L£»
¢ŪNO2ŗĶ°±Ęų·¢Éś¹éÖŠ·“Ӧɜ³ÉµŖĘųŗĶĖ®£¬¹Ź»Æѧ·½³ĢŹ½ĪŖ£ŗ6NO2+8NH3=7N2+12H2O£¬¹Ź“š°øĪŖ£ŗ6NO2+8NH3=7N2+12H2O£»
£Ø4£©Fe2O3ŹĒ¼īŠŌŃõ»ÆĪļ£¬ÄÜŗĶĖį·“Ó¦£»¶ųSiO2ŹĒĖįŠŌŃõ»ÆĪļ£¬ÄÜŗĶ¼ī·“Ó¦£¬¹ŹÄÜÓĆ¼īČÜŅŗ³żČ„Fe2O3ÖŠµÄSiO2£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗSiO2+2OH-=SiO32-+H2O£»
ĀČĘųŗĶĒāŃõ»ÆøĘ·“Ó¦ÖĘČ”ĘÆ°×·Ū£¬»Æѧ·½³ĢŹ½ĪŖ£ŗ2Cl2+2Ca£ØOH£©2=CaCl2+Ca£ØClO£©2+2H2O£®
¹Ź“š°øĪŖ£ŗSiO2+2OH-=SiO32-+H2O£»2Cl2+2Ca£ØOH£©2=CaCl2+Ca£ØClO£©2+2H2O£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·½³ĢŹ½µÄ¼ĘĖć£¬×¢Ņā°ŃĪÕ°±ĘųµÄŠŌÖŹŗĶÖĘ·Ø£¬½ā“š±¾ĢāµÄ¹Ų¼üŹĒ°ŃĪÕŃõ»Æ»¹Ō·“Ó¦µÄĢŲµćŗĶ»Æѧ·½³ĢŹ½µÄÓŠ¹Ų¼ĘĖć£¬£Ø3£©ĪŖŅדķµć£¬“šĢāŹ±×¢ŅāŹĒ¶žŃõ»ÆµŖŹĒVmL£¬¶ų²»ŹĒ¶žŃõ»ÆµŖŗĶŃõĘųµÄ»ģŗĻĘųĢ壮


 ĆĻ½ØĘ½ĆūŠ£æ¼¾ķĻµĮŠ“š°ø
ĆĻ½ØĘ½ĆūŠ£æ¼¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŗĻ³É°±¹¤ŅµŹĒĪŅŹ”æŖĮ×¼ÆĶŵÄÖŲŅŖÖ§Öł²śŅµÖ®Ņ»£®°±ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ŌŚ¹¤Å©ŅµÉś²śÖŠÓŠ¹ć·ŗµÄÓ¦ÓĆ£®
ŗĻ³É°±¹¤ŅµŹĒĪŅŹ”æŖĮ×¼ÆĶŵÄÖŲŅŖÖ§Öł²śŅµÖ®Ņ»£®°±ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ŌŚ¹¤Å©ŅµÉś²śÖŠÓŠ¹ć·ŗµÄÓ¦ÓĆ£®| »Æѧ¼ü | N-H | N”ŌN | Br-Br | H-Br |
| ¼üÄÜ/kJ•mol-1 | 391 | 946 | 194 | 366 |
| Ź±¼ä/min | CH4£Ømol£© | H2O£Ømol£© | CO £Ømol£© | H2 £Ømol£© |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | a | 0.80 | c | 0.60 |
| 7 | 0.20 | b | 0.20 | d |
| 10 | 0.21 | 0.81 | 0.19 | 0.64 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µŖĘųµÄ½į¹¹Ź½£ŗN=N | B£® | F-µÄ½į¹¹Ź¾ŅāĶ¼£ŗ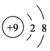 | ||
| C£® | ÖŠ×ÓŹżĪŖ20 µÄĀČŌ×Ó£ŗ2017Cl | D£® | NH3 µÄµē×ÓŹ½£ŗ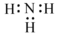 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| »Æѧ¼ü | N”ŌN | H-O | N-H | O=O |
| E/£ØkJ/mol£© | 946 | 463 | 391 | 496 |
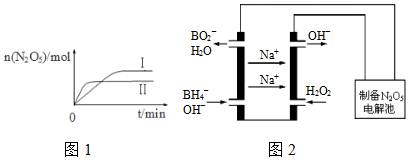
| .01mol/L µÄČÜŅŗ | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĘĻĢŃĢĒ | B£® | ĒāŃõ»ÆÄĘ | C£® | ĀČ»Æ¼Ų | D£® | Ģś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1L0.1mol•L-1NaClOČÜŅŗÖŠ£¬ClO-µÄŹżÄæĪŖ0.1NA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬11.2LCH4ŗ¬ÓŠµÄ¹²ÓƵē×Ó¶ŌŹżÄæĪŖ2NA | |
| C£® | 16gO2ÓėO3»ģŗĻĘųĢåÖŠ£¬ŃõŌ×ӵďżÄæĪŖ1.5NA | |
| D£® | 1molFeÓė×ćĮæCl2ĶźČ«·“Ó¦ŗó£¬×ŖŅʵĵē×ÓŹżÄæĪŖ3NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °Ń¹żĮæŠĀÖʵÄĀČĖ®µĪ¼Óµ½ŹÆČļŹŌŅŗÖŠ£¬ČÜŅŗŃÕÉ«Ļȱ䥶ŗóĶŹÉ« | |
| B£® | ×ŌĄ“Ė®³§ÓĆĀČĘųøųĖ®Ļū¶¾£¬ŹĒŅņĪŖĀČĘųÓėĖ®·“Ӧɜ³ÉµÄHClO¾ßÓŠĒæŃõ»ÆŠŌ | |
| C£® | Cl2”¢Cl-¾łÓŠ¶¾ | |
| D£® | Cl2”¢HClO”¢H2O2¶¼¾ßÓŠĘư׊Ō |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com