
 石灰石(主要成分为CaCO3)是重要的工业原料,
石灰石(主要成分为CaCO3)是重要的工业原料,| 物理量/单位 实验序号 | m(CaCO3)/g | V(2mon?L-1HCl)/mL | V(H2O)/mL | |
| 1 | P | 20 | 0 | |
| 2 | P |
 ;
; ;
;| 物理量/单位 实验序号 | 固体全部溶解的时间/min | |||
| 1 | 20 | 0 | t1 | |
| 2 | 20 | a | t2 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

| NaOH/H2O |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 烧杯中通入过量的CO2,出现白色沉淀,则溶液中一定含有AlO2- 烧杯中通入过量的CO2,出现白色沉淀,则溶液中一定含有AlO2- |
B、 装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、氧化性 装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、氧化性 |
C、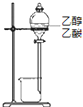 装置可以除去乙醇中的乙酸 装置可以除去乙醇中的乙酸 |
D、 装置可以比较碳酸钠、碳酸氢钠的热稳定性 装置可以比较碳酸钠、碳酸氢钠的热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 高铁酸盐在能源环保领域有广泛用途.用镍(Ni),铁做电极电解浓氢氧化钠溶液制备Na2FeO4的装置如图,说法合理的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni),铁做电极电解浓氢氧化钠溶液制备Na2FeO4的装置如图,说法合理的是( )| A、镍是阳极,电极反应4OH--4e-=2H2O+O2↑ |
| B、电解时电流方向:负极→镍电极→溶液→铁电极→正极 |
| C、若隔膜是阴离子交换膜,则OH-自右向左移动 |
| D、电解时阳极区pH降低,阴极区pH升高,撤去隔膜后与原溶液比较pH降低(假设电解前后体积变化忽略不计) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定有乙烷 |
| B、一定有甲烷 |
| C、一定没有甲烷 |
| D、不一定有甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 国庆期间对大量鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,说法正确的是( )
国庆期间对大量鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,说法正确的是( )| A、分子式C15H21O4 |
| B、既能发生加聚反应,又能发生缩聚反应 |
| C、分子中有两个手性碳原子 |
| D、既能使氯化铁溶液发生显色反应,又能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知:NH2COO-+2H2O?HCO3-+NH3?H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )
已知:NH2COO-+2H2O?HCO3-+NH3?H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )| A、无法判断T1和T2的大小关系 |
| B、T1℃时,第6min反应物转化率为6.25% |
| C、T2℃时,0~6min ν(NH2COO-)=0.3mol?L-1?min-1 |
| D、往平衡体系加水稀释,平衡右移,溶液中各种离子浓度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验内容 | 实验目的 |
| A | 向FeCl2溶液中加入几滴KSCN溶液,观察溶液颜色 | 检验FeCl2溶液是否已变质 |
| B | 将Cl2通入NaBr溶液中 | 比较氯气与溴的氧化性强弱 |
| C | 用冰水冷却铜与浓硝酸反应生成的气体 | 研究温度对化学平衡的影响 |
| D | 直接将CuCl2溶液加热蒸干 | 制取无水CuCl2固体 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com