
����Ŀ��һ�������£�������̼�ɺϳɵ�̼ϩ������������ЧӦ���������̼��Դ��
��1����֪����C2H4(g)+2O2(g)=2CO2(g)+2H2(g) ��H1
��2H2(g)+O2(g)=2H2O(1) ��H2
��H2O(1)=H2O(g) ��H3
��2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ��H4
C2H4(g)+4H2O(g) ��H4
����H4=___(����H1����H2����H3��ʾ)��
��2����Ӧ�ܵķ�Ӧ�¶ȡ�Ͷ�ϱ�[![]() =x]��CO2ƽ��ת���ʵ�Ӱ����ͼ��ʾ��
=x]��CO2ƽ��ת���ʵ�Ӱ����ͼ��ʾ��
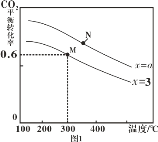
��a__3������>������<������=������M��N���㷴Ӧ��ƽ�ⳣ��KM__KN��������>������<������=����
��M����ϩ�������Ϊ__��������2λ��Ч���֣�
��300�棬��6L��Ӧ�����м���3molH2��1molCO2����Ӧ10min�ﵽƽ�⡣��0��10min������ƽ����Ӧ����Ϊ__��
��3���п�Ժ���ݻ�ѧ�����о�����Fe3(CO)12/ZSM-5��CO2����ϳɵ�̼ϩ����Ӧ�����ò��ﺬCH4��C3H6��C4H8�ȸ������Ӧ������ͼ��
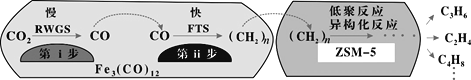
����������Na��K��Cu����������Ҳ������ã��ɸı䷴Ӧ��ѡ���ԣ�������������ͬʱ�����Ӳ�ͬ������������ͬʱ�����CO2ת���ʺ���������ʵ����������±���
���� | CO2ת���� ��%�� | �����������в����е�ռ�ȣ�%�� | ||
C2H4 | C3H6 | ���� | ||
Na | 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
Cu | 9.8 | 80.7 | 12.5 | 6.8 |
������ߵ�λʱ������ϩ�IJ�������Fe3(CO)12/ZSM-5������__����Ч����ã�������������ߵ�λʱ������ϩ�����ĸ���ԭ����__��
������˵����ȷ����__��
a���ڢ�������ӦΪ��CO2+H2![]() CO+H2O
CO+H2O
b���ڢ�����Ӧ�Ļ�ܵ��ڵڢ���
c������������Ҫ�ڵ;۷�Ӧ���칹����Ӧ����������
d��Fe3(CO)12/ZSM-5ʹCO2����ϳɵ�̼ϩ������H��С
e�����Ӳ�ͬ������Ӧ��ƽ�ⳣ��������ͬ
��4��2018�꣬ǿ���Ե����ԭCO2����ϩ�о�ȡ��ͻ�ƽ�չ��ԭ����ͼ��ʾ��
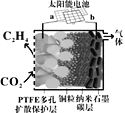
��b���ӵ���̫���ܵ�ص�__����
����֪PTFE�����˱���KCl��Һ����д�������ĵ缫��Ӧʽ__��
���𰸡�2��H2+4��H3-��H1 > > 9.7%��![]() 0.03mol��L-1��min-1 K ����������ϩ�ķ�Ӧ����Ҫ�Ļ�ܣ��ӿ���ϩ�������ʣ�������������Ӧ������Ӱ�� ac �� 2CO2+12e-+8H2O=C2H4+12OH-
0.03mol��L-1��min-1 K ����������ϩ�ķ�Ӧ����Ҫ�Ļ�ܣ��ӿ���ϩ�������ʣ�������������Ӧ������Ӱ�� ac �� 2CO2+12e-+8H2O=C2H4+12OH-
��������
��1�����ø�˹���ɼ��㣻
��2����ͼ�Ͽ���Ͷ�ϱ���ͬʱ���¶����ߣ�������̼ת���ʼ�С��˵���¶����ߣ�ƽ�������ƶ����淴Ӧ�����ȷ�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����H<0��Ͷ�ϱȴ�3��a��������̼��ת��������˵��3��aͶ�ϱ�������ƽ�ⳣ��ֻ���¶��йأ�ƽ�����еļ���������ʽ���
��3���ӱ���������ʹ��Na������ת������ߣ�����ϩ������ͣ�ʹ��Cu��������ϡ������ߣ���������̼ת������ͣ�ʹ��K������������̼ת���ʸ�����ϩ����Ҳ�ߣ���λʱ���ڲ�����ϩ��ࣻ��������ʹ��Ӧ����ѡ���Ե�ԭ��������������ij����Ӧ����Ļ�ܣ���ͬ�����¸�������ij����Ӧ���£�
��4��PTFE�缫CO2���C2H4��̼Ԫ�ػ��ϼ۴�+4���͵�-2��Ϊ������
�����Ϸ�������
��1�����ݸ�˹���ɣ�����ʽ�����¹�ϵ��2����-��+4����=�ܣ����ԡ�H 4=2��H2+4��H3-��H1���ʴ�Ϊ��2��H2+4��H3-��H1��
��2������ͬ�¶��£�Ͷ�ϱȴ�3��a��������̼ת��������˵��Ͷ�ϱ�����������a>3��Ͷ�ϱ���ͬʱ�������¶ȣ�������̼ת���ʼ�С��˵�������¶ȣ�ƽ�������ƶ�����K��С����N���¶ȸ���M�㣬����KM>KN���ʴ�Ϊ��>��>��
����ͼ��֪,M��Ͷ�ϱ�Ϊ3��������̼ת����Ϊ0.6���迪ʼͶ��1mol������̼��3mol�������������̼ת����Ϊ0.6��������ʽ�ⷨ���£�
����M����ϩ���������=![]() ��100%=9.7%���ʴ�Ϊ��9.7%��
��100%=9.7%���ʴ�Ϊ��9.7%��
��ͬ��������ʽ�������£�

��֪����������10min������1.8mol������Ũ�ȼ�Сֵ=![]() =0.3mol��L-1������v(H2)=
=0.3mol��L-1������v(H2)=![]() =0.03mol����L��min��-1���ʴ�Ϊ��0.03mol��L-1��min-1��
=0.03mol����L��min��-1���ʴ�Ϊ��0.03mol��L-1��min-1��
��3����ʹ��Na������ת������ߣ�����ϩ������ͣ�ʹ��Cu��������ϡ������ߣ���������̼ת������ͣ�ʹ��K������������̼ת���ʸ�����ϩ����Ҳ��,��λʱ���ڲ�����ϩ��ࣻ��������ʹ������ϩ����ѡ���Ե�ԭ��������������������ϩ��Ӧ����Ļ�ܣ���ͬ�����¸�����������ϩ������������Ӧ������Ӱ�죻�ʴ�Ϊ��K������������ϩ�ķ�Ӧ����Ҫ�Ļ�ܣ��ӿ���ϩ�������ʣ�������������Ӧ������Ӱ�죻
��a����������֪�ڢ�����Ӧ��Ϊ������̼����������������CO������������ԭ��Ӧ�ɵ÷���ʽΪCO2+H2![]() CO+H2O��a��ȷ��
CO+H2O��a��ȷ��
b���ڢ�����Ӧ�������ڵڢ�����Ӧ���ʵڢ�����Ӧ�����������ڢ�����Ӧ�Ļ�ܸ��ͣ�b����
c����ͼ�Ͽ�����CH4��C3H6��C4H8�ȸ�������Ҫ�ڵ;۷�Ӧ���칹����Ӧ���ڣ�����������Ҫ�ڵ;۷�Ӧ���칹����Ӧ���������ã�c��ȷ��
d����H�뷴Ӧ;���أ�ֻ����ʼ�йأ�d����
e����Ӧ��ƽ�ⳣ��ֻ���¶��йأ��¶Ȳ��䣬K���䣬e����
�ʴ�Ϊ��ac��
��4����PTFE(a��)�缫CO2���C2H4��̼Ԫ�ػ��ϼ۴�+4���͵�-2��Ϊ��������b��Ϊ��������̫���ܵ�������������ʴ�Ϊ������
�������ĵ缫��ӦʽΪ2CO2+12e-+8H2O=C2H4+12OH-���ʴ�Ϊ��2CO2+12e-+8H2O=C2H4+12OH-��


 ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ŵ�������Ի���������Ӱ����������أ��������������Ⱦ���еĵ��������Ϊ���ǹ�ע����Ҫ����֮һ��
��.����NH3�Ļ�ԭ�Կ������������������Ⱦ�����г�ȥNO����Ҫ��Ӧ���£�4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) ��H��0
5N2(g)+6H2O(l) ��H��0
(1)д��һ�ֿ������NO��ת���ʵķ�����__________
(2)һ���¶��£��ں����ܱ������а���n(NH3)�Un(NO) =2�U3���뷴Ӧ�����������Ӧ�����������жϸ÷�Ӧ�ﵽƽ��״̬����___________
A.c(NH3)�Uc(NO) =2�U3 B.n(NH3)�Un(N2) ���� C.������ѹǿ���� D.�����ڻ��������ܶȲ��� E.1molN��H�����ѵ�ͬʱ������1molO��H��
(3)��֪�÷�Ӧ����v��=k����c4(NH3)��c6 (NO)��v��=k����cx(N2)��cy(H2O) (k����k���ֱ��������淴Ӧ���ʳ���)���÷�Ӧ��ƽ�ⳣ��K=k��/k��,��x=_____��y=_______��
(4)ij�о�С�齫2molNH3��3molNO��һ������O2����2L�ܱ������У���Ag2O�������淢��������Ӧ��NO��ת�������¶ȱ仯�������ͼ��ʾ��

����5min�ڣ��¶ȴ�420K���ߵ�580K����ʱ����NO��ƽ����Ӧ����v(NO)=_______;
�������������£��¶�580K֮��NO����N2��ת���ʽ��͵�ԭ�������___________��
��.������[(NH2)2CO]ˮ��Һ���յ�������Ҳ��һ�ֿ��еķ�����NO��NO2��ͬ��Ȼ����ͨ��������Һ�У��ܵ���ԭ������ȹ�ϵ��ͼ��

(5)������[(NH2)2CO]ˮ��Һ���������Ϊ1��1��NO��NO2��������ɽ�NԪ��ת��Ϊ�Ի����������塣д���÷�Ӧ�Ļ�ѧ����ʽ____��
(6)����NO��NO2��ȵ���ߣ��ܵ���ԭ�ʽ��͵���Ҫԭ����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��ŵ������ѧ����������ӵ�صķ����ߣ�LiFePO4������ӵ�ص��������ϡ��ú�﮷�������Ҫ����Ԫ�صĺ�����Li 8.50%��Ni 6.55%��Mg 13.24%���Ʊ�Li2C2O4���������Ʊ�LiFePO4���ֹ���������ͼ�������̿������ˮ������Ⱦ����
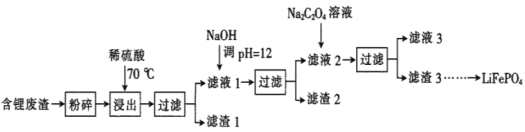
��֪����Һ1����Һ2�в������ӵ�Ũ�ȣ�g��L-1����
Li+ | Ni2+ | Mg2+ | |
��Һ1 | 22.72 | 20.68 | 60.18 |
��Һ2 | 21.94 | 7.7��10-3 | 0.78��10-3 |
I.�Ʊ�Li2C2O4
(1)����2����Ҫ�ɷ���__���ѧʽ����
(2)Na2C2O4��Һ�и����ӵ�Ũ���ɴ�С˳��Ϊ__��
(3)д������Na2C2O4��Һʱ������Ӧ�����ӷ���ʽ��__��
��.�Ʊ�LiFePO4
(4)����ؼ�Li2C2O4��FePO4���ڸ����·�Ӧ����LiFePO4��һ���������壬�÷�Ӧ�Ļ�ѧ����ʽ��___��
(5)LiFePO4��Ҫ�ڸ����³��ͺ������Ϊ�缫�����³���ʱҪ��������ʯī����ʯī��������__����дһ�㣩��
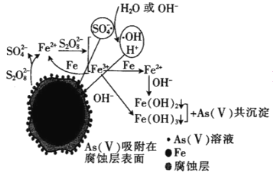
(6)�ҹ���ѧ���о��������������ƣ�Na2S2O8��ȥ����ˮ�е�As(��)�������ģ����ͼ�������������������Ʒ�Ӧ�����ӷ���ʽ��__���ڸ�ģ���еõ������鹲�����ᆳ���գ���Ԫ�ػ��ϼ۱仯����õ�һ�ִ��Ի������ѧʽΪFe7As2O14���������ж��������������ĸ�����Ϊ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ҿ������õĽ��ȡ���ʹ�����ס�����ʪ���ã���������ҵĺϳ�·�����£�
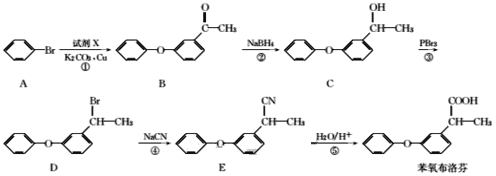
�ش��������⣺
(1)����������й����ŵ�����Ϊ___��
(2)̼ԭ��������4����ͬ��ԭ�ӻ����ʱ����̼��Ϊ����̼��A-D���������У���������̼���л���Ϊ___������ĸ����
(3)��Ӧ�ڵķ�Ӧ������___��
(4)�����̢ٷ�������ȡ����Ӧ������һ�ֲ���ΪHBr����A����B������Ӧ�Ļ�ѧ����ʽΪ___��
(5)�л���M��C��Ϊͬ���칹�壬M��������������
I.����FeCl3��Һ������ɫ��Ӧ��1molM������2molNaOH��
��.M��������6�ֲ�ͬ��ѧ�������⣬�˴Ź�������Ϊ3��2��2��2��2��3���ҷ����к���![]() �ṹ��
�ṹ��
M�Ľṹ��___�֣�д������һ�ֽṹ��ʽ��___��
(6)��������֪ʶ����������Ϣ��д���Ա�ͪ(CH3COCH3)Ϊԭ���Ʊ�2һ������ĺϳ�·������ͼ�����Լ����ã�___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������LiFePO4��ض�Ӧ���ڹ�����ͨ���ṹ��ͼ��ʾ������м��Ǿۺ���ĸ�Ĥ������Ҫ�������ڷ�Ӧ������ֻ��Li+ͨ����ԭ�����£�(1x)LiFePO4+xFePO4+LixCn![]() LiFePO4+nC������˵���������ǣ� ��
LiFePO4+nC������˵���������ǣ� ��

A.�ŵ�ʱ��Li+�������ƶ�
B.�ŵ�ʱ�������ɸ������õ���������
C.���ʱ��������ӦΪxLi++nC+xe-=LixCn
D.���ʱ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У���ȷ���ǣ� ��
A.Na��Mg��Al��δ�ɶԵ�������������
B.�۵����Ų�Ϊ4s24p3��Ԫ��λ�ڵ������ڵڢ�A�壬��p��Ԫ��
C.2p��3p�����״��Ϊ�����Σ�����Ҳ���
D.��ԭ�ӵ����������Ų�ͼ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ƺ�ͭ�ĵ��ʼ��仯���������ʵ�������Ź㷺��Ӧ�á�
��1��NaCl����ľ����ṹ��ͼ��ʾ��ÿ��NaCl�ľ����к��е������ӵĸ���Ϊ__����������Χ����ҵȾ���������ӵĸ���Ϊ__��
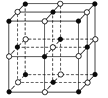
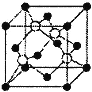
��2���⻯����Һ������ͭ��Һ�ܷ�Ӧ����һ��ͭ�ĵ⻯��A����ɫ��������A�ľ�������ͼ��ʾ����A�Ļ�ѧʽ��__��A��ͭԪ�صĻ��ϼ�Ϊ__��
��3��������ͭ��Һ�еμӰ�ˮ��������ɫ�������ٵμӰ�ˮ�������պ�ȫ���ܽ�ɵõ�����ɫ��Һ�����������м��뼫�Խ�С���Ҵ�������������ɫ��[Cu(NH3)4]SO4��H2O�������������е�NH3ͨ��___������������Cu2����ϣ�NH3������Nԭ�ӵ��ӻ���ʽ��__����NH3���ӻ�Ϊ�ȵ������һ����������__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�����A��B�����2L���ܱ������У��������·�Ӧ��3A(g)+B(g)xC(g)+2D(g)����5min���ƽ��״̬����ʱ���D��Ũ��Ϊ0.5mol/L���������������Ϊ134.4L(��״��)��C��ƽ����Ӧ����Ϊ0.1mol/(L��min)������
(1)��ʱC��Ũ��c(C)=__________mol/L��x��ֵΪ___________��
(2)��Ӧ��ʼǰ�����е�A.B�����ʵ�����n(A)=n(B)=________mol��
(3)A��ƽ����Ӧ����Ϊ___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������Ԫ��M��N��P��Q����������Ӧˮ����ֱ�ΪX��Y��Z��W��M�Ƕ�������ԭ�Ӱ뾶����Ԫ�أ�������X��Z��W������Y��Ӧ��M��P��Q��ԭ��������0.1mol/LX��Z��W��Һ��pH��ͼ��ʾ������˵����ȷ���ǣ� ��
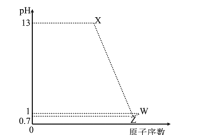
A.Nԭ�ӵĵ��Ӳ������������������
B.M�����Ӱ뾶С��N�����Ӱ뾶
C.P�⻯���ȶ��Դ���Q�⻯���ȶ���
D.X��W�����ʺ��еĻ�ѧ��������ͬ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com