
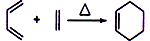
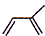
 ,化学名称是2-甲基-1,3-丁二烯;
,化学名称是2-甲基-1,3-丁二烯;
 :
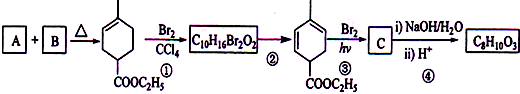
: 分析 化合物A是合成天然橡胶的单体,分子式为C5H8,A是异戊二烯,A和B反应生成 ,根据异戊二烯和
,根据异戊二烯和 的结构简式知,A和B发生了加成反应,B的结构简式为:CH2=CHCOOCH2CH3,
的结构简式知,A和B发生了加成反应,B的结构简式为:CH2=CHCOOCH2CH3, 和溴发生加成反应生成
和溴发生加成反应生成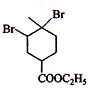 ,
, 和氢氧化钠的醇溶液发生消去反应生成
和氢氧化钠的醇溶液发生消去反应生成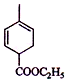 ,
, 和溴反应生成C,C为单溴代物,分子中有两个亚甲基,C和氢氧化钠的水溶液反应,再和酸反应生成C8H10O3,所以C的结构简式为:
和溴反应生成C,C为单溴代物,分子中有两个亚甲基,C和氢氧化钠的水溶液反应,再和酸反应生成C8H10O3,所以C的结构简式为: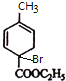 ,分子式为C8H10O3结构简式
,分子式为C8H10O3结构简式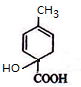 ,据此答题.
,据此答题.
解答 解:化合物A是合成天然橡胶的单体,分子式为C5H8,A是异戊二烯,A和B反应生成 ,根据异戊二烯和
,根据异戊二烯和 的结构简式知,A和B发生了加成反应,B的结构简式为:CH2=CHCOOCH2CH3,
的结构简式知,A和B发生了加成反应,B的结构简式为:CH2=CHCOOCH2CH3, 和溴发生加成反应生成
和溴发生加成反应生成 ,
, 和氢氧化钠的醇溶液发生消去反应生成
和氢氧化钠的醇溶液发生消去反应生成 ,
, 和溴反应生成C,C为单溴代物,分子中有两个亚甲基,C和氢氧化钠的水溶液反应,再和酸反应生成C8H10O3,所以C的结构简式为:
和溴反应生成C,C为单溴代物,分子中有两个亚甲基,C和氢氧化钠的水溶液反应,再和酸反应生成C8H10O3,所以C的结构简式为: ,分子式为C8H10O3结构简式
,分子式为C8H10O3结构简式 .
.
(1)通过以上分析知,A是异戊二烯,结构简式为 ,化学名称是2-甲基-1,3-丁二烯,
,化学名称是2-甲基-1,3-丁二烯,
故答案为: ;2-甲基-1,3-丁二烯;
;2-甲基-1,3-丁二烯;
(2)B的结构简式为:CH2=CHCOOCH2CH3,则其分子式为C5H8O2,故答案为:C5H8O2;
(3) 和氢氧化钠的醇溶液发生消去反应生成
和氢氧化钠的醇溶液发生消去反应生成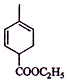 ,反应方程式为
,反应方程式为 ,
,
故答案为: ;
;
(4)通过以上分析知,①和③的反应类型分别是加成反应和取代反应,故答案为:加成反应;取代反应;
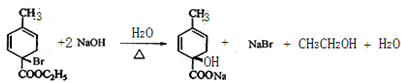
(5)C为单溴代物,分子中有两个亚甲基,C和氢氧化钠的水溶液反应,④的化学方程式为 ,
,
故答案为: .
.
点评 本题考查有机物的推断,需要结合信息,利用烯烃、溴代烃等有机物的性质来分析解答,注意书写同分异构体时应按照顺序书写,如按照碳链异构、官能团位置异构、类别异构(如同碳数的二烯烃与炔烃,醇与醚,羧酸与酯、羟基醛等属于类别异构)和顺反异构等,难度中等.


科目:高中化学 来源: 题型:解答题
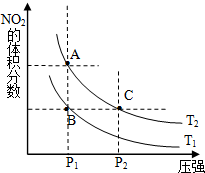 (1)对反应N2O4(g)═2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.T1<T2(填“>”、“<”或“=”);A、C两点的速率VA<VC(同上).
(1)对反应N2O4(g)═2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.T1<T2(填“>”、“<”或“=”);A、C两点的速率VA<VC(同上).| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
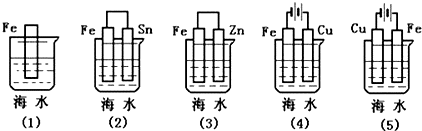
| A. | (5)(2)(1)(3)(4) | B. | (5)(2)(3)(1)(4) | C. | (4)(2)(1)(3)(5) | D. | (4)(2)(1)(5)(3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现有aA、bB、cC、dD、eE五种短周期元素,它们都是生命不可缺少的重要元素.已知它们的原子序数有如下关系:a+b=c,a+c=d,c+d=e;B、D、E都有多种同素异形体,B的化合物种类与A的化合物种类何者最多尚有争议.据此,回答下列有关问题:
现有aA、bB、cC、dD、eE五种短周期元素,它们都是生命不可缺少的重要元素.已知它们的原子序数有如下关系:a+b=c,a+c=d,c+d=e;B、D、E都有多种同素异形体,B的化合物种类与A的化合物种类何者最多尚有争议.据此,回答下列有关问题: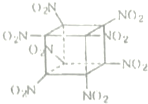 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n(Cl2):n(Fe)=5:4 5Cl2+4Fe $\frac{\underline{\;点燃\;}}{\;}$2FeCl2+2FeCl3 | |
| B. | n(Cl2):n(FeBr2)=1:1 Fe2++2Br-+Cl2═Fe3++Br2+2Cl- | |
| C. | n(MnO4-):n(H2O2)=2:3 2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | |
| D. | n(Fe):n[HNO3(稀)]=1:3 4Fe+12H++3NO3-═3Fe2++Fe3++3NO↑+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 两同学为制得纯净的Fe(OH)2,根据如图所示的装置,回答问题.A管中是Fe+H2SO4,B管中是NaOH溶液
两同学为制得纯净的Fe(OH)2,根据如图所示的装置,回答问题.A管中是Fe+H2SO4,B管中是NaOH溶液查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲同学为测定0.01mol•L-1盐酸的pH值:用湿的玻璃棒蘸取盐酸,点在pH试纸上 | |
| B. | 乙同学要检验(NH4)2Fe(SO4)2•12H2O晶体中的NH4+:取少量晶体溶于水,加入足量浓NaOH溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体 | |
| C. | 丙同学为检验Fe3O4中+2价铁元素:先用稀盐酸溶解Fe3O4,再滴加KMnO4溶液 | |
| D. | 丁同学要验证FeCl3与KI反应的限度:可将少量的FeCl3溶液与过量的KI溶液混合,充分反应后用CCl4萃取,静置,再滴加KSCN溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com