
������ʵ����ʵ���ó�����Ӧ������ȷ����
ʵ����ʵ | ���� | |
�� | ��ij����ͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ | ������һ����SO2 |
�� | ��ȼ�յ�þ������CO2���ܼ���ȼ�� | ��ԭ�ԣ�Mg��C |
�� | NaHCO3��Һ��NaAlO2��Һ��ϲ�����ɫ���� | ���ԣ�HCO3-��Al��OH��3 |
�� | �����°�����ȼ���������ڷŵ�ʱ����������Ӧ | �ǽ����ԣ�P��N |
�� | ��CO2ͨ��Na2SiO3��Һ�У��а�ɫ�������� | ���ԣ�H2CO3��H2SiO3 |
�� | ����Һ�еμ������ữ��BaCl2��Һ���ְ�ɫ���� | ����Һ��һ����SO42�� |
A���٢ڢ� B���٢ܢ� C���ڢۢ� D���ܢݢ�
 ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д� �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���һ�����pH=12��Ba(OH)2��Һ����μ���һ�����ʵ���Ũ�ȵ�NaHSO4��Һ������Һ�е�Ba2+ǡ����ȫ����ʱ����ҺpH=11����������ԼӺͣ���V(Ba(OH)2����V( NaHSO4��Ϊ�� ��
A��1��4 B��1��1 C��1��2 D��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪�ֳ��������ѧУ�����ϵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ����٤��������ֵ������˵������ȷ����
A�����³�ѹ�£�11.2L��NO2��CO2������庬��NA��Oԭ��
B����״���£�22.4L����ϩ�к��еĹ��õ��Ӷ���Ϊ12NA
C��1L0.1mol��L��1�İ�ˮ�к���0.1NA��OH?
D����ʯīΪ�缫����Ȼ�ͭ��Һʱ����������ʧȥ����NA������������������32g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������������������ѧ��һ��10�»�ѧ���������棩 ���ͣ�������
��1��Nԭ�ӵ�Ħ��������_________��1mol HNO3��������____________�� 1mol HNO3Լ����_________________����ԭ��.
��2����״����11.2L HCl��������ʵ�����______________,����HCl���� ����ˮ�����1L��Һ,����������Һ�����ʵ���Ũ����____________________.
��3��2mol OH? Լ����___________________������.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ������ѧ��12�µ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��������Ϊa��ij���ʵ���Һmg����������Ϊb�ĸ����ʵ���Һng��Ϻ�������pgˮ���õ�����Һÿ��������Ϊqg�����ʵ���Ũ��Ϊc�������ʵķ���������Է���������Ϊ( )
A��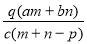 B��
B��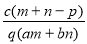 C��
C��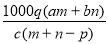 D��
D��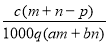
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ������
���������ۡ�8��12���ش���ֱ�ը�¹ʣ���һ�����������ǶԻ�������Ĺ�ע��
��1��Ϊ�˼��ٿ�����SO2���ŷţ�����ȡ�Ĵ�ʩ�ǽ�úת��Ϊ�������ȼ�ϡ�
��֪��H2(g)��1/2O2(g)==H2O(g) ��H1����241.8 kJ��mol��1
C(s)��1/2O2(g)===CO(g) ��H2����110.5 kJ��mol��1
��̿��ˮ������Ӧ����CO���Ȼ�ѧ����ʽΪ�� ��
��2������CaC2�������ơ������ص������ܹ���ˮ��Ӧ���ֺ��Ԯ���������˺ܶ����ѡ������ʵ���ң��㴦���������Ż�ķ����� ��
��3���¹ʷ�����,��ը����������ը������¥�ܱ��Լ����ӵȴ����ܵ������ص��軯����Ⱦ������NaCN�ķ����ǣ���NaClO�ڼ��������¸�NaCN��Ӧ�������������ʣ���д���÷�Ӧ�����ӷ�Ӧ����ʽ ��
��4���绯ѧ���ⷨ����������ˮ�������ε���Ⱦ���绯ѧ����NO3-��ԭ����ͼ��ʾ����Դ����Ϊ ���a����b���������ܷ�ӦΪ4NO3-+4H+=5O2��+2N2��+2H2O����������ӦʽΪ ��

��5�������ͷ�ˮ���ؽ���Ԫ�ظ��Ķ��ԣ��ɽ�Cr2O72-ת��ΪCr(OH)3������ȥ����֪�ڳ����£�Ksp[Fe(OH)2]= 1��10��15��Ksp[Fe(OH)3]= 1��10��38 ��Ksp[Cr(OH)3]= 1��10��23 ��������Ũ����1��10��5mol/L����ʱ��Ϊ�������Ѿ���ȫ��������ش�
����ͬ�¶���Fe(OH)3���ܽ�� Cr(OH)3���ܽ�ȣ��>������<����=����
��Ũ��Ϊ0.1mol/L��Fe2+��10. 0mol/L Cr3+ͬʱ���ɳ�����pH��Χ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ��д��ȷ����
A�� Na2O ����ˮ��Na20+ H2O=2Na+ + 20H��
B���� Ca(C10)2 ��Һ��ͨ����� C02 �� 2C10-+H20+C02=2HC1O+CO32-
C����FeC13��Һ��ʴͭ�壺Fe3ʮʮCu=Fe2ʮʮCu2ʮ
D��̼�������ϡ����:CaCO3+2H+=Ca2++CO2 +H20
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij���������Ļ����Һ20 mL�����к��������Ũ��Ϊ2 mol��L��1�����������Ũ��Ϊ1 mol��L��1���������м���0.96 g ͭ�ۣ���ַ�Ӧ��(����ֻ����NO����)�������ռ�����״���µ���������Ϊ ( )
A��224 mL B��168 mL C��112 mL D��448 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͭ��һ����Ũ���ᷴӦ�õ�����ͭ��Һ��NO2��N2O4��NO �Ļ�����壬��Щ������1.68LO2����״������Ϻ�ͨ��ˮ�У�����������ȫ��ˮ�����������ᡣ������������ͭ��Һ�м���5mol/LNaOH��Һ��Cu2+ ǡ����ȫ������������NaOH��Һ������ǣ� ��
A��60mL B��45mL C��30mL D��15mL.
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com