
【题目】下列化学方程式或离子方程式,书写规范、正确的是(反应条件略)
A. 
B. 
C. 苯酚钠溶液中通入少量二氧化碳的离子方程式:![]() +H2O+CO2→
+H2O+CO2→![]() +HCO3-
+HCO3-
D. 乙酸与碳酸钠溶液反应的离子方程式:2H++CO32-=CO2↑+H2O
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要意义。对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
2NH3(g),在673 K、30 MPa下,n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
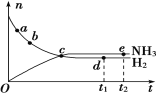
A. 点a的正反应速率比点b的小B. 点c处反应达到平衡
C. 点d(t1时刻)和点e(t2时刻)处n(N2)不一样D. 点e处反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于温度与反应方向的关系,下列判断不正确的是( )
A.ΔH<0,ΔS>0,所有温度下反应自发进行
B.ΔH>0,ΔS>0,所有温度下反应自发进行
C.ΔH<0,ΔS<0,低温下反应自发进行
D.ΔH>0,ΔS<0,所有温度下反应不能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人类必需的生命元素,在人体的生长发育过程中起着重要作用,实验小组进行碘单质的制备。
【查阅资料】碱性条件下,I2会发生歧化反应生成I-和IO3-,酸性条件下, I-和IO3-又会发生归中反应生成I2;碘在水中的溶解度为0.029g。
【碘的制取】以海带为原料,按照以下步骤进行实验。

(1)将海带灼烧成灰后再用水浸取,目的是_______________。
(2)步骤B发生的反应是“氧化”,这一操作中可供选用的试剂: ①Cl2;②Br2;③稀硫酸和H2O2,从无污染角度考虑,你认为合适试剂是______(填编号),反应中I-转化为I2 的离子反应方程式为_______________。
(3)步骤C中使用的起到分离作用的仪器是_____________,使用该仪器时,第一步操作是_______________。
(4)有同学查资料后发现CCl4有毒,提议用乙醇代替,请判断该提议是否可行,原因是_______________。
【碘的分离】得到含I2的CCl4溶液后,利用右图装置进行碘的提取并回收溶剂。

(5)图中有两处明显错误,分别是①_________;②_________。
(6)对实验装置的错误改正之后进行分离操作。预期锥形瓶中得到无色的CCl4,实验结果锥形瓶中得到紫红色液体,请分析出现该实验结果的原因____________,为了保证实验成功,请提出改进方案:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的示意图如下。
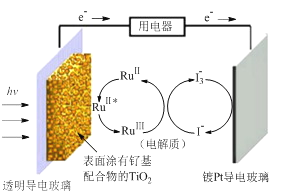
电池工作时发生的反应为:
RuII ![]() RuII *(激发态)
RuII *(激发态)
RuII *→RuIII+e-
I3-+ 2e-→3I-
RuIII+3I-→RuII++ I3-
下列关于该电池叙述错误的是 ( )
A. 电池中镀Pt导电玻璃为正极
B. 电池工作时,I-离子在镀Pt导电玻璃电极上放电
C. 电池工作时,电解质中I-和I3-浓度不会减少
D. 电池工作时,是将太阳能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OH![]() ClO+Cl+H2O是放热反应。
ClO+Cl+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
(2)步骤Ⅱ合成N2H4·H2O的装置如题19图1所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_____________;使用冷凝管的目的是_________________________________。

(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3(水溶液中H2SO3、![]() 、
、![]() 随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。
随pH的分布如题19图2所示,Na2SO3的溶解度曲线如题19图3所示)。

①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通SO2的实验操作为_________________。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案: _______________________,用少量无水乙醇洗涤,干燥,密封包装。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求写出下列反应的离子方程式(标明化学方程式的除外)
(1)Na2S溶液和AgNO3溶液混合:_____________。
(2)硫磺与足量浓NaOH溶液共热,其中一种产物为Na2SO3: _____________。
(3)灭火器中NaHCO3与Al2(SO4)3溶液混合: _____________。
(4)工业流程中除去溶液中Fe3+时,也可采用以下方法:将pH值调整到1.6~1.8左右,并将溶液加热至85~95℃时,加入适量Na2SO4,析出淡黄色晶体黄钠铁矾Na2Fe6(SO4)4(OH)12,反应的离子方程式为______________。
(5)含0.300molH3PO4的水溶液滴加到含0.500molCa(OH)2的悬浊液中,反应恰好完全,生成1种难溶盐和16.2gH2O。反应的化学方程式为______________。
(6)向一定比例的CuSO4、NaCl溶液中加入一定量的Na2SO3溶液可制得CuCl白色沉淀,并有刺激性气味气体产生: _____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com