
| A. | 书写共价化合物的电子式只需把结构式中的一个单键改成一对电子即可 | |
| B. | 已知  ,可见,成键的一方不提供电子也可能形成化学键 ,可见,成键的一方不提供电子也可能形成化学键 | |
| C. | 将某种化合物溶于水,若能导电说明这种化合物是离子化合物 | |
| D. | 只要是离子化合物其熔点就比共价化合物的熔点高 |
分析 A.将共用电子对用一条短线来代替所得到的式子即为结构式,书写共价化合物的电子式不只需把结构式中的一个单键改成一对电子,分子中存在较复杂的π键等;
B.成键的一方不提供电子也可能形成化学键,如共价键中形成的配位键;
C.共价化合物溶于水也会导电;
D.原子构成的共价化合物形成的是原子晶体熔沸点可能高于离子化合物;
解答 解:A.书写共价化合物的电子式不只需把结构式中的一个单键改成一对电子,如苯分子中存在大π键,电子式书写不同,故A错误;
B.成键的一方不提供电子也可能形成化学键,如 ,故B正确;
,故B正确;
C.将某种化合物溶于水,若能导电说明这种化合物可能是离子化合物或共价化合物,如NaCl、HCl等,故C错误;
D.原子构成的共价化合物形成的是原子晶体熔沸点可能高于离子化合物,如二氧化硅熔沸点高于某些化合物,故D错误;
故选B.
点评 本题考查了常见物质的电子式和结构式的书写、化合物性质分析判断,应注意的是书写电子式之前先判断此化合物中的化学键的类型,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L SO3中含有氧原子数目为3.0NA | |
| B. | 常温常压下,12.2g NaHSO4中含有离子总数为0.3NA | |
| C. | 在标准状况下,11.2L N2和O2混合气体中所含分子数为0.5NA | |
| D. | 某密闭容器盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | F |
| 原子半径/nm | 0.077 | 0.075 | 0.117 |
| 主要化合价 | +4、-4 | +5、-3 | +4、-4 |
| 元素 | D | M | G | E |
| 性质结构信息 | 单质制成的高压灯,发出的黄光透雾力强,射程远 | 氢化物常温下呈液态,M的双原子阴离子有18个电子 | 原子核外的M层比L层少2个电子 | +3价阳离子的核外电子排布与氖原子相同 |
 ,此化合物中含有的化学键类型(填离子键,共价键或非极性键)离子键和非极性键共价键.
,此化合物中含有的化学键类型(填离子键,共价键或非极性键)离子键和非极性键共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | W |
| T |
| A. | 含Y元素的盐水溶液可呈酸性或碱性 | |
| B. | 气态氢化物的稳定性:X>W>Z | |
| C. | 根据元素周期律推测,金属性T比Y强 | |
| D. | Z单质性质不活泼.在自然界中有游离态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个D2O分子中所含中子数为8 | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<HNO3 | D. | 碱性强弱:KOH>NaOH>Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子的结构是由键角决定的 | |
| B. | 共价键的键能越大,共价键越牢固,由该键形成的分子越稳定 | |
| C. | CF4、CCl4、CBr4、CI4中C-X键的键长、键角均相等 | |
| D. | H2O分子中的共价键比HF分子中的共价键牢固 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海带中提取碘单质的过程涉及氧化还原反应 | |
| B. | 往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输 | |
| C. | 赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的 | |
| D. | 从海水中获得食盐和淡水必须经过化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
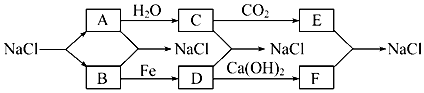
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜电极应与Y电极相连接 | |
| B. | H十透过质子交换膜由左向右移动 | |
| C. | 当N电极消耗0.25mol气体时,则铁电极增重16g | |
| D. | M电极反应式为:CO(NH2)2+H2O-6e-═CO2↑+N2↑+6H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com