
分析 某烷烃A在同温同压下蒸汽的密度是H2的29倍,则其相对分子质量为29×2=58,分子中C原子数目为$\frac{58-2}{14}$=4,故A的分子式为C4H10,在一定条件下对烷烃A进行催化裂解,得到两种烃B和C,烃C能使溴水褪色,已知烃B中氢的质量分数为25.0%,则B中碳、氢原子数目之比为$\frac{1-25%}{12}$:$\frac{25%}{1}$=1:4,则B为CH4,C为CH2=CHCH3.
解答 解:某烷烃A在同温同压下蒸汽的密度是H2的29倍,则其相对分子质量为29×2=58,分子中C原子数目为$\frac{58-2}{14}$=4,故A的分子式为C4H10,在一定条件下对烷烃A进行催化裂解,得到两种烃B和C,烃C能使溴水褪色,已知烃B中氢的质量分数为25.0%,则B中碳、氢原子数目之比为$\frac{1-25%}{12}$:$\frac{25%}{1}$=1:4,则B为CH4,C为CH2=CHCH3.
(1)烃A的分子式:C4H10,故答案为:C4H10;
(2)B为CH4,为正四面体结构,且二氯代物的结构有1种,故答案为:1;
(3)烃C与溴水反应的化学方程式为:CH2=CHCH3+Br2→BrCH2CHBrCH3,
故答案为:CH2=CHCH3+Br2→BrCH2CHBrCH3.
点评 本题考查有机物的推断,关键是利用相对分子质量与烷烃通式确定A的分子式,侧重考查学生分析计算能力,熟练掌握有机化学基础.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | 足球烯(C60)在苯中的溶解度大 | 足球烯是原子晶体 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
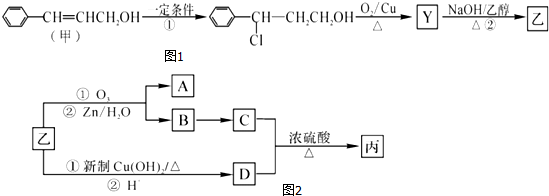
 .
. ;
;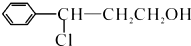 →Y:
→Y: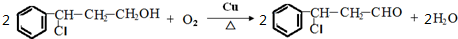 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(NH4+)>c(Cl-)>c(H+)>c(OH-) | B. | c(Na+)+c(H+)=c(Cl-)+c(OH-) | ||
| C. | c(NH4+)+c(NH3•H2O)=0.10mol•L-1 | D. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浓硫酸与蛋白质的颜色反应鉴别部分蛋白质 | |
| B. | 用乙醇从碘水中萃取碘 | |
| C. | 用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸 | |
| D. | 用食醋浸泡有水垢的水壶清除其中的水垢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com