
容积固定为3 L的某密闭容器中加入1 mol A、2 mol B,一定温度下发生如下反应:A(s)+2B(g)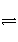
 C(g)+D(g),经反应5 min后,测得C的浓度为0.3 mol·L-1。则下列说法中正确的是( )
C(g)+D(g),经反应5 min后,测得C的浓度为0.3 mol·L-1。则下列说法中正确的是( )
A.5 min内D的平均反应速率为0.02 mol·L-1·min-1
B.5 min内A的平均反应速率为0.06 mol·L-1·min-1
C.经5 min后,向容器内再加入C,正反应速率变小
D.平衡状态时,生成1 mol D时同时生成1 mol A
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4L CCl4含有的分子数为 NA
B.2.4gMg溶于足量稀盐酸,转移的的电子数为0.1NA
C.通常状况下,32gO2与32gO3所含的氧原子数均为2NA
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 的数目为 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
除去工业尾气中的氮氧化物,常用氨催化吸收法。原理是NH3与NOx反
应生成无毒物质。某同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。
(一)提供的装置
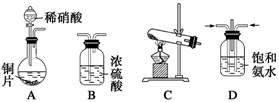
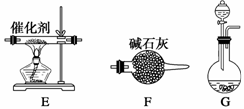
(二)NH3的制取
(1)下列有关实验室制备气体的说法正确的有 (填序号)。
① 用赤热的炭与水蒸气反应制取氢气 ② 用排饱和食盐水的方法收集氯气
③ 实验室制氧气有时需要加热,有时不需要加热 ④ 用无水氯化钙干燥氨气
(2)若选择装置G制取氨气,则分液漏斗中盛装的液体试剂是 。
(3)若选择装置C制取氨气,则反应的化学方程式是 。
(三)模拟尾气的处理
选用上述部分装置,按下列顺序连接成模拟尾气处理装置,回答有关问题:
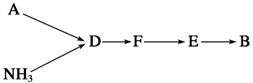
(4)A装置中反应的离子方程式为__________________________________。
(5)D装置中的液体可换成 (填序号)。
a . CuSO4 b . H2O c . CCl4 d . 浓硫酸
(6)该同学所设计的模拟尾气处理实验存在的明显缺陷是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对达到平衡状态的可逆反应:A+B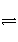
 C+D,若t1时增大压强,正、逆反应速率变化如图所示(v代表反应速率,t代表时间),下列有关A、B、C、D的状态叙述中正确的是( )
C+D,若t1时增大压强,正、逆反应速率变化如图所示(v代表反应速率,t代表时间),下列有关A、B、C、D的状态叙述中正确的是( )
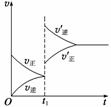
A.A、B、C是气体,D不是气体
B.A、B是气体,C、D有一种是气体
C.C、D是气体,A、B有一种是气体
D.C、D有一种是气体,A、B都不是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
能源是人类生存和发展的重要支柱。研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义。已知下列热化学方程式:
①2H2(g)+O2(g)===2H2O(l) ΔH=-570 kJ·mol-1;
②H2(g)+1/2O2(g)===H2O(g) ΔH=-242 kJ·mol-1;
③C(s)+1/2O2(g)===CO(g) ΔH=-110.5 kJ·mol-1;
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1;
⑤CO2(g)+2H2O(g)===2CH4(g)+2O2(g) ΔH=+890 kJ·mol-1
回答下列问题:
(1)上述反应中属于吸热反应的是___________________________________________。
(2)H2的燃烧热为_______________________________________________________。
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。已知C(s)+H2O(g)===H2(g)+CO(g) ΔH=a kJ·mol-1;则a=________;该反应的熵ΔS________0(选填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学键说法中不正确的是 ( )
A.化学键是一种作用力
B.化学键可以使离子相结合,也可以使原子相结合
C.化学反应过程中,反应物分子内化学键断裂,生成物分子内化学键形成
D.非极性键不是化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
有短周期元素A、B、C、D、E,已知:① 常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜 ;② B元素的原子序数比A元素大,其原子的次外层的电子数是最外层电子数的2倍 ;③ E与A同周期,C、D、E三种元素形成的单质或化合物可发生如下图所示的反应。
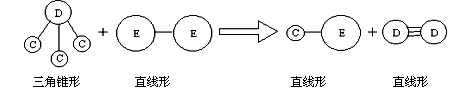
请回答下列问题:
(1)写出A元素最高价氧化物与NaOH溶液反应的离子方程式: ;
(2)D元素的原子结构示意图是: ;
(3)B元素与E元素的最高价氧化物的水化物的酸性强弱(用化学式表示):
> ;
(4)请用化学方程式表示E元素的单质在工业上的一种重要用途: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸、硫代硫酸(H2S2O3)等,其中硫酸最为重要,在工业上有广泛的应用。
完成下列计算:
(1) 浓硫酸与铜在加热时发生反应,生成二氧化硫气体的体积为4.48L(标准状况),若将反应后的溶液稀释至500mL,该溶液中硫酸铜的物质的量浓度为 mol·L-1;
(2)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸,若将445g焦硫酸溶于水配成4.00L硫酸,该硫酸的物质的量浓度为 mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com