
| A. | 乙酸乙酯的结构简式:CH3CH2COOCH3 | |
| B. | 丙烯的键线式 | |
| C. | 乙醇的结构式: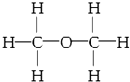 | |
| D. | 乙烯的结构简式:CH2=CH2 |
分析 A.乙酸乙酯为乙酸与乙醇发生酯化反应生成的酯;
B. 为2-丁烯,丙烯分子中含有3个C;
为2-丁烯,丙烯分子中含有3个C;
C. 为二甲醚的结构式,乙醇分子中含有羟基;
为二甲醚的结构式,乙醇分子中含有羟基;
D.乙烯分子中含有2个C原子和1个碳碳双键.
解答 解:A.CH3CH2COOCH3为丙酸甲酯,乙酸乙酯正确的结构简式为:CH3COOCH2CH3,故A错误;
B.丙烯的结构式为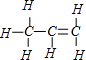 ,则丙烯的键线式为
,则丙烯的键线式为 ,故B错误;
,故B错误;
C.乙醇中含有CH3CH2-和-OH,乙醇正确的结构式为: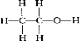 ,故C错误;
,故C错误;
D.乙烯分子中含有1个碳碳双键,其结构简式为:CH2=CH2,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及结构式、结构简式、键线式等知识,明确常见化学用语的表示方法为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:选择题
| A. | 溶液中一定含Cu2+ | B. | 溶液中不一定含Fe2+ | ||
| C. | 剩余固体一定含Cu和Fe | D. | 加入KSCN溶液一定不变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
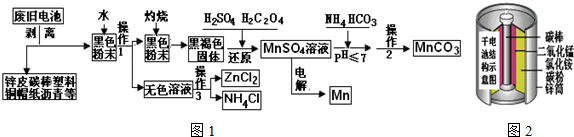
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氧、稀硫酸、氨气 | B. | 干冰、氢氧化镁、氢氧化铁胶体 | ||
| C. | 冰、氯化钠固体、乙醇 | D. | 生石灰、熟石灰、石灰石 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Fe2+、Cr2O72-、SO42- | B. | Na+、OH-、SO42-、HCO3- | ||
| C. | K+、Mg2+、SO42-、OH- | D. | H+、K+、CO32-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2+2NaOH═NaCl+NaClO+H2O | B. | Fe+CuSO4═FeSO4+Cu | ||
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | D. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若A、B均能发生消去反应,则C一定能发生消去反应 | |
| B. | 若 A、B分子中分别含有1个、2个碳原子,则C的摩尔质量不小于60g.mol-1 | |
| C. | 若A是乙醇,则B可能是丙三醇 | |
| D. | 若A、B均存在醇类同分异构体,则 C一定存在醇类同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com