
| A. | 氧化还原反应一定有单质参与 | |
| B. | 氧化还原反应的实质是电子转移 | |
| C. | 有元素化合价升降的反应一定是氧化还原反应 | |
| D. | 氧化剂在反应中化合价降低 |
分析 A.存在元素化合价变化的反应是氧化还原反应;
B.氧化还原反应的特征为化合价的变化,实质为电子转移;
C.氧化还原反应的特征为化合价的变化;
D.氧化剂中元素的化合价降低.
解答 解:A.存在元素化合价变化的反应是氧化还原反应,氧化还原反应中不一定有单质参加,如硫酸亚铁与硝酸的反应生成硫酸铁、NO和水,故A错误;
B.氧化还原反应的特征为化合价的变化,实质为电子转移,故B正确;
C.氧化还原反应的特征为化合价的变化,则有元素化合价升降的反应一定是氧化还原反应,故C正确;
D.氧化剂中存在某种元素得电子,其化合价降低,故D正确.
故选A.
点评 本题考查氧化还原反应,明确元素的化合价是解答本题的关键,注意把握氧化还原反应的特征与实质,难度不大.


科目:高中化学 来源: 题型:解答题
 下列装置中,a5是铁电极,其余为石墨电极,烧杯中液体体积均为100mL,放置一段时间后(溶质都有剩余),回答下列问题(不考虑溶液体积变化)
下列装置中,a5是铁电极,其余为石墨电极,烧杯中液体体积均为100mL,放置一段时间后(溶质都有剩余),回答下列问题(不考虑溶液体积变化)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
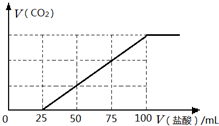 钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
钠及其化合物在生产和生活中有广泛的应用.完成下列计算:| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发利用了溶质的溶解性随温度升高而降低的性质 | |
| B. | 蒸馏利用了液体沸点不同的性质 | |
| C. | 萃取利用了物质在不同溶剂中溶解度不同的性质 | |
| D. | 分液利用了两种液体互不相溶且密度不同的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 酸雨的PH为5.6 | |
| B. | 酸雨的形成过程发生了氧化还原反应 | |
| C. | 酸雨的主要成分为氮、硫元素的氧化物 | |
| D. | 形成酸雨的主要原因是因为雷雨天气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖能发生水解反应生成乙醇和二氧化碳 | |
| B. | 氨基乙酸、氯乙烯、乙二醇均可发生聚合反应 | |
| C. | 实验室用溴乙烷在浓硫酸、170℃条件下制备乙烯 | |
| D. | 苯酚能跟碳酸钠溶液反应,苯酚的酸性比碳酸强 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:选择题
在pH=1溶液中能大量共存的是
A.Na+、SO42-、Ba2+、Cl- B.Na+、K+、CH3CHOO-、NO3-
C.H+、Cu2+、OH-、CO3- D.Na+、K+、Cl-、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com