
SO2的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论。其原因是 (用化学方程式表示)。为进一步研究酸雨的成分,该同学取某一时段的这种雨水V L,加入0.5 mol ·L—1的Ba(OH)2溶液至不再产生沉淀时,恰好消耗40.00 mL Ba(OH)2溶液。请计算:
①该V L雨水中共溶解的SO2体积是___ mL(标准状况)。
②若在上述实验中生成沉淀物的质量为4.50 g,该雨水中含有H2SO3的物质的量浓度是多
少?(要求写出计算过程)
H2SO3+O2=H2SO4
设V L雨水中含有H2SO3的物质的量为n1,含有H2SO4的物质的量为n2
H2SO3+ Ba(OH)2 =BaSO3 ↓+2H2O H2SO4+Ba(OH)2 =BaSO4 ↓+2H2O
n1+ n2 =0.5mol·L-1×0.0400 L,
共溶解的SO2体积V(SO2)=0.02mol×22.4 L· mol—1×1000mL ·L—1= 448 mL
217g·mol-1 n1+233g·mol-1 n2 =4.50 g
n1=0.01 mol
c(H2SO3)=0.01/V mol ·L—1
【解析】考查酸雨的形成及有关计算等。亚硫酸碱液还原性,能被氧化生成强酸硫酸。所以pH减小,方程式为H2SO3+O2=H2SO4。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
 N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.
N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 污染指数 | 首要污染物 | 空气质量等级 | 空气质量状况 |
| 55 | SO2 | Ⅱ | 良 |

查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
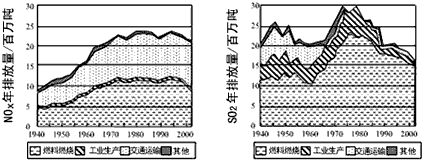
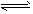 N2+2CO2将有害的污染物转化为可参与大气循环的N2和CO2。在某温度下用气体传感器测得不同时间的NO和CO浓度如下表
N2+2CO2将有害的污染物转化为可参与大气循环的N2和CO2。在某温度下用气体传感器测得不同时间的NO和CO浓度如下表
查看答案和解析>>
科目:高中化学 来源:2011年浙江省杭州市萧山区高考化学模拟试卷(二十二)(解析版) 题型:填空题

 N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.
N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.| 时间/h | 1 | 2 | 3 | 4 | 5 | |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com