
在水溶液中,重铬酸钾K2Cr2O7存在以下平衡: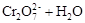

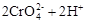 ,下列说法正确的是
,下列说法正确的是
| A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色 |
| B.该反应不是氧化还原反应 |
| C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大 |
D.该反应的平衡常数表达式是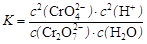 |
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:单选题
对于可逆反应H2(g) + I2(g) 2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
| A.H2(g)的消耗速率与HI(g)的生成速率比为2:1 |
| B.反应进行的净速率是正、逆反应速率之差 |
| C.正、逆反应速率的比值是恒定的 |
| D.达到平衡时,正、逆反应速率不一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
T10C 时,将9molCO2和12molH2充入3L密闭容器中,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH <0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法正确的是
CH3OH(g)+H2O(g) ΔH <0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法正确的是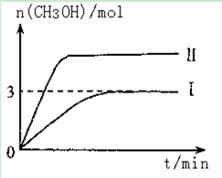
| A.曲线II对应的条件改变是减小压强 |
| B.若T2°C时上述反应的平衡常数为0.42,则T2< T1 |
| C.在T10C,若起始时向容器中充入5 mol CO2、5 mol H2、5 mol CH3OH(g)和 5 mol H2O(g),则达平衡前v(正)>v(逆) |
| D.在T10C,若起始时向容器中通入4 .5 molCO2、6mol H2 ,平衡时容器内的压强P1=P/2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是( )
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
| A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
| C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
| D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)  ?nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
?nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
| 容器体积/L 温度/℃ c(Y)/mol·L-1 | 1 L | 2 L | 4 L |
| 100℃ | 1.00 | 0.75 | 0.53 |
| 200℃ | 1.20 | 0.90 | 0.63 |
| 300℃ | 1.30 | 1.00 | 0.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知:2M(g) N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器
N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器
中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )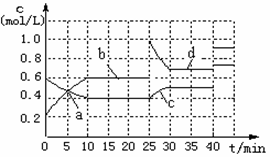
| A.a、b、c、d四个点中处于平衡状态的点是a、b |
| B.反应进行至25min时,曲线发生变化的原因是加入了 0.4molN |
| C.若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
| D.若40min后出现如图所示变化,则可能是加入了某种催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是 ( )
| A.碳酸铵分解是吸热反应,根据焓判据判断能自发分解 |
| B.多次洗牌以后,扑克牌的毫无规律的混乱排列的几率大,越混乱,熵值越大 |
| C.水总是自发地由高处往低处流,这是一个自发反应 |
| D.室温下水结成冰是自发过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定条件下,固定容积的密闭容器中反应:2NO2(g)  2NO(g)+O2(g)△H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
2NO(g)+O2(g)△H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是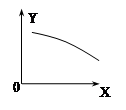
| A.X表示温度时,Y表示NO2物质的量 |
| B.X表示NO2物质的量,Y表示O2的物质的量 |
| C.X表示反应时间时,Y表示混合气体的密度 |
| D.X表示压强时,Y表示NO2的含量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com