
【题目】下列化合物中既能发生消去反应,又能发生水解反应的是( )
A.乙醇
B.氯甲烷
C.氯乙烷
D.乙酸乙酯
科目:高中化学 来源: 题型:
【题目】“探险队员”﹣盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过. 
(1)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有个,属于氧化还原反应的有个,其中能“吃掉”盐酸的盐是(填化学式),写出该反应的离子方程式 .
(2)在不能与盐酸反应的物质中,属于电解质的是(填写物质序号,下同),属于非电解质的是
(3)请你帮助它走出迷宫(用图中物质前的序号连接起来表示所走的路线)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
![]() 试通过计算和推理完成下面的问题:
试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成。A应该属于________(用字母代号填写)。
a. 酸 b. 碱 c. 盐 d. 酸性氧化物 e. 碱性氧化物
(2)A物质可以使酸性![]() 溶液褪色,此反应中(填写化学式,下同)_______失去电子,氧化剂是________。
溶液褪色,此反应中(填写化学式,下同)_______失去电子,氧化剂是________。
(3)足量的铜片与10mL 18mol/L的浓![]() 充分反应,如果该反应过程中转移了0.1mol电子,生成的
充分反应,如果该反应过程中转移了0.1mol电子,生成的![]() 的物质的量为_______mol,生成的A气体在标准状况下体积为________L(假设气体全部逸出)。
的物质的量为_______mol,生成的A气体在标准状况下体积为________L(假设气体全部逸出)。
(4)计算:将反应后得到的溶液与足量![]() 溶液混合,充分反应。反应后所得沉淀的质量为______g。
溶液混合,充分反应。反应后所得沉淀的质量为______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在工业上常用CO和H2合成甲醇,反应方程式为:CO(g)+2H2(g)CH3OH(g)△H=akJ/mol
已知:①CO(g)+ ![]() O2(g)═CO2(g)△H1=﹣283.0kJ/mol
O2(g)═CO2(g)△H1=﹣283.0kJ/mol
②H2(g)+ ![]() O2(g)═H2O(g)△H2=﹣241.8kJ/mol
O2(g)═H2O(g)△H2=﹣241.8kJ/mol
③CH3OH(g)+ ![]() O2(g)═CO2(g)+2H2O(g)△H3=﹣192.2kJ/mol
O2(g)═CO2(g)+2H2O(g)△H3=﹣192.2kJ/mol
答下列问题:
(1)a=
(2)能说明反应CO(g)+2H2(g)CH3OH(g)已达平衡状态的是(填字母).
A.单位时间内生成1mol CH3OH(g)的同时消耗了1mol CO(g)
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,气体的平均摩尔质量不再变化
(3)在T1℃时,体积为2L的恒容容器中充人物质的量之
和为3mol的H2和CO,反应达到平衡时CH3OH的体积分数(V%)与 ![]() 的关系如图1所示.
的关系如图1所示.
①当起始 ![]() =2,经过5min达到平衡,CO的转化率为0.6,则0~5min内平均反应速率v(H2)= . 若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将(选填“增大”、“减小”或“不变”);
=2,经过5min达到平衡,CO的转化率为0.6,则0~5min内平均反应速率v(H2)= . 若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将(选填“增大”、“减小”或“不变”);
②当 ![]() =3.5时,达到平衡状态后,CH3 OH的体积分数可能是图像中的点(选填“D”、“E”或“F”)
=3.5时,达到平衡状态后,CH3 OH的体积分数可能是图像中的点(选填“D”、“E”或“F”)
(4)CO和H2来自于天然气.已知CO2(g)+CH4 (g)2CO(g)+2H2 (g).在密闭容器中有浓度均为0.1molL﹣1的CH4与CO2 , 在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如图2,则压强p1p2(选填“大于”或“小于”);当压强为p2时,在y点:v(正)v(逆)(选填“大于”、“小于”或“等于”).若p2=3MPa,则T℃时该反应的平衡常数Kp=MPa2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数). 
(5)含有甲醇的废水会造成环境污染,可通入ClO2气体将其氧化为CO2 . 写出相关反应的离子方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的有()个
①将铁屑放入稀HNO3中,证明Fe比H2活泼
②FeCl3腐蚀Cu 制印刷电路板是由于铁比铜的金属性强
③检验溶液中是否含有Fe2+,取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN 溶液,观察实验现象
④磁性氧化铁溶于稀硝酸的离子方程式为:3Fe2++4H++NO3-==3Fe3++NO↑+3H2O
⑤将NaOH浓溶液滴加到饱和的FeCl3溶液中,制备Fe(OH)3胶体
⑥氢氧化铁与HI溶液反应的离子方程式为: Fe(OH)3+3H+==Fe3++3H2O
⑦铁与水蒸气在高温下的反应产物为Fe2O3 和H2
⑧1mol FeI2与足量氯气反应时转移的电子数为3NA
⑨检验Fe (NO3)2晶体是否氧化变质的方法是将Fe (NO3) 2样品溶于稀H2SO4后,滴加KSCN 溶液,观察溶液是否变红
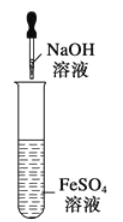
⑩图示装置能较长时间观察到Fe (OH) 2白色沉淀
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境监察局常用“定电位”NOx传感器来监测化工厂的氮氧化物气体是否达到排放标准,其工作原理如图所示.下列说法不正确的是( ) 
A.“对电极”是负极
B.“工作电极”上发生的电极反应为NO2+2e﹣+2H+═NO+H2O
C.传感器工作时H+由工作电极移向对电极
D.对电极的材料可能为活泼金属锌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光纤通讯是光导纤维传送信号的一种通讯手段,合成光导纤维及氮化硅(一种无机涂层)的工艺流程如图: 
回答下列问题:
(1)反应I的化学方程式为 , 氧化剂为(填化学式).
(2)经反应II所得的四氯化硅粗品中所含的物质如表:
组分名称 | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
质量分数 | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
沸点/℃ | 57.6 | 31.8 | 8.2 | ﹣85 | 12.5 | 75.5 |
图中“操作X”的名称为;PCl3的电子式为 .
(3)反应III和IV中尾气的用途为;反应IV的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性大小:羧酸>碳酸>酚,下列含溴化合物中的溴原子,在适当条件下都能被羟其(﹣OH)取代(均可称之为水解反应),所得产物能跟NaHCO3溶液反应的是( )
A.
B.
C.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com