
有关海洋中部分资源的利用(如图)的说法不正确的是( )
|
| A. | 工业上利用Cl2与澄清石灰水反应制取漂白粉 |
|
| B. | 用MgCl2•6H2O晶体制无水MgCl2,需在HCl气流中加热脱水 |
|
| C. | SO2水溶液吸收Br2的化学方程式为Br2+SO2+2H2O═H2SO4+2HBr |
|
| D. | 粗碘中混有少量ICl和IBr,可加入KI进行升华提纯 |
| 海水资源及其综合利用;物质分离和提纯的方法和基本操作综合应用.. | |
| 专题: | 元素及其化合物. |
| 分析: | A.应该用Cl2与石灰乳制制取漂白粉; B.为了抑制Mg2+水解; C.溴单质能把SO2氧化为硫酸; D.ICl和IBr中I元素均为+1价,与KI中的﹣1价I发生归中反应,生成I2,然后进行升华提纯. |
| 解答: | 解:A.因为澄清石灰水中Ca(OH)2的浓度太小,故应该用Cl2与石灰乳制制取漂白粉,故A错误; B.为了抑制Mg2+水解,MgCl2•6H2O晶体制无水MgCl2时需在HCl气流中加热脱水,故B正确; C.溴单质能把SO2氧化为硫酸,其反应为:Br2+SO2+2H2O═H2SO4+2HBr,故C正确; D.ICl和IBr中I元素均为+1价,与KI中的﹣1价I发生归中反应,生成I2,然后进行升华提纯,故D正确; 故选A. |
| 点评: | 本题考查了工业生产中的化学原理,难度适中,考查了学生对元素及化合物知识的理解和应用能力. |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
某溶液中含有HCO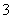 、SO
、SO 、CO
、CO 、CH3COO-4种阴离子.若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的是 ( )
、CH3COO-4种阴离子.若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的是 ( )
A.CH3COO- B.SO
 C.CO
C.CO D.HCO
D.HCO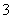
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在指定条件下电离方程式正确的是 ( )
A.Na2CO3溶于水 Na2CO3===Na+CO
B.Al(OH)3酸式电离 Al(OH)3===H++AlO+H2O
C.NaHS溶于水HS-的电离 HS-+H2O H2S+OH-
H2S+OH-
D.NaHCO3加热熔化 NaHCO3===Na++HCO
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能存在Br﹣、CO32﹣、SO32﹣、Al3+、I﹣、Mg2+、Na+等7种离子中的几种.现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
据此可以推断:该溶液中肯定不存在的离子组是( )
|
| A. | Al3+、Mg2+、I﹣、SO32﹣ | B. | Mg2+、Na+、CO32﹣、I﹣ |
|
| C. | Al3+、Na+、SO32﹣、I﹣ | D. | Al3+、CO32﹣、Br﹣、SO32﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学是一门实用的、中心的学科,如果运用不当也会产生负面的影响.下列有关叙述不正确的是( )
|
| A. | 次氯酸和臭氧都是强氧化剂,都能杀死水中的细菌.自来水常用氯气来杀菌消毒,是因为氯气杀菌消毒效果要比臭氧好,且不会残留有毒、有害物质 |
|
| B. | 废旧电池会对生态环境和公众健康造成危害,所以废旧电池必须回收再利用 |
|
| C. | 明矾常用作净水剂,但人体摄入大量铝盐,易患“老年性痴呆症”,所以饮用水不能大量采用明矾作净水剂 |
|
| D. | 氟氯烃是制冷效果极佳的致冷剂,但它会破坏臭氧层,科研人员正在积极研发环保型的替代产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在 1L K2SO4、CuSO4的混合溶液中,c(SO42﹣)=2mol•L﹣1,用石墨作电极电解此溶液,当通电一段时间后(电解完全),两极均收集到22.4L气体(标准状况),原溶液中c(K+)为( )
|
| A. | 0.5 mol•L﹣1 | B. | 1 mol•L﹣1 | C. | 1.5 mol•L﹣1 | D. | 2 mol•L﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质M具有热导率高、高温下电绝缘性好、高温下材料强度大、无毒等优异性能.经检测,M中只含有两种短周期元素.现取82gM溶于适量的NaOH溶液中恰好反应,得到无色溶液A和44.8L气体B(气体体积为标准状况下),该气体能使红色石蕊试纸变蓝.往反应后的溶液中逐滴加入盐酸,可观察到溶液先变浑浊后变澄清.
物质B有如下转化关系:BCD EE是一种强酸.将c和D的混合物溶解在接近零度的水中,即可得到一种弱酸F的水溶液.请回答下列问题:
EE是一种强酸.将c和D的混合物溶解在接近零度的水中,即可得到一种弱酸F的水溶液.请回答下列问题:
(1)物质M的化学式为 ,属于 晶体(填“分子”、“离子”、“原子”等).
(2)无色溶液A呈碱性,其原因是 (用离子方程式表示).
(3)弱酸F是一种比醋酸酸性稍强的弱酸,很不稳定,通常在室温下易分解.要制得F溶液,可以往冷冻的其钠盐浓溶液中加入或通入某种物质,下列物质不适合使用的是 (填序号).
a.盐酸 b.二氧化碳 c.稀硫酸 d.二氧化硫
(4)工业碱性废水中若含有NO﹣2,可用铝粉除去.已知此反应体系中检测到B气体.写出上述反应的离子方程式 .若改用电解法将废水中NO﹣2转换为N2除去,N2将在 (填“阴极”或“阳极”)生成,电极反应为 .
(5)现发现一种活性很强的化合物G,其组成为NH5,G遇水能产生两种气体,其中一种气体为B,则物质G的电子式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
氮是大气中含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用,减少氮氧化物的排放是环境保护的重要内容之一.请回答下列氮及其化合物的相关问题:
(1)据报道,意大利科学家获得了极具研究价值的N4,其分子结构与白磷分子的正四面体结构相似.已知断裂1mol N﹣N键吸收167kJ热量,生成1mol N≡N键放出942kJ热量,请写出N4气体转变为N2反应的热化学方程式: N4(g)=2N2(g);△H=﹣882kJ/mol .
(2)据报道,NH3可直接用作车用燃料电池,写出该电池的负极反应式: 2NH3+6OH﹣﹣6e﹣=N2+6H2O .
(3)在T1℃时,将5mol N2O5置于10L固定容积的密闭容器中发生下列反应:2N2O5(g)⇌4NO2(g)+O2(g);△H>0.反应至5分钟时各物质的浓度不再发生变化,测得NO2的体积分数为50%.
①求该反应的平衡常数K= 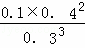 (数字代入式子即可),上述平衡体系中O2的体积分数为 12.5% .
(数字代入式子即可),上述平衡体系中O2的体积分数为 12.5% .
②用O2表示从0~5min内该反应的平均速率υ(O2)= 0.02mol/(L•min) .
③将上述平衡体系的温度降至T2℃,密闭容器内减小的物理量有 AC .
A.压强 B.密度 C.反应速率 D.N2O5的浓度
(4)在恒温恒容的密闭容器中充入NO2,建立如下平衡:2NO2(g)⇌N2O4(g),平衡时N2O4与NO2的物质的量之比为a,其它条件不变的情况下,分别再充入NO2和再充入N2O4,平衡后引起的变化正确的是 B .
A.都引起a减小
B.都引起a增大
C.充入NO2引起a减小,充入N2O4引起a增大
D.充入NO2引起a增大,充入N2O4引起a减小.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中正确的是( )
A.澄清石灰水与稀盐酸反应Ca(OH)2+2H+===Ca2++ 2H2O
2H2O
B.氢氧化钡与硫酸反应OH-+H+===H2O
C.铜片插入硝酸银溶液中Cu+Ag+===Cu2++Ag
D.氯化镁溶液与氢氧化钠溶液反应Mg2++2OH-===Mg(OH)2↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com