
����Ŀ���縡ѡ���۷��ǹ�ҵ�ϲ��õ�һ����ˮ����������������ˮ��pH��5.0- 6.0 ֮�䣬ͨ���������Fe(OH)3���壬Fe(OH)3�����������ԣ�������������������������о�ˮ���ã�ģ���װ����ͼ��ʾ������˵����ȷ����
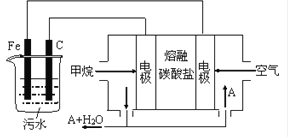
A.��ȼ�ϵ�ظ����ĵ缫��ӦʽΪCH4-8e-+10OH-=CO32-+7H2O
B.����ʱ�������е�CO32-��������
C.�õ�����Fe���ĵ缫��ӦʽΪ: 2H++2e-=H2��
D.Ϊʹ��س�ʱ���ȶ����������в���A���ʲ���ѭ������AΪCO2
���𰸡�D
��������
��ʾ��ͼ��֪�����Ϊȼ�ϵ�أ�ͨ������һ��Ϊ������������������������ʧȥ���ӷ���������Ӧ���ɶ�����̼���缫��ӦʽΪCH4��4CO32����8e����5CO2��2H2O��ͨ��������һ��Ϊ�����������������������µõ����ӷ�����ԭ��Ӧ����̼������缫��ӦʽΪO2��2CO2��4e����2CO32�����ҳ�Ϊ���أ����������������缫Ϊ����������������ʧȥ���ӷ���������Ӧ�����������ӣ��缫��ӦʽΪFe-2e-=Fe2+�����������Ӿ��л�ԭ�ԣ��ܱ������������������������壬�븺��������̼�缫Ϊ�������������������ϵõ����ӷ�����ԭ��Ӧ�����������缫��ӦʽΪ2H+��2e����H2����
A.ͨ������һ��Ϊȼ�ϵ�صĸ�����������������������ʧȥ���ӷ���������Ӧ���ɶ�����̼���缫��ӦʽΪCH4��4CO32����8e����5CO2��2H2O����A����
B.ȼ�ϵ�ع���ʱ�����������ƶ�����CO32-��������B����
C. �����У����������������缫Ϊ����������������ʧȥ���ӷ���������Ӧ�����������ӣ��缫��ӦʽΪFe-2e-=Fe2+����C����
D. �����������̼����Ϊ����ʣ�����ѭ�����õ�����ֻ�ж�����̼����D��ȷ��
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ѽ��������ᡢǿ�ȸߡ������õĿ���ʴ�������䵥�ʼ��仯�����ں��պ��졢����װ������Դ��������ұ�𡢽����ͽ�ͨ������Ӧ��ǰ���������ش��������⣺
(1)�������ѿ�������ȡ�ѷ���������̬ F ԭ�Ӻ�����_____��δ�ɶԵ��ӣ�Ti ԭ���γ�Ti3+ʱ�۲���Ӳ��Ų�ʽΪ_____��
(2)TiO2 ���۵�Ϊ 1800�棬TiCl4 ���۵�Ϊ-25�棬�� TiO2 �ľ�������Ϊ_____��TiCl4 �۵�͵�ԭ��Ϊ_____��
(3)��ij���������ڴ���ϩ���ۺϣ������ͼ��ʾ��
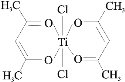
���ѵ���λ��Ϊ_____���û������е縺�����Ԫ����_____(��Ԫ�ط���)��
�ڸ�������в����еĻ�ѧ����_____(����ĸ���)��
a.���Ӽ� b.���� c.������ d.����
(4)��֪ TiO2 ��Ũ���ᷴӦ�����������ѣ��������Ѿ�����������Ϊ��״�ۺ���ʽ�����ӣ��ṹ��ͼ��ʾ���������ӻ�ѧʽΪ_____���������� O ���ӻ���ʽΪ_____�������ӵĿռ乹��Ϊ_____��
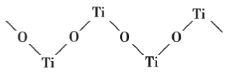
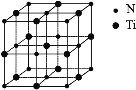
(5)�����ѿ�������������صIJ��ϣ��侧����ͼ���þ������ܶ�Ϊ�� g��cm-3���뵪ԭ��������Ҿ�����ȵ���ԭ����_____������ԭ������ԭ������ľ���Ϊ_____cm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mLFeBr2��Һ��ͨ����������6.72L������ȫ������ԭ�������Һc(Br����=c(Cl������ԭ��Һ��FeBr2��Һ��Ũ�ȣ� ��(mol��L��1)
A.2B.4C.4.5D.6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�ijѧ����0.1 mol��L��1H2SO4��Һ�ζ�0.1 mol��L��1NaOH��Һ���кͺ��ˮ��100 mL�����ζ��յ���ж��������ٵ���һ��H2SO4��Һ���ڶ����һ��H2SO4��Һ(1��Ϊ0.05 mL)����ٺ͢����������������Һ��pH֮����(����)
A. 4B. 4.6C. 5.4D. 6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪NaHC2O4��Һ��pH < 7�������£���pH=8.4��Na2C2O4��Һ�еμ�0.1mol/L��HCl��Һ����ҺpH��pOH[pOH=-lgc(OH-)�ݵı仯��ϵ��ͼ��ʾ�����и�����ʾ��Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ����

A. a�㣺c(H+)+c(HC2O4-)+2c(H2C2O4)=c(OH-)
B. b�㣺c(Cl-)>c(H2C2O4)+c(HC2O4-)+c(C2O42-)
C. c�㣺c(Na+)=c(HC2O4-)+ c(C2O42-)+c(Cl-)
D. d�㣺c(OH-)+ c(Cl-)��c(H+)+2c(H2C2O4)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1Lϡ�����ϡ����Ļ��Һ�������ʵ���Ũ�ȷֱ�Ϊ0.1mol/L��0.4mol/L������û����Һ�м���������ͭ�ۣ������ӷ�Ӧ�ĽǶȷ�������������ܽ�ͭ�۵�����Ϊ�� ��
A. 9.6gB. 6.4 gC. 3.2 gD. 2.4 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����Ѿ���SO2���ʹ����Ϊ0.25 g��L��1��ȡ300.00 mL���Ѿƣ�ͨ���ʵ��ķ���ʹ ����SO2ȫ���ݳ�����H2O2����ȫ������ΪH2SO4��Ȼ����0.090 0 mol��L��1NaOH����Һ���еζ���
���ζ�ǰ������ʱ��Ӧѡ����ͼ�е�________(�����)��
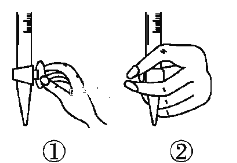
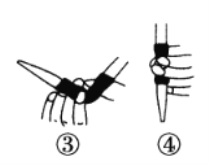
������50 mL�ζ��ܽ���ʵ�飬���ζ����е�Һ���ڿ̶���10�����������Һ������___(�����)��
����10 mL ����40 mL ����10 mL ����40 mL��
�������ζ�ʵ���У���ѡ��___Ϊָʾ����ѡ���ָʾ��ʱ����жϷ�Ӧ����ζ��յ㣺_____��
�ܵζ��յ����ʱ���ӿ̶��ߣ�����������ʵ��ֵ________������ƫ��������ƫ����������Ӱ��������
��2��ijѧ����0.100molL-1��KOH����Һ�ζ�δ֪Ũ�ȵ����ᣬ�����Ϊ��
A����ȡ20mL����������Һע��ྻ����ƿ�У�������2��3�η�̪��
B���ñ���Һ��ϴ�ζ���2��3�Σ�
C����ʢ�б���Һ�ļ�ʽ�ζ��̶ܹ��ã����ڵζ���ʹ���촦������Һ��
D��ȡ��KOH��Һע���ʽ�ζ������̶���0������2��3cm ����
E������Һ������0������0�����¿̶ȣ����¶�����
F������ƿ���ڵζ������棬�ñ�KOH��Һ�ζ����յ㲢���¿̶ȡ�
ʵ���� | KOH��Һ��Ũ�ȣ�mol/L�� | �ζ����ʱ��KOH��Һ����������mL�� | ����������Һ�������mL�� |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
����ȷ���������˳���ǣ��������ĸ��д��___________________________
�ڸ����������ݣ��ɼ�����������Ũ��ԼΪ______________��������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ���ɼס�����������ɣ���ͼ��ʾ�������ǽ���ˮ���Ҷ���[H2N(CH2)2NH2]����Ϊ�����Ѻ������γɵĻ�ѧ��Դ������ع���ʱ������˵��������ǣ� ��
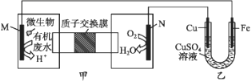
A. ����H+�����ӽ���Ĥ���������ƶ�
B. M���缫��Ӧʽ��H2N(CH2)2NH2+4H2O-16e-![]() 2CO2��+N2��+16H+
2CO2��+N2��+16H+
C. һ��ʱ�������CuSO4��ҺŨ�Ȼ������ֲ���
D. ��N������0.25 mol O2ʱ������������16 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() Ϊ����٤��������ֵ������˵������ȷ����
Ϊ����٤��������ֵ������˵������ȷ����
A.�����£�1LpH=10��![]() ��Һ������
��Һ������![]() ����ĿΪ
����ĿΪ![]() NA
NA
B.�ȼҵ��ת��2mol����ʱ��ͨ�������ӽ���Ĥ��![]() ����ĿΪ2NA
����ĿΪ2NA
C.������ͭ�뺬0.2mol![]() ��Ũ���ᷴӦ��ת�Ƶ��ӵ���Ŀ����0.1NA
��Ũ���ᷴӦ��ת�Ƶ��ӵ���Ŀ����0.1NA
D.��������1LpH=1�Ĵ�����Һ�м�ˮϡ�ͣ�������Һ��![]() ����Ŀ����0.1NA
����Ŀ����0.1NA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com