
����Ŀ���⻯�ƣ�CaH2����һ�ֳ��õĴ�����ϡ�ij��ѧ��ȤС����ȡ�⻯�Ƶ�ʵ��װ����ͼ�����ϣ��⻯��Ҫ�ܷⱣ�棬�ڿ��������ױ��ʡ�����˵������ȷ���ǣ�������
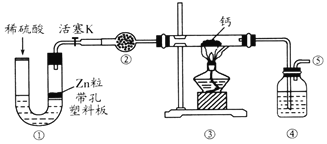
A.�������зֱ�ʢװ��ʯ�Һ�Ũ����
B.��Ӧ������Ӧ��ֹͣ���ȣ�ͨ��һ��ʱ���ٹرջ���K
C.��ȼ�ƾ���ǰ�������Թ��������ռ����岢��ȼ��ͨ�������ж����崿��
D.װ����Ҳ�����ڶ���������Ũ���ᷴӦ�Ʊ�����
���𰸡�D
��������
����ϡ������п��Ӧ���������������ø������������ü�ʯ�ҵȣ����м��������������Ʒ�Ӧ�����⻯�ƣ�������Ũ���ᣬ��������е�ˮ�������������⻯�Ʊ��ʡ�
A��������ʢװ���壬���ü�ʯ�ң�������ʢװҺ�壬����Ũ���ᣬ��A��ȷ��
B����Ӧ������Ӧ��ֹͣ���ȣ�����ͨ����������������ȴ���ٹرջ���K��������屻��������B��ȷ��
C�������������뷴Ӧ�����ڼ��������½��У�Ӧ���ⲻ���������ڼ���ʱ��ը�����ȼ�ƾ���ǰ�������Թ��������ռ����岢��ȼ��ͨ�������ж����崿�ȣ���C��ȷ��
D��װ��������Ҫ���ȷ�Ӧ���ɽ��У����������̺�Ũ�����ڼ��������½��У���װ�����������ڶ���������Ũ���ᷴӦ�Ʊ���������D����
��ѡ��D��


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������F���ж��ص�����ҩ�����ã�ʵ�����ɷ��㻯����A�Ʊ�F��һ�ֺϳ�·�����£�
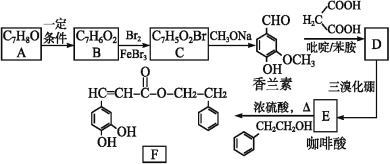
��֪����R��Br![]() R��OCH3
R��OCH3
��R��CHO+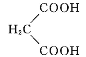
![]() R��CH=CH��COOH
R��CH=CH��COOH
�ش��������⡣
��1��A������Ϊ___��B����C�ķ�Ӧ����Ϊ___��
��2��������Ľṹ��ʽΪ___��
��3��д��F������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��___��
��4��GΪ�����ص�ͬ���칹�壬��ʹFeCl3��Һ����ɫ��������ֻ������ȡ�����ţ��ܷ���ˮ�ⷴӦ������Ҫ���ͬ���칹����___�֣���д����������һ�ֺ˴Ź�������ͼ��ʾ��4�ֲ�ͬ�������⣬�������Ϊ3��2��2��1��G�Ľṹ��ʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������P(s)��Cl2(g)������Ӧ����PCl3(g)��PCl5(g)����Ӧ�����е�������ϵ��ͼ��ʾ(ͼ�е���H��ʾ����1 mol���������)��
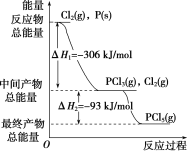
������ͼ�ش��������⣺
(1)P(s)��Cl2(g)��Ӧ����PCl3(g)���Ȼ�ѧ����ʽ��________________________________________________________��
(2)PCl5(g)�ֽ��PCl3(g)��Cl2(g)���Ȼ�ѧ����ʽ��_____________________��
(3)P(s)��Cl2(g)��������Ӧ����1 mol PCl5(g)����H3��____��P(s)��Cl2(g)һ����Ӧ����1 mol PCl5(g)����H4____(������������С��������������)��H3��
(4)��֪1mol���ױ��1mol���ų�18.39KJ�����������������Ȼ�ѧ����ʽ��
4P(���ף�s)��5O2(g)=2P2O5(s)�� ��H1��
4P(���ף�s)��5O2(g)=2P2O5(s)�� ��H2��
����H1����H2�Ĺ�ϵ��ȷ������______��
A����H1����H2���� B����H1����H2 C����H1����H2���� D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��25��Cʱ��Ksp[Mg(OH)2]=5.61��10-12��Ksp[MgF2]=7.42��10-11,����˵����ȷ����
A.25��Cʱ������Mg(OH)2��Һ�뱥��MgF2��Һ��ȣ�ǰ�ߵ�c(Mg2+)��
B.25��Cʱ����Mg(OH)2������Һ����������NH4Cl���壬c(Mg2+)����
C.25��Cʱ��Mg(OH)2������20mL 0.01 mol/L��ˮ�е�Ksp����20mL 0.01mol/L NH4Cl��Һ�е�KspС
D.25��Cʱ����Mg(OH)2������Һ����ŨNaF��Һ��Mg(OH)2������ת����ΪMgF2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��2NO2������ɫ��![]() N2O4����ɫ����H��0����һ������NO2����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵����ȷ���ǣ� ��
N2O4����ɫ����H��0����һ������NO2����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵����ȷ���ǣ� ��
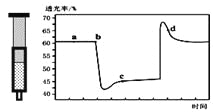
A. b��IJ�����ѹ��ע����
B. c����a����ȣ�c��NO2������c��N2O4����С
C. d �㣺v��������v���棩
D. ����������ϵ�¶ȱ仯����û��������ʧ����T��b����T��c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������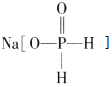 ���������ƣ����л�ѧ��ͭ����Ӧ�Ļ�ѧ����ʽΪ CuSO4+2NaH2PO2+2NaOH=Cu+2NaH2PO3+Na2SO4+H2��������˵����ȷ���ǣ�������
���������ƣ����л�ѧ��ͭ����Ӧ�Ļ�ѧ����ʽΪ CuSO4+2NaH2PO2+2NaOH=Cu+2NaH2PO3+Na2SO4+H2��������˵����ȷ���ǣ�������
A.��ѧ��Ӧ�У���ԭ����ΪCu��H2
B.CuSO4��Һ������Ũ�ȵĴ�С˳��Ϊc��SO42-����c��Cu2+����c��OH-����c��H+��
C.��Һ��H2PO2-�ĵ��뷽��ʽΪH2PO2-H++HPO22-
D.NaH2PO3�����NaOH��Ӧ����Na2HPO3���ж�H3PO3Ϊ��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��ŵ������ѧ�������ڿ�������ӵ�ط�������Խ������λ��ѧ�ҡ�����ӵ�صĹ㷺Ӧ��Ҫ����﮵�ط����Խ�Լ��Դ����������������Ӷ��ε����������Ĥ��Ҫ����LiCoO2��A1�ȣ������÷��ϵ�һ�ֹ�������ͼ��ʾ��
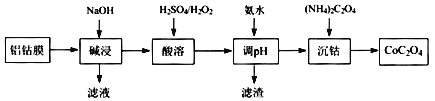
�ش��������⣺
(l) LiԪ����Ԫ�����ڱ��е�λ��Ϊ____________��LiCoO2��Co�Ļ��ϼ���____��
(2)�������ʱAl�ܽ�����ӷ���ʽΪ________��
(3)��������ʱ����H2O2��Ŀ����____������pH������������ҪΪ____��
(4)�������������ӷ���ʽΪ________��
(5)����100 mL l.0 mol/L (NH4)2C2O4��Һ����Ҫ�IJ������������������ձ��⣬����Ҫ_________��
(6)ȡCoC2O4����4.41 g�ڿ����м�����300�棬�õ��ܵ�������2.41 g����÷�Ӧ�Ļ�ѧ����ʽΪ _________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�Ҷ�һ̼��ѧ�����˹㷺������о���ȡ����һЩ��Ҫ�ɹ���
��1����֪��CO(g)+2H2(g) ![]() CH3OH(g) ��H1����90.0kJ/mol��
CH3OH(g) ��H1����90.0kJ/mol��
3CH3OH(g) ![]() CH3CH=CH2(g)+3H2O(g) ��H2����31.0kJ/mol
CH3CH=CH2(g)+3H2O(g) ��H2����31.0kJ/mol
CO��H2�ϳ�CH3CH=CH2���Ȼ�ѧ����ʽΪ________��
��2���״���CH3OH������Ϊ������������ȼ�ϣ���ҵ�Ͽ���CO�� H2�ڴ��������ºϳɼ״����������Ϊ2L�ĺ��ݾ����ܱ������У�����1molCO ��2mo1H2������Ӧ��CO(g)+2H2(g) ![]() CH3OH(g) ��H1��-90.0kJ/mol������Ӧ���е�5minʱ�ﵽƽ��״̬����ʱCH3OH�����ʵ���Ϊ0.6mol����
CH3OH(g) ��H1��-90.0kJ/mol������Ӧ���е�5minʱ�ﵽƽ��״̬����ʱCH3OH�����ʵ���Ϊ0.6mol����
��5 min�ڷ�Ӧ��ƽ��������(H2) = _____ mol/(L��min)��
�ڴﵽƽ��ʱ�ų�������Ϊ________ kJ
�۲���˵���÷�Ӧ�Ѵﵽƽ��״̬����____��ѡ����ĸ��ţ�
a��CO�����ʵ������ٸı� b���������¶ȱ��ֲ���
c��CH3OH����������������������� d�������ڵ��ܶȱ��ֲ���
��3��һ�ּ״�ȼ�ϵ����ͼ��ʹ�õĵ������Һ��2mol��L��1��KOH��Һ��
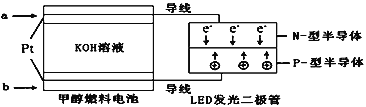
��д������(ͨ��)a����һ���ĵ缫��Ӧʽ_____��ÿ����9.6g�״�ת�Ƶĵ�����Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.01 mol��L1�Ĵ�����Һ�е���pH=7�Ĵ������Һ����ҺpH�����������Һ����仯������ʾ��ͼ����ͼ��ʾ�����з�����ȷ����

A��a�㣬pH = 2
B��b�㣬c(CH3COO-) > c(NH4+)
C��c�㣬pH���ܴ���7
D��ac�Σ���ҺpH������CH3COOH![]() H+ + CH3COO-�����ƶ��Ľ��
H+ + CH3COO-�����ƶ��Ľ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com