
【题目】由某精矿石(MCO3·ZCO3)可以制备单质M,制备过程中排放出的二氧化碳可以作为原料制备甲醇,取该矿石样品1.84g,高温灼烧至恒重,得到0.96g仅含两种金属氧化物的固体,其中m(M)︰m(Z)=3:5,请回答:
(1)该矿石的化学式为______________。
(2)①以该矿石灼烧后的固体产物为原料,真空高温条件下用单质硅还原,仅得到单质M和一种含氧酸盐(只含Z、Si和O元素,且Z和Si的物质的量之比为2︰1)。写出该反应的化学方程式____________________________________________。
②单质M还可以通过电解熔融MCl2得到,不能用电解MCl2溶液的方法制备M的理由是_______________________________________________________________。
(3)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1:CO2(g)+H2(g)CO(g)+H2O(g) △H1
反应2:CO(g)+2H2(g)CH3OH(g) △H2
反应3:CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H1
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图1所示。

则△H1_______△H2 (填“大于”、“小于”、“等于”),理由是______________________。
(4)在温度T1时,使体积比为3︰1的H2和CO2在体积恒定的密闭容器内进行反应。T1温度下甲醇浓度随时间变化曲线如图2所示;不改变其他条件,假定t时刻迅速降温到T2,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线。

【答案】 MgCO3CaCO3 2MgO+2CaO+Si![]() 2Mg+Ca2SiO4 电解MgCl2溶液时,阴极上H+比Mg2+容易得到电子,电极反应式为2H2O+2e-=H2↑+2OH-,所以得不到镁单质 小于;曲图l可知,随着温度升高,K1增大,则△H1>0,根据盖斯定律又得△H3=△H1+△H2,所以△H2<△H3;
2Mg+Ca2SiO4 电解MgCl2溶液时,阴极上H+比Mg2+容易得到电子,电极反应式为2H2O+2e-=H2↑+2OH-,所以得不到镁单质 小于;曲图l可知,随着温度升高,K1增大,则△H1>0,根据盖斯定律又得△H3=△H1+△H2,所以△H2<△H3; 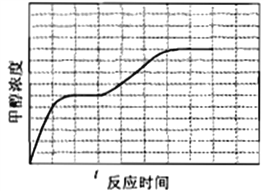
【解析】(1)由于M和Z的相对原子质量之比为3:5,故设M和Z的相对原子质量分别为3x,5x,
由于MCO3ZCO3中MCO3和ZCO3的物质的量之比为1:1,故得到的氧化物中MO和ZO的物质的量之比也为1:1,根据MCO3ZCO3的质量为1.84g,得到氧化物的质量为0.96g,可得: ![]() =
=![]() ,解得:x=8,M的相对原子质量为3x=24,故M为Mg,Z的相对原子质量为5x=40,故Z为Ca,则矿石的化学式为MgCO3CaCO3,故答案为:MgCO3CaCO3;
,解得:x=8,M的相对原子质量为3x=24,故M为Mg,Z的相对原子质量为5x=40,故Z为Ca,则矿石的化学式为MgCO3CaCO3,故答案为:MgCO3CaCO3;
(2)①由于灼烧后的产物为CaO和MgO的混合物,而真空高温条件下用单质硅还原,仅得到单质Mg和一种含氧酸盐,由于此含氧酸盐中只含Z、Si和O元素,且Z和Si的物质的量之比为2:1,故为Ca2SiO4,故此反应的化学方程式为:2MgO+2CaO+Si![]() 2Mg+Ca2SiO4,故答案为:2MgO+2CaO+Si
2Mg+Ca2SiO4,故答案为:2MgO+2CaO+Si![]() 2Mg+Ca2SiO4;
2Mg+Ca2SiO4;
②溶液中含有的阳离子的放电顺序为:H+>Mg2+,阴离子的放电顺序为:Cl->OH-,电解MgCl2溶液时,阴极上H+比Mg2+容易得到电子,电极反应式为2H2O+2e-=H2↑+2OH-,所以得不到镁单质,故答案为:电解MgCl2溶液时,阴极上H+比Mg2+容易得到电子,电极反应式为2H2O+2e-=H2↑+2OH-,所以得不到镁单质;
(3)由图l可知,随着温度升高,K1增大,则反应1:CO2(g)+H2(g)CO(g)+H2O(g)△H1>0,反应3由反应1+2所得,根据盖斯定律:△H3=△H1+△H2,所以△H2<△H3,故答案为:小于;曲图l可知,随着温度升高,K1增大,则△H1>0,根据盖斯定律又得△H3=△H1+△H2,所以△H2<△H3;
(4)由图l可知,随着温度升高,K3减小,则反应3CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H3<0,t时刻迅速降温到T2,降低温度平衡向正反应方向移动,CH3OH浓度增大,t时刻后甲醇浓度随时间变化至平衡的示意曲线为: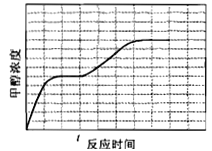 ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】纤维素被称为“第七营养素”,食物中的纤维素虽然不能被消化,但能刺激肠道蠕动和分泌消化液,有助于食物的消化和废物的排泄。在化学分类中,纤维素属于( )
A.蛋白质B.脂肪C.多糖D.氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X的分子式为C4H8O2,X在酸性条件下与水反应,生成分子内均含有2个碳原子的有机物Y和Z,Y在铜催化下被氧化为W,W能发生银镜反应。
(1)写出X和Z的结构简式X____________________,Z________________________。
(2)写出下列反应的化学方程式
X在酸性条件下与水反应________________________,反应类型为__________________。
Y与浓硫酸的混合物共热发生消去反应_____________________________________________。
W与新制Cu(OH)2反应的现象是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快。如图为反应速率v(ClO3-)随时间(t)的变化曲线。下列有关说法不正确的是( )

A. KClO3和KHSO3发生反应的氧化剂与还原剂的物质的量之比为1∶3
B. 反应开始阶段速率逐渐增大可能是c(H+)逐渐增高导致的
C. 反应后期速率逐渐减小的主要原因是c(ClO3-)、c(HSO3-))降低
D. 纵坐标为v(HSO3-)时的v-t曲线与原图曲线完全吻合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6.4g铜与100g98%H2SO4在烧瓶中加热发生反应.
(1)铜完全溶解后,计算生成的气体在标准状况下的体积是多少?
(2)将反应后烧瓶中的物质配成500mL溶液. ①在配制过程中用到的仪器有;配制溶液时,若稀释后立即转移并定容,则所配得的溶液浓度(填“偏大”“偏小”或“不变”).
②求所配得溶液中H2SO4的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起.气体X和液体Y不可能是( ) 
A.X是NH3 , Y是水
B.X是SO2 , Y是NaOH浓溶液
C.X是CO2 , Y是稀硫酸
D.X是HCl,Y是NaNO3稀溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在杠杆的两端分别挂着质量、体积都相同的铝球和铁球,此时杠杆平衡.然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,如图所示,则下列说法正确的是( ) 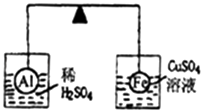
A.铝球一定是空心的
B.左边烧杯中的溶液质量减少了
C.去掉两烧杯杠杆仍平衡
D.右边铁球上出现红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com