
| A组 | B组 |
| Ⅰ.H—I键键能大于H—Cl键键能 Ⅱ.H—I键键能小于H—Cl键键能 Ⅲ.HI分子间作用力大于HCl分子间作用力 Ⅳ.HI分子间作用力小于HCl分子间作用力 | ①HI比HCl稳定 ②HI比HCl不稳定 ③HI沸点比HCl高 ④HI沸点比HCl低 |
科目:高中化学 来源:不详 题型:单选题
| A.I2微溶于水,易溶于CCl4;HCl易溶于水 |
| B.在水中的溶解度:C2H5OH>CH3CH2CH2CH2OH |
| C.不同的烃之间相互溶解 |
| D.I2易溶于KI溶液中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.BF3和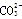 是等电子体,均为平面正三角形结构 是等电子体,均为平面正三角形结构 |
| B.B3N3H6和苯是等电子体,B3N3H6分子中不存在“肩并肩”式重叠的轨道 |
| C.NH3和PCl3是等电子体,均为三角锥形结构 |
D.CH4和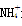 是等电子体,键角均为60° 是等电子体,键角均为60° |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.沉淀溶解后,生成深蓝色溶液是由于存在配合离子[Cu(NH3)4]2+ |
| C.向反应后的溶液中加入乙醇,将析出深蓝色的晶体CuSO4·5H2O |
| D.在[Cu(NH3)4]2+离子中,既存在离子键,又存在共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CO和N2 | B.O3和SO2 | C.N2H4和C2H4 | D.CO2和N2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.水溶液能导电 | B.由金属和非金属元素的原子组成 |
| C.熔融状态能导电 | D.可以溶于水并放出热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CS2为V形的极性分子 |
| B.电子云示意图中的每个小黑点都表示一个电子 |
| C.非极性键也可以存在于化合物中 |
| D.甲烷、氨和水都是由极性键结合而成的极性分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯化铝是共价化合物 |
| B.氯化铝的化学式应为Al2Cl6 |
C.氯化铝的结构式为: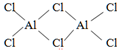 ,分子结构中有配位键 ,分子结构中有配位键 |
| D.在一定条件下,将AlCl3晶体加热至融化,熔融态的AlCl3可以导电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com