
【题目】山梨酸钾(CH3CH=CHCH=CHCOOK,简写为RCOOK)是常用的食品防腐剂,其水溶液显碱性。下列叙述正确的是( )
A.山梨酸和山梨酸钾都是强电解质
B.稀释山梨酸钾溶液时,n(OH-)、c(OH-)都减小
C.若山梨酸的电离常数为Ka,则RCOOK稀溶液中c(K+)=c(RCOO-)[1+ ]
]
D.山梨酸能发生加成反应,但不能发生取代反应
【答案】C
【解析】
A. 山梨酸钾是盐,属于强电解质,其水溶液显碱性,说明该盐是强碱弱酸盐,水解使溶液显碱性,因此山梨酸是一元弱酸,属于弱电解质,A错误;
B. 山梨酸钾是强碱弱酸盐,水解使溶液显碱性,稀释时,水解程度增大,水解产生的OH-物质的量增大,但稀释倍数大于水解增大的倍数,所以稀释后的溶液中n(OH-)增大,但c(OH-)减小,B错误;
C.根据物料守恒可得c(K+)=c(RCOO-)+c(RCOOH),山梨酸钾水解平衡常数Kh=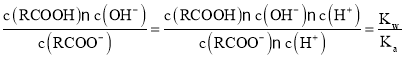 ,所以c(RCOOH)=
,所以c(RCOOH)=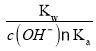 c(RCOO-),故c(K+)=c(RCOO-)+c(RCOOH)=c(RCOO-)[1+
c(RCOO-),故c(K+)=c(RCOO-)+c(RCOOH)=c(RCOO-)[1+ ],C正确;
],C正确;
D. 山梨酸分子中含有碳碳双键能发生加成反应,含有羧基能发生取代反应,D错误;
故合理选项是C。


 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4∶3,Z原子的核外电子数比X原子多4。下列说法正确的是( )
A.W、Y、Z的电负性大小顺序一定是Z>Y>W
B.Z的氢化物分子间存在氢键
C.Y、Z形成的化合物分子的中心原子可能采取sp3杂化
D.WY2分子中σ键与π键的数目之比一定是2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化剂是化工技术的核心,绝大多数的化工生产需采用催化工艺。
I.(1)催化剂的选择性指在能发生多种反应的反应系统中,同一催化剂促进不同反应的程度的比较,实质上是反应系统中目的反应与副反应之间反应速度竞争的表现。如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。在有催化剂作用下,CH3OH与O2反应主要生成____(选填“CO或CO2或HCHO”)。
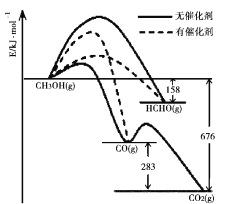
(2)2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家哈德·埃特尔,他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论。埃特尔研究的氮气和氢气分子在固体催化剂表面发生的部分变化过程如图所示:
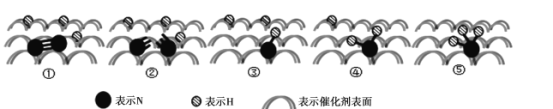
①下列说法不正确的是____。
A 升高温度可以提高一段时间内NH3的生产效率
B 图示中的②一③以及后面几个过程均是放热过程
C 此图示中存在H-H键断裂和N-N键断裂,以及N-H键的形成过程
②合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用Cu(NH3)2Ac(醋酸二氨合亚铜,Ac代表醋酸根)溶液来吸收原料气中的CO,其反应是: ![]()
生产中必须除去原料气中CO的原因是 ___;Cu(NH3)2Ac溶液吸收原料气中的CO的生产适宜条件应是___。
Ⅱ.氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一,存在较多蓝、绿藻类的酸性水体中存在如有图所示的氮循环,请回答相关问题。
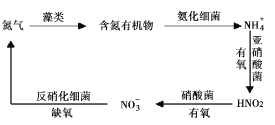
(3) NH4+硝化过程的方程式是2NH4++3O2 ![]() 2HNO3+2H2O+2H+,恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是____(填标号)。
2HNO3+2H2O+2H+,恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是____(填标号)。
A 溶液的pH不再改变
B NH4+的消耗速率和H+的生成速率相等
C 溶液中NH4+、NH3H2O、HNO3、NO2-的总物质的量保持不变
实验测得在其它条件一定时,NH4+硝化反应的速率随温度变化曲线如下图A所示,温度高于35℃时反应速率迅速下降的原因可能是 ___。
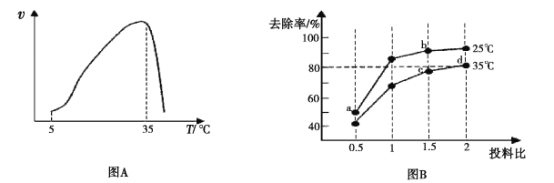
(4)亚硝酸盐含量过高对人和动植物都会造成直接或间接的危害,因此要对亚硝酸盐含量过高的废水进行处理。处理亚硝酸盐的方法之一是用次氯酸钠将亚硝酸盐氧化为硝酸盐,反应方程式是ClO-+ NO2-=NO3-+Cl-。在25℃和35℃下,分别向NO2-初始浓度为5×10-3 mol/L的溶液中按不同的投料比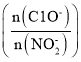 加人次氯酸钠固体(忽略溶液体积的变化),平衡时NO2-的去除率和温度、投料比的关系如上图B所示,a、b、c、d四点ClO-的转化率由小到大的顺序是____,35℃时该反应的平衡常数K=____(保留三位有效数字)。
加人次氯酸钠固体(忽略溶液体积的变化),平衡时NO2-的去除率和温度、投料比的关系如上图B所示,a、b、c、d四点ClO-的转化率由小到大的顺序是____,35℃时该反应的平衡常数K=____(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
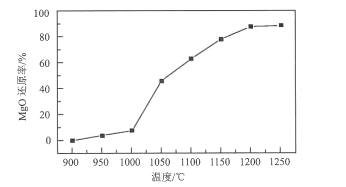
【题目】我国是世界产镁大国,金属镁的产量居世界前列。一种由白云石(主要成分为CaOMgO,含少量SiO2、A12O3、Fe2O3等杂质)冶炼金属镁的工艺流程如图:
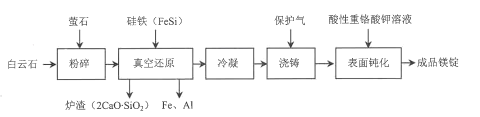
已知:萤石的主要成分是CaF2,用于降低真空还原反应的活化能。
回答下列问题:
(1)①粉碎的主要目的________。
②萤石在真空还原反应中的作用是________(填标号)。
A.氧化剂 B.还原剂 C.催化剂
(2)Mg2+、Ca2+、Fe3+、Fe2+、A13+五种离子的氧化性由强到弱的顺序为Fe3+>Fe2+>___(用离子符号表示)。
(3)结合流程以及如图温度对MgO还原率的影响关系,真空还原反应温度的最佳选择为___;高温真空还原时,CaO、MgO和FeSi反应生成单质镁的化学方程式为___。
(4)液态镁浇铸成镁锭时,通入的保护气不可选用N2或CO2,其原因是_______。
(5)镁锭冷却后,用酸性K2Cr2O7溶液进行表面钝化形成致密的氧化物保护膜,还原产物为Cr3+。该反应的离子方程式为________。
(6)为测定镁锭的纯度,称取a g除去氧化膜的成品镁锭样品溶于足量稀硫酸中,配成250 mL溶液。取25 mL该溶液,用0.1000 mol/L的EDTA标准溶液进行滴定(杂质不干扰滴定),三次滴定平均消耗EDTA标准溶液V mL(己知Mg2+与EDTA反应的化学计量数之比为1:1)。该样品的纯度为___%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生设计了如下三个实验方案,探究用化学方法检验淀粉的水解情况。
方案甲:![]() 结论:淀粉完全水解
结论:淀粉完全水解
方案乙:![]() 结论:淀粉完全没有水解
结论:淀粉完全没有水解
方案丙:![]() 结论:淀粉已经水解
结论:淀粉已经水解
试从实验操作、结论两个方面对上述三种方案进行评价,其中正确的是____,理由是______,有错误的是_____,理由是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
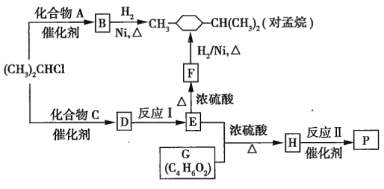
【题目】优良的有机溶剂对孟烷、耐热型特种高分子功能材料![]() 的合成路线如图所示:
的合成路线如图所示:
已知芳香化合物苯环上的氢原子可被卤代烷中的烷基取代,如:![]() (
(![]() 为烷基,
为烷基,![]() 为卤素原子)。
为卤素原子)。
(1)已知B为芳香烃。
①由B生成对孟烷的反应类型是__________________。
②![]() 与A反应生成B的化学方程式是_________________。
与A反应生成B的化学方程式是_________________。
③![]() 的同系物中相对分子质量最小的物质是_________________________。
的同系物中相对分子质量最小的物质是_________________________。
(2)已知![]() 的分子式为
的分子式为![]() 且含有一个酚羟基,且苯环上的另一个取代基与酚羟基处于间位;
且含有一个酚羟基,且苯环上的另一个取代基与酚羟基处于间位;![]() 不能使
不能使![]() 的
的![]() 溶液褪色。
溶液褪色。
①F中含有的官能团名称是_____________________。
②C的结构简式是________________。
③反应I的化学方程式是________________。
(3)G的核磁共振氢谱有3个峰,其峰面积之比为![]() ,且G与
,且G与![]() 溶液反应放出
溶液反应放出![]() 。写出反应Ⅱ的化学方程式:_________________________________。
。写出反应Ⅱ的化学方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某多肽的化学式为![]() ,完全水解后只得到以下三种氨基酸:
,完全水解后只得到以下三种氨基酸:![]() (甘氨酸)、
(甘氨酸)、![]() (赖氨酸)和
(赖氨酸)和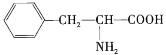 (苯丙氨酸)
(苯丙氨酸)
(1)该多肽为_______肽。
(2)![]() 该多肽完全水解后能生成__________
该多肽完全水解后能生成__________![]() 甘氨酸、_______
甘氨酸、_______![]() 苯丙氨酸、_______
苯丙氨酸、_______![]() 赖氨酸。
赖氨酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃与氢气发生加成反应后,所得产物为2,2,3-三甲基戊烷,则该烃的结构简式可能有(两个双键连接同一碳原子上时结构不稳定)( )
A.3种B.4种C.5种D.6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯的结构简式为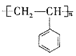 ,试回答下列问题:
,试回答下列问题:
(1)聚苯乙烯的分子式为__________,链节是____________,单体是_________________。
(2)实验测得聚苯乙烯的相对分子质量(平均值)为52000,则该高聚物的聚合度![]() 为________。
为________。
(3)一定条件下合成聚苯乙烯的化学方程式为______,该反应类型为_______反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com