
| A. | 加入少量MgCl2固体 | B. | 继续加水 | ||
| C. | 加入少量Na2CO3固体 | D. | 升高温度 |
分析 A.镁离子与氢氧根离子反应生成氢氧化镁沉淀,平衡右移,但氢氧根离子的浓度降低;
B.加水稀释,平衡右移,但c(Ca2+)减小,c(OH-)减小;
C.钙离子与碳酸根离子结合生成碳酸钙沉淀,平衡右移;
D.升高温度,平衡左移,c(Ca2+)、c(OH-)都减小.
解答 解:A.镁离子与氢氧根离子反应生成氢氧化镁沉淀,平衡右移,c(Ca2+)减小,氢氧根离子的浓度降低,故A错误;
B.加水稀释,平衡右移,但c(Ca2+)减小,c(OH-)减小,故B错误;
C.钙离子与碳酸根离子结合生成碳酸钙沉淀,平衡右移,c(Ca2+)减小,c(OH-)增大,故C正确;
D.氢氧化钙溶解度会随着温度升高而降低,升高温度,平衡左移,c(Ca2+)、c(OH-)都减小,故D错误,
故选C.
点评 本题考查溶解平衡,难度不大,注意利用平衡移动原理分析或借助溶度积常数理解.


科目:高中化学 来源: 题型:多选题
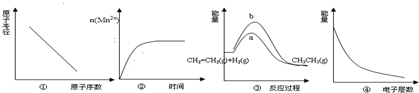
| A. | 图①表示第IA族元素原子半径的变化规律 | |
| B. | 图②表示10 mL 0.01 mol•L-1 KMnO4 酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,溶液中n(Mn2+) 随时间的变化 | |
| C. | 图③中a、b曲线分别表示反应:CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0在使用和未使用催化剂时,反应过程中的能量变化 | |
| D. | 图④表示核外电子能量与电子层数的关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | S区的元素一定是主族元素 | B. | d区元素一定是副族元素 | ||
| C. | p区的元素一定是主族元素 | D. | ds区元素一定是副族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价 | |
| B. | 只有非金属能形成含氧酸或含氧酸盐 | |
| C. | 除稀有气体外的非金属元素都能生成不同价态的含氧酸 | |
| D. | 非金属的最高价含氧酸不一定具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;1mol O22+中含有的π键数目为2NA.
;1mol O22+中含有的π键数目为2NA.| 代号 | 结构简式 | 水中溶解度/g(25℃) | 熔点/℃ | 沸点/℃ |
| X | 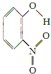 | 0.2 | 45 | 100 |
| Y | 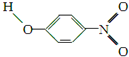 | 1.7 | 114 | 295 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 甲的分子数比乙的分子数多 | |
| B. | 甲的物质的量比乙的物质的量少 | |
| C. | 甲的密度比乙的密度小 | |
| D. | 甲的相对分子质量比乙的相对分子质量大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2的水溶液能导电,所以SO2是电解质 | |
| B. | BaSO4难溶于水,其水溶液的导电能力极弱,所以BaSO4是弱电解质 | |
| C. | 液溴不导电,所以液溴是非电解质 | |
| D. | HI熔融状态不能导电,但HI是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molH2中含有的氢原子数为2NA | |
| B. | 22.4L氧气所含的氧原子数为2NA | |
| C. | 常温常压下,28g氮气所含的分子数为2NA | |
| D. | 2g氢气所含的氢原子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com