
已知酸性条件下有反应:2Cu+ Cu2++Cu。氢气还原氧化铜实验由于反应温度不同,可能产生Cu或Cu2O,两者都是红色固体。某同学对某次氢气还原氧化铜的红色固体产物做了如下实验,实验操作和实验现象列表如下:
Cu2++Cu。氢气还原氧化铜实验由于反应温度不同,可能产生Cu或Cu2O,两者都是红色固体。某同学对某次氢气还原氧化铜的红色固体产物做了如下实验,实验操作和实验现象列表如下:
| 加入试剂 | 稀硫酸 | 浓硫酸 并加热 | 稀硝酸 | 浓硝酸 |
| 实验现象 | 红色固体 不反应 | 无色气体 | 无色气体 蓝色溶液 | 红棕色气体 蓝色溶液 |
由此推出本次氢气还原氧化铜实验的产物( )
A.是Cu
B.是Cu2O
C.一定有Cu,一定有Cu2O
D.一定有Cu2O,可能有Cu
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
A、两种气体的压强相等 B、O2比O3的质量小
C、两种气体的分子数目相等 D、两种气体的氧原子数目相等
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,下列各溶液中有关微粒物质的量浓度关系正确的是
A.0.1 mol·L-1Na2S溶液中:2c(Na+) =c(S2-)+c(HS-) +c(H2S)
B.pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合:
c(Na+)+ c(H+)= c(OH-)+c(CH3COO-)
C.0.1 mol·L-1盐酸与0.1 mol·L-1K2CO3溶液等体积混合:
c(K+) >c(Cl-)>c(HCO3-)>c(OH-)>c(H+)
D.0.1 mol·L-1NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:
c(Na+)>c(NH4+)>c(SO42-)>c(OH-) =c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下向1L pH=2的醋酸溶液中加入2L pH=2的盐酸,则混合溶液的pH为(假设混合后溶液体积不变,室温下醋酸的电离平衡常数为1.8×10-5)( )
A.2.3 B.1.7 C.2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
分析推理是化学学习的方法之一。下列实验推理中,正确的是 ( )
A.金属的冶炼方法与金属的活泼性有很大关系,所以铁、锌等金属一般用热还原法冶炼
B.钠比铜活泼,所以钠可以从硫酸铜溶液中置换出铜
C.工业上电解熔融氯化镁可制得金属镁,所以工业上电解熔融氯化铝可制得铝
D.将镁条和铝片用导线连接后插进稀NaOH溶液中,镁条上产生气泡,说明铝比镁活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
铜及其合金在生产和生活中都有广泛的应用。铜含量很高的铜合金称紫铜或红铜;以锌为主要添加元素的铜合金称黄铜;以镍为主要添加元素的铜合金称白铜;黄铜中含有少量镍称镍黄铜。
某学习小组拟对上述铜及其合金进行探究。
(1)铜的核外电子排布式: ,镍在周期表中位于 周期、
族。
(2)现有某种铜合金,经测定含有镍元素,对该铜合金类型作如下探究:
假设一:该铜合金是 。
假设二:该铜合金是 。
(3)为确定该铜合金的组成,你还需要进行的实验:
| 实验步骤 | 预期实验现象和结论 |
| ①用锉刀将铜合金挫成粉末,称取一定质量的铜合金粉末 | |
| ② | |
| ③ |
已知:镍和铁性质相似,锌和铝性质相似。
表中实验步骤可以不填满,也可以自行添加。
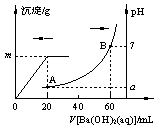
(4)取1.50 g该铜合金,与足量碱反应产生气体体积(已经折算成标准状况下的体积)的图像如图所示,该合金含锌质量分数 (小数点后保留一位数字)。

查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: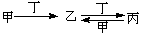 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
A. 若甲为焦炭,则丁可能是O2 B. 若甲为SO2,则丁可能是氨水
C. 若甲为Fe,则丁可能是盐酸 D. 若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的转化在给定条件下能实现的是
①Al2O3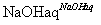 NaAlO2(aq)
NaAlO2(aq) Al(OH)3
Al(OH)3
②S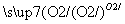 SO3
SO3 H2SO4
H2SO4
③饱和NaCl(aq) NaHCO3
NaHCO3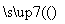 Na2CO3
Na2CO3
④Fe2O3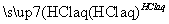 FeCl3(aq)
FeCl3(aq)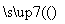 无水FeCl3
无水FeCl3
⑤MgCl2(aq) Mg(OH)2
Mg(OH)2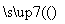 MgO
MgO
A.①③⑤ B.②③④ C.②④⑤ D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在25 ℃时,醋酸、次氯酸、碳酸和亚硫酸的电离平衡常数分别为
醋酸K=1.75×10-5
次氯酸K=2.95×10-8
碳酸K1=4.30×10-7 K2=5.61×10-11
亚硫酸K1=1.54×10-2 K2=1.02×10-7
(1)写出碳酸的第一级电离平衡常数表达式K1=______。
(2)在相同条件下,等浓度的CH3COONa、NaClO、Na2CO3和Na2SO3溶液中碱性最强的是________。等浓度的Na2CO3和NaHCO3的混合溶液中各离子浓度大小顺序为______________。
(3)若保持温度不变,在醋酸溶液中通入少量HCl,下列量会变小的是________(填字母序号,下同)。
a.c(CH3COO-) b.c(H+) c.醋酸的电离平衡常数
(4)下列离子方程式中错误的是________。
a.少量CO2通入次氯酸钠溶液中:CO2+H2O+ClO-===HCO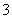 +HClO
+HClO
b.少量SO2通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO
c.过量CO2通入澄清石灰水中:CO2+OH-===HCO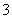
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com