
室温时,下列混合溶液的pH一定小于7的是( )
|
| A. | pH=3的盐酸和pH=11的氨水等体积混合 |
|
| B. | pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 |
|
| C. | pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 |
|
| D. | pH=3的硫酸和pH=11的氨水等体积混合 |
考点:
酸碱混合时的定性判断及有关ph的计算.
专题:
电离平衡与溶液的pH专题.
分析:
根据酸碱的强弱判断溶液中n(H+)与n(OH﹣)关系进行判断和计算.
解答:
解:A、pH=3的盐酸中c(H+)=1×10﹣3mol/L,pH=11的氨水中c(OH﹣)=1×10﹣3mol/L,由于氨水为弱碱,则氨水过量,在室温下等体积混合后,pH>7,故A错误.
B、PH=3的盐酸中c(H+)=1×10﹣3mol/L,pH=11的氢氧化钡溶液c(OH﹣)=1×10﹣3mol/L,酸碱都是强电解质,在室温下等体积混合后,pH=7,故B错误;
C、pH=3的醋酸c(H+)=1×10﹣3mol/L,pH=11的氢氧化钡溶液中c(OH﹣)=1×10﹣3mol/L,由于醋酸为弱酸,则醋酸过量,在室温下等体积混合后,pH<7,故C正确.
D、pH=3的硫酸中c(H+)=1×10﹣3mol/L,pH=11的氨水中c(OH﹣)=1×10﹣3mol/L,由于氨水为弱碱,则氨水过量,在室温下等体积混合后,pH>7,D错误.
故选C.
点评:
本题考查酸碱混合时的定性判断及有关pH的计算,题目难度不大,注意判断酸碱的强弱并以此判断反应的过量问题.


科目:高中化学 来源: 题型:
用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2g含有少量中性易溶杂质的样品,配成500mL待测溶液.称量时,样品可放在 (填编号字母)上称量
(A)小烧杯 (B)洁净纸片 (C)直接放在托盘上
(2)滴定时,用0.2000mol•L﹣1的盐酸来滴定待测溶液,不可选用 (填编号字母)作指示剂.
(A)甲基橙 (B)石蕊 (C)酚酞
(3)根据你所选择的指示剂,正确判断滴定终点的现象是: .
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是 mol•L﹣1,烧碱样品的纯度是 97.56% .
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 |
|
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
(5)下列实验操作会对滴定结果产生的后果.(填“偏高”、“偏低”或“无影响”)
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果 .
②若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是部分短周期元素化合价与原子序数的关系图(X、Y、Z、W、R代表元素符号)下列说法中,正确的是
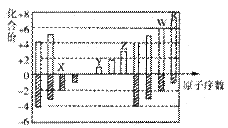
| A.原子半径比较: | B.气态氢化物的还原性比较:W>R |
| C.WX3和水反应形成的化合物是离子化合物 | D.含Z元素的盐溶液一定显示酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有一支50mL酸式滴定管中盛盐酸,液面恰好在amL刻度处,把管内液体全部放出,盛入量筒内,所得液体体积一定是( )
|
| A. | a mL | B. | (50﹣a)mL | C. | 大于(50﹣a)mL | D. | 大于a mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,水的电离可达到平衡:H2O⇌H++OH﹣△H>0,下列叙述正确的是( )
|
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH﹣)降低 |
|
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
|
| C. | 向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)降低 |
|
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为Va、Vb,则两者的关系正确的是( )
|
| A. | Va>10Vb | B. | Va=10Vb | C. | Vb<10Va | D. | Vb>10Va |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是恒温下某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( )
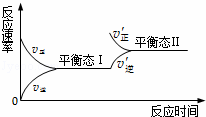
|
| A. | 反应达平衡时,正反应速率和逆反应速率相等 |
|
| B. | 该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ |
|
| C. | 该反应达到平衡态后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ |
|
| D. | 同一种反应物在平衡态Ⅰ和平衡Ⅱ时浓度不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将﹣CH3、﹣OH、﹣COOH、﹣CHO、﹣ 五种原子团两两结合,所得有机化合物水溶液呈酸性的共( )
五种原子团两两结合,所得有机化合物水溶液呈酸性的共( )
|
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
乙醇分子中各化学键如图所示对乙醇在各种反应中应断裂的键说明不正确的是( )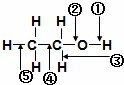
|
| A. | 和金属钠作用时,键①断裂 |
|
| B. | 和浓硫酸共热至170℃时,键②和⑤断裂 |
|
| C. | 和浓硫酸共热至140℃时,键②和③断裂 |
|
| D. | 在铜催化下和氧气反应时,键①和③断裂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com