
”¾ĢāÄæ”æŹµŃéŹŅÓŠŅŌĻĀ¼øÖÖĪļÖŹ£ŗ½šøÕŹÆ”¢ÉśĢś”¢Ńõ»ÆĀĮ”¢ĒāŃõ»Æ¼Ų”¢“×Ėį”¢¾Ę¾«£®Ēė°“ŅŖĒ󊓳öÓŠ¹ŲĪļÖŹµÄ»ÆѧŹ½£®
ŹōÓŚµ„ÖŹµÄŹĒ£»ŹōÓŚ¼īµÄŹĒ£»ŹōÓŚŃõ»ÆĪļµÄŹĒ£»ŹōÓŚĖįµÄŹĒ £®
”¾“š°ø”æC£»KOH£»Al2O3£»CH3COOH
”¾½āĪö”æ½ā£ŗ½šøÕŹÆÓŠĢ¼ŌŖĖŲ×é³É£¬ŹōÓŚµ„ÖŹ£¬ÉśĢśŹĒĢśŗĶĢ¼µÄŗĻ½š£¬ŹōÓŚ»ģŗĻĪļ£¬Ńõ»ÆĀĮĀś×ćŃõ»ÆĪļµÄøÅÄī£®ŹōÓŚŃõ»ÆĪļ£¬ĒāŃõ»Æ¼ŲµēĄė³öµÄŅõĄė×ÓČ«²æŹĒĒāŃõ»ÆøłĄė×Ó£¬ŹōÓŚ¼ī£¬“×ĖįµēĄėŹ±Éś³ÉµÄŃōĄė×ÓČ«²æŹĒĒāĄė×Ó£¬ŹōÓŚĖį£¬¾Ę¾«²»»įµēĄė£¬ŹōÓŚÓŠ»śĪļ£¬
ĖłŅŌ“š°øŹĒ£ŗC£¬KOH£¬Al2O3 £¬ CH3COOH£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ[2016ŗ£ÄĻ]ĻĀĮŠÓŠ¹ŲŹµŃé²Ł×÷µÄŠšŹö“ķĪóµÄŹĒ
A£®¹żĀĖ²Ł×÷ÖŠ£¬Ā©¶·µÄ¼ā¶ĖÓ¦½Ó“„ÉÕ±ÄŚ±Ś
B£®“ÓµĪĘæÖŠČ”ÓĆŹŌ¼ĮŹ±£¬µĪ¹ÜµÄ¼ā×ģæÉŅŌ½Ó“„ŹŌ¹ÜÄŚ±Ś
C£®µĪ¶Ø½Ó½üÖÕµćŹ±£¬µĪ¶Ø¹ÜµÄ¼ā×ģæÉŅŌ½Ó“„׶ŠĪĘæÄŚ±Ś
D£®ĻņČŻĮæĘæ×ŖŅĘŅŗĢåŹ±£¬µ¼Į÷ÓĆ²£Į§°ōæÉŅŌ½Ó“„ČŻĮæĘæÄŚ±Ś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠX”¢Y”¢ZČżÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬XµÄĘųĢ¬Ēā»ÆĪļ»ÆѧŹ½ĪŖH2X£¬“ĖĒā»ÆĪļµÄĻą¶Ō·Ö×ÓÖŹĮæÓėX×ī×īøß¼ŪŃõ»ÆĪļµÄĻą¶Ō·Ö×ÓÖŹĮæÖ®±ČĪŖ17£ŗ40£¬XŌ×ÓŗĖÄŚÖŹ×ÓŹżÓėÖŠ×ÓŹżĻąµČ£¬YÓėXæÉŅŌŠĪ³ÉĄė×Ó»ÆŗĻĪļY2X£¬YµÄŃōĄė×Óµē×Ó²ć½į¹¹ÓėNeĻąĶ¬£¬ZÓėXĶ¬ÖÜĘŚ£¬ĘäĘųĢ¬µ„ÖŹŹĒĖ«Ō×Ó·Ö×Ó£¬Į½Ō×Ó¹²ÓĆ1¶Ōµē×Ó£®ŹŌ»Ų“š£ŗ
£Ø1£©Š“³öø÷ŌŖĖŲĆū³Ę£ŗX______”¢Y______”¢Z______£®
£Ø2£©XĄė×ӵĽį¹¹¼ņŹ½Ķ¼ĪŖ_________£¬XÓėYŠĪ³ÉµÄĄė×Ó»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ______£¬ZÓėĒāŠĪ³ÉµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ ______£®
£Ø3£©Yµ„ÖŹŌŚæÕĘųÖŠČ¼ÉÕ²śĪļÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
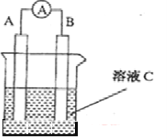
”¾ĢāÄæ”æ£Ø1£©ČēĶ¼ĖłŹ¾£¬ČōCĪŖÅØĻõĖį£¬µēĮ÷±ķÖøÕė·¢ÉśĘ«×Ŗ£¬Bµē¼«²ÄĮĻĪŖFe ,Aµē¼«²ÄĮĻĪŖCu£¬ŌņBµē¼«µÄµē¼«·“Ó¦Ź½ĪŖ______________£¬Aµē¼«µÄµē¼«·“Ó¦Ź½ĪŖ £»·“Ó¦½ųŠŠŅ»¶ĪŹ±¼äŗóČÜŅŗCµÄpH½« (Ģī”°Éżøß”±”°½µµĶ”±»ņ”°»ł±¾²»±ä”±)”£
£Ø2£©ĪŅ¹śŹ×““ŅŌĀĮæÕĘųŗ£Ė®µē³Ų×÷ĪŖÄÜŌ“µÄŠĀŠĶµÄŗ£Ė®±źÖ¾µĘ£¬ŅŌŗ£Ė®ĪŖµē½āÖŹČÜŅŗ£¬æææÕĘųÖŠµÄŃõĘųŹ¹ĀĮ²»¶ĻŃõ»Æ¶ų²śÉśµēĮ÷£¬Ö»ŅŖ°ŃµĘ·ÅČėŗ£Ė®Źż·ÖÖÓ£¬¾Ķ»į·¢³öŅ«ŃŪµÄ°×¹ā”£ŌņµēŌ“µÄøŗ¼«²ÄĮĻŹĒ________£¬øŗ¼«·“Ó¦ĪŖ___________£»Õż¼«·“Ó¦ĪŖ________________”£
£Ø3£©ČŪŃĪµē³Ų¾ßÓŠøߵķ¢µēŠ§ĀŹ£¬Ņņ¶ųŹÜµ½ÖŲŹÓ£¬ æÉÓĆLi2CO3ŗĶNa2CO3µÄČŪČŚŃĪ»ģŗĻĪļ×÷µē½āÖŹ£¬COĪŖøŗ¼«Č¼Ęų£¬æÕĘųÓėCO2µÄ»ģŗĻĘųĪŖÕż¼«ÖśČ¼Ęų£¬ÖʵĆŌŚ650 ”ęĻĀ¹¤×÷µÄČ¼ĮĻµē³Ų£¬Ķź³ÉÓŠ¹Ųµē³Ų·“Ó¦Ź½”£øŗ¼«·“Ó¦Ź½ĪŖ2CO£«2CO32-£4e£=4CO2£¬Õż¼«·“Ó¦Ź½ĪŖ________________£¬µē³Ų×Ü·“Ó¦Ź½ĪŖ___________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµČĪĀµČŃ¹¹ż³ĢŌŚµĶĪĀĻĀ²»ÄÜ×Ō·¢½ųŠŠ£¬¶ųŌŚøßĪĀĻĀæÉ×Ō·¢½ųŠŠµÄĢõ¼žŹĒ
A. ”÷H<0, ”÷S<0 B. ”÷H>0, ”÷S<0 C. ”÷H<0, ”÷S>0 D. ”÷H>0, ”÷S>0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijæÉÄę·“Ó¦:2A(g)![]() B(g)+D(g)ŌŚ3ÖÖ²»Ķ¬Ģõ¼žĻĀ½ųŠŠ£¬BŗĶDµÄĘšŹ¼ÅØ¶Č¾łĪŖ0£¬·“Ó¦ĪļAµÄÅضČĖę·“Ó¦Ź±¼äµÄ±ä»ÆĒéæöČēĻĀ±ķ£ŗ
B(g)+D(g)ŌŚ3ÖÖ²»Ķ¬Ģõ¼žĻĀ½ųŠŠ£¬BŗĶDµÄĘšŹ¼ÅØ¶Č¾łĪŖ0£¬·“Ó¦ĪļAµÄÅضČĖę·“Ó¦Ź±¼äµÄ±ä»ÆĒéæöČēĻĀ±ķ£ŗ
ŹµŃé ŠņŗÅ | Ź±¼ä/min ÅضČ/mol”¤L-1 ĪĀ¶Č/”ę | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 950 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)ŹµŃé1ÖŠ£¬ŌŚ1020 minÄŚ£¬ŅŌĪļÖŹA±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ______mol”¤L-1£¬50minŹ±£¬v£ØÕż£©_____£ØĢī”°<”± ”°>”± »ņ”°=”±£©v(Äę)”£
(2)020 minÄŚ£¬ŹµŃé2±ČŹµŃé1µÄ·“Ó¦ĖŁĀŹ________(Ģī”°æģ”±»ņ”°Āż”±)£¬ĘäŌŅņæÉÄÜŹĒ__________”£
(3)ŹµŃé3±ČŹµŃé1µÄ·“Ó¦ĖŁĀŹ____________(Ģī”°æģ”±»ņ”°Āż”±£©£¬ĘäŌŅņŹĒ_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĢžAŹĒÓŠ»ś»Æѧ¹¤ŅµµÄ»ł±¾ŌĮĻ£¬Ęä²śĮææÉŅŌÓĆĄ“ŗāĮæŅ»øö¹ś¼ŅµÄŹÆÓĶ»Æ¹¤·¢Õ¹Ė®Ę½£¬A»¹ŹĒŅ»ÖÖÖ²ĪļÉś³¤µ÷½Ś¼Į£¬AæÉ·¢ÉśČēĶ¼ĖłŹ¾µÄŅ»ĻµĮŠ»Æѧ·“Ó¦”£¾ŻĶ¼»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Š“³öA”¢C”¢DµÄ½į¹¹¼ņŹ½£ŗ
A__________£¬C____________£¬D____________”£
(2)Š“³ö¢Ł¢ŚĮ½²½·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬²¢×¢Ć÷·“Ó¦ĄąŠĶ£ŗ
¢Ł________________________(·“Ó¦ĄąŠĶ________)”£
¢Ś________________________(·“Ó¦ĄąŠĶ________)”£
(3)¢Ż·“Ó¦·¢ÉśŹ±¶ŌĀČĘųŅŖĒó£ŗ_______”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠČżøöŹż¾Ż£ŗ¢Ł7.2”Į10-4”¢¢Ś2.6”Į10-4”¢¢Ū4.9”Į10-10·Ö±šŹĒČżÖÖĖįµÄµēĄėĘ½ŗā³£Źż£¬ČōŅŃÖŖÕāŠ©ĖįæÉŅŌ·¢ÉśČēĻĀ·“Ó¦£ŗNaCN+HNO2=HCN+NaNO2£»NaCN+HF=HCN+NaF £» NaNO2+HF=HNO2+NaF £¬ ÓÉ“ĖæÉÅŠ¶ĻĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A. HNO2µÄµēĄėĘ½ŗā³£ŹżŹĒ¢Ū B. HNO2µÄµēĄėĘ½ŗā³£ŹżŹĒ¢Ł
C. HCNµÄµēĄėĘ½ŗā³£ŹżŹĒ¢Ś D. HFµÄµēĄėĘ½ŗā³£ŹżŹĒ¢Ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ2 molĒāĘųĶźČ«Č¼ÉÕÉś³ÉĖ®ÕōĘųŹ±·Å³öÄÜĮæ484 kJ£¬ĒŅŃõĘųÖŠ1 mol O===O¼üĶźČ«¶ĻĮŃŹ±ĪüŹÕÄÜĮæ496 kJ£¬Ė®ÕōĘųÖŠ1 mol H”ŖO¼üŠĪ³ÉŹ±·Å³öÄÜĮæ463 kJ£¬ŌņĒāĘųÖŠ1 mol H”ŖH¼ü¶ĻĮŃŹ±ĪüŹÕÄÜĮæĪŖ
A£®920 kJ B£®557 kJ C£®436 kJ D£®188 kJ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com