
【题目】已知X、Y、Z、W、M均为短周期主族元素。25℃时,各元素最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的pH和原子半径的关系如图所示。下列说法不正确的是( )

A. 从图中得出同浓度下W的最高价氧化物对应的水化物的pH比Z小,故非金属性:W>Z
B. X、Z的最简单气态氢化物在常温下可以反应生成离子化合物
C. X、Y、Z、W、M五种元素单质中Y常见单质熔点最高
D. 简单离子半径大小顺序:X>M
【答案】A
【解析】
X、Y、Z、W、M均为常见的短周期主族元素,由常温下,其最高价氧化物对应的水化物溶液(浓度均为 0.01mol/L)的pH,X的pH=2,为一元强酸,则为硝酸,X为N元素,Y的半径大于N,且酸性较硝酸弱,应为C元素;Z的原子半径大于C,Z的最高价含氧酸为一元强酸,则Z为Cl,W的原子半径大于Cl,且对应的酸的pH小于2,应为硫酸,W为S元素;M的原子半径最大,且0.01mol/LM的最高价氧化物对应的水化物溶液的pH为12,为一元强碱,则M为Na,据此分析解答。
根据上述分析,X为N元素,Y为C元素,Z为Cl元素,W为S元素,M为Na元素。
A.从图中得出同浓度下W的最高价氧化物对应的水化物的pH比Z小,Z的最高价含氧酸为一元强酸,则W的最高价含氧酸也是强酸,但是为二元强酸,不能据此说明非金属性强弱,实际上非金属性:W<Z,故A错误;
B.X为N元素,Z为Cl元素,X、Z的最简单气态氢化物分别为氨气和氯化氢,在常温下可以反应生成离子化合物氯化铵,故B正确;
C.C元素的单质常见的有石墨和金刚石,熔点均很高,而其他元素的单质是分子晶体或金属晶体,熔点均较低,故C正确;
D.X为N元素,M为Na元素,简单离子具有相同的电子层结构,核电荷数越大,离子半径越小,离子半径大小顺序:X>M,故D正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】镉镍可充电电池的充、放电反应按下式进行:Cd+2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2,由此判断,下列说法错误的是
Cd(OH)2+2Ni(OH)2,由此判断,下列说法错误的是
A. 放电时,NiO(OH)作正极
B. 放电时,Cd发生还原反应
C. 电解质溶液为碱性溶液
D. 充电时,阳极反应为Ni(OH)2+OH--e-== NiO(OH)+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,实验室制备联氨(N2H4)的化学方程式为:2NH3 +NaClO=N2H4 +NaCl+ H2O。下列说法正确的是
A. 0. lmolN2H4中所含质子数为1. 8NA
B. 0. 1mol·L-1的NaClO溶液中,ClO-的数量为0.1NA
C. 消耗4.48LNH3时,转移电子数为0.2NA
D. 1.6g N2H4中存在共价键总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)双氧水(H2O2)是一种绿色氧化剂,它的电子式为__。
(2)在常压下,乙醇的沸点(78.2℃)比甲醚的沸点(-23℃)高。主要原因是__。
(3)联氨(又称肼,分子式N2H4)是一种应用广泛的化工原料,可用作火箭燃料。联氨为二元弱碱,在水中的电离方程式与氨相似。
①肼的水溶液显碱性原因是__(请用肼在水中一级电离的方程式来表示)。
②联氨与硫酸形成的酸式盐的化学式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】达喜是常用的中和胃酸的药物,其有效成分是含结晶水的铝镁碱式盐。取该碱式盐6.02g,向其中逐滴加入4.00mol·L-1的盐酸,当加入盐酸42.5mL时开始产生CO2,加入盐酸至45.0mL时恰好反应完全。
(1)计算该碱式盐样品中碳酸根与氢氧根的物质的量之比:__。
(2)若达喜中镁、铝元素的物质的量之比为3:1,则氢元素的质量分数为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述不正确的是( )
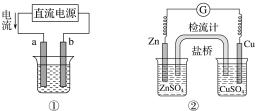
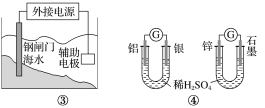
A.用图①装置实现铁上镀铜,a极为铜,电解质溶液可以是CuSO4溶液
B.图②装置盐桥中KCl的Cl-移向右烧杯
C.图③装置中钢闸门应与外接电源的负极相连获得保护
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某样品中氟元素的质量分数进行如下实验,利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(氢氟酸为低沸点酸,含量低,不考虑对玻璃仪器的腐蚀),用水蒸气蒸出,再通过滴定测量。实验装置如下图所示,加热装置省略。

(1) 仪器C名称是___________,长导管作用是_____________________________。
(2)实验时,首先打开活塞K,待水沸腾时,关闭活塞K,开始蒸馏。若蒸馏时因反应装置局部堵塞造成长导管水位急剧上升,应立即______________________。
(3)连接水蒸气发生装置和反应装置之间的玻璃管常裹以石棉绳,其作用是________。
(4)B中加入一定体积高氯酸和1.00g 氟化稀土矿样,D中盛有滴加酚酞的NaOH溶液。加热A、B,使A中产生的水蒸气进入B。
①下列物质不可代替高氯酸的是___________(填标号)
a. 硫酸 b.硝酸 c.磷酸 d.乙酸 e.盐酸
②D中主要反应的离子方程式为_________________________________。
(5)向馏出液中加入25.00mL0.1000mol·L-1La(NO3)3溶液,得到LaF3沉淀(La3+不发生其他反应),再用0.1000 mol· L-1EDTA标准溶液滴定剩余La3+(La3+与EDTA按1︰1发生络合反应),消耗EDTA标准溶液平均19.80mL,则氟化稀土样品中氟的质量分数为______(百分数保留小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知无水FeCl3能与氯苯反应:2FeCl3+C6H5Cl=2FeCl2+C6H4Cl2+HCl↑,实验室利用该装置制备无水FeCl2并检测FeCl3的转化率。已知:C6H5Cl、C6H4Cl2沸点依次为132℃、173℃。如图为制备FeCl2装置(加热和加持仪器省略)
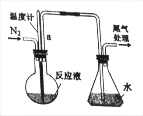
(1)蒸干并灼烧FeCl2溶液最终得到_____
(2)导管a的作用是_____;反应前通入N2的作用是_____;
(3)锥形瓶的作用是_____;该装置的不足之处为_____。
(4)反应结束后,回收过量氯苯的操作方法名称是_____。
若32.500g无水FeCl3与过量氯苯充分反应后将锥形瓶内溶液配制成250mL溶液,量取其中25.00mL溶液,滴加指示剂后,用0.4000mol/L的NaOH溶液滴定,重复三次,达到滴定终点平均消耗19.60mLNaOH溶液。
(5)滴定终点的现象是_____。
(6)FeCl3的转化率(转化量占总量的百分率)为_____%。
若制备反应后未通入足量N2,测定结果会_____(选项:偏高、偏低或不影响)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是四种常见有机物的比例模型示意图。下列说法不正确的是( )

A.甲与丙烷互为同系物
B.乙可与溴水发生加成反应,也可以被酸性高锰酸钾溶液氧化
C.丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键
D.丁(CH3CH2OH)可由乙烯与水发生取代反应制得
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com