
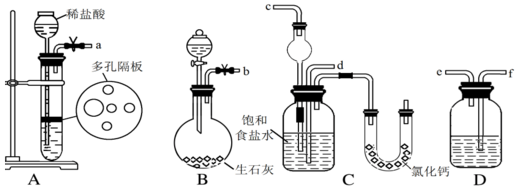
分析 (1)根据装置A制取CO2,装置B制取NH3,装置D除去二氧化碳中的HCl,二氧化碳与氨气通入C中应防止倒吸,据此分析连接仪器装置;
(2)检查A装置气密性的具体操作是关闭弹簧夹,通过长颈漏斗往试管中加水,使长颈漏斗中的水面高于试管中的睡眠,静置片刻,漏斗内水面不下降,说明A装置气密性良好;
(3)A装置是制备二氧化碳气体一般用碳酸钙和盐酸反应生成,B是制取氨气装置,二氧化碳气体中含有氯化氢气体,会影响碳酸氢钠的生成,D为装置除杂可以用饱和碳酸氢钠溶液;
(4)装有无水CaCl2的U形管的作用吸收多余的NH3;
(5)氯化铵晶体中常含有少量的氯化钠和碳酸氢钠,实验证明所得固体的成分大部分是氯化铵,是利用氯化铵的性质,受热生成氯化氢和氨气气体,在试管口处温度降低重新生成固体氯化铵分析判断.
解答 解:(1)足量的CO2与NaOH反应生成NaHCO3,装置A产生CO2,装置B产生NH3,装置D除去二氧化碳中的HCl,二氧化碳与氨气通入C中应防止倒吸,则b接c,故a接f、e接d,
故答案为:f;e;d;c;
(2)检查A装置气密性的具体操作是关闭弹簧夹,通过长颈漏斗往试管中加水,使长颈漏斗中的水面高于试管中的睡眠,静置片刻,漏斗内水面不下降,说明A装置气密性良好;
故答案为:关闭弹簧夹,通过长颈漏斗往试管中加水,使长颈漏斗中的水面高于试管中的睡眠,静置片刻,漏斗内水面不下降,说明A装置气密性良好;
(3)石A装置是制备二氧化碳气体的反应,所以固体为CaCO3用块状石灰石,生成的二氧化碳气体中含有氯化氢,若不除去碳酸氢钠难以形成,所以应用饱和碳酸氢钠溶液或饱和氯化钠溶液除去;
故答案为:块状石灰石;饱和NaHCO3溶液;
(4)装有无水CaCl2的U形管的作用吸收多余的NH3;
故答案为:吸收多余的NH3;
(5)步骤④中所得的氯化铵晶体中常含有少量的氯化钠和碳酸氢钠(约占5%~8%),设计简单的实验证明所得固体的成分大部分是氯化铵,是利用氯化铵的分解产物为气体,温度降低氨气和氯化氢气体会重新生成固体氯化氨,方法为:取少量样品于试管中,用酒精灯加热,看到试管上端有白烟生成(或试管口有白色晶体),最后剩余极少量的固体,从而证明所得固体的成分大部分是氯化铵;
故答案为:取少量样品于试管中,用酒精灯加热,看到试管上端有白烟生成(或试管口有白色晶体),最后剩余极少量的固体,从而证明所得固体的成分大部分是氯化铵.
点评 本题考查了实验制备碳酸氢钠的过程分析和装置作用判断,掌握候氏制碱的反应原理和反应特征是解题关键,熟练掌握工业制备流程和注意问题,能顺利解决问题,侧重于考查学生的实验探究能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物 | |
| B. | 常温下,浓度均为0.1mol/L①醋酸、②盐酸、③醋酸钠溶液,水电离程度的顺序为③>①>② | |
| C. | 常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为碱性 | |
| D. | 物质的浓度相同的①氯化铵溶液、②硫酸钠溶液、③碳酸氢钠溶液,pH的顺序为:③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B元素形成的一系列化合物中,其中A元素质量分数的最大值为25% | |
| B. | 四种元素中电负性最大的是B | |
| C. | C所形成的气态氢化物,在其同主族元素的气态氢化物中沸点最低 | |
| D. | 四种元素中第一电离能最小的是D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
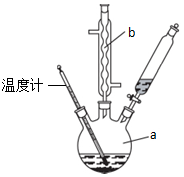 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一,
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一,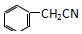 +2H2O+H2SO4$\stackrel{100-130℃}{→}$+NH4HSO4
+2H2O+H2SO4$\stackrel{100-130℃}{→}$+NH4HSO4 ,混合溶剂中乙醇的作用是增大苯乙酸的溶解度,便于充分反应.
,混合溶剂中乙醇的作用是增大苯乙酸的溶解度,便于充分反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 准确量取20.00mL高锰酸钾溶液,可选用25mL碱式滴定管 | |
| B. | 将水加热,Kw增大,pH不变 | |
| C. | 用惰性电极电解1L浓度均为2mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 mol 电子转移时,阴极析出6.4g金属 | |
| D. | NaAlO2的水溶液经加热浓缩、蒸干灼烧后能得到NaAlO2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发时将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 | |
| B. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| C. | 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 | |
| D. | 向某溶液中加入NaOH溶液得白色沉淀,又观察到沉淀颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com