
 如图甲、乙是电化学实验装置.请回答下列问题:
如图甲、乙是电化学实验装置.请回答下列问题: 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.0mol/L Na2CO3溶液:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| B. | 1.0mol/L Na2CO3溶液:c(H2CO3)+c(HCO3-)+c(CO32-)+C(Na+)=3.0mol/L | |
| C. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 B
B C
C
 的邻位异构体分子内脱水的反应方程式
的邻位异构体分子内脱水的反应方程式 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O.
+H2O.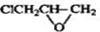 ,写出由D生成M的化学反应方程式
,写出由D生成M的化学反应方程式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO-3+Ba2++2OH-═BaCO3↓+2H2O+CO32- | |
| B. | Fe(NO3)3溶液中加入过量的HI溶液;2Fe3++2I-═2Fe2++I2 | |
| C. | Na2S203溶液中加入稀硫酸:S2O32-+2H+═SO2+S↓+H2O | |
| D. | 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+═Cl2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
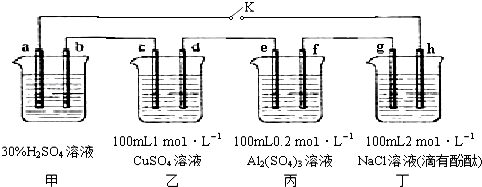
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
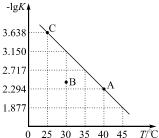 将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )
将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )| A. | 该反应的△H>0 | |
| B. | 30℃时,B点对应状态的v(正)<v(逆) | |
| C. | A点对应状态的平衡常数K(A)=10-2.294 | |
| D. | NH3的体积分数不变时,该反应一定达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H | B. | F | C. | Na | D. | Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
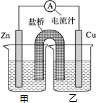 (1)已知下热化学方程式:
(1)已知下热化学方程式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com