
【题目】不能够区分碳酸钠和碳酸氢钠固体的方法是( )
A. 加热 B. 与等体积等浓度盐酸反应的剧烈程度
C. 与氯化钙溶液反应的现象 D. 与澄清石灰水的反应现象
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】W是由A、B两种元素组成的AB2型化合物.
(1)若W是最常见的温室气体则其结构式为;
(2)若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛.该反应的化学方程式为 .
(3)若W是离子化合物,其阴、阳离子均含18个电子,
①当阴、阳离子个数比为2:1时W的电子式为;
②当阴、阳离子个数比为1:1时阴离子的电子式为
(4)若A、B是同主族元素,W溶于水生成一种二元弱酸.
①如A、B为相邻周期时B在元素周期表中的位置为 . W的水溶液被双氧水氧化的化学方程式为 .
②如果A元素的周期序数是B元素的两倍,A的最高价氧化物对应水化物的分子式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液.现做如下实验:
①取440mL甲溶液与120mL乙溶液反应,产生1.56g沉淀.
②取120mL甲溶液与440mL乙溶液反应,产生1.56g沉淀.
③取120mL甲溶液与400mL乙溶液反应,产生3.12g沉淀.
通过必要的计算和推理判定:甲溶液为________溶液,理由是:________
甲溶液的物质的量浓度是多少?
(1)通过必要的计算和推理判定:甲溶液为 溶液,理由是:
(2)甲溶液的物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是
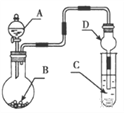
A. 若A为H2O2,B为MnO2,C中盛有Na2S溶液, C中溶液变浑浊
B. 若A为浓盐酸,B为MnO2,C中盛有KI淀粉溶液,C中溶液变蓝色
C. 若A为浓氨水,B为生石灰,C中盛有AlCl 3溶液, C中先产生白色沉淀后沉淀又溶解
D. 若A为浓H2SO4 ,B为CaCO3,C中盛有Na2SiO3 溶液,C中溶液出现白色沉淀,证明非金属性S>C>Si
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下化学反应不属于氧化还原反应的是
A. 2Na+2H2O=2NaOH+H2 ↑ B. N2H4+O2=N2+2H2O
C. FeO+2HCl=FeCl2+H2O D. NO + NO2 + Na2CO3=2NaNO2 + CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解饱和食盐水所得溶液经多次循环使用后,ClO-、ClO3-含量会增加。
已知:Ⅰ.NaHCO3固体50℃开始分解,在溶液中分解温度更低。
Ⅱ.碱性条件下,ClO-有强氧化性,ClO3-性质稳定。
Ⅲ.酸性条件下,ClO3-被Fe2+还原为Cl-,MnO4-被Fe2+还原为Mn2+。
(1)氯酸盐产生的原因可表示为3ClO-![]() 2Cl-+ClO3-,该反应的平衡常数表达式为 。
2Cl-+ClO3-,该反应的平衡常数表达式为 。
(2)测定电解盐水中ClO3-含量的实验如下:
步骤1:量取盐水样品V mL,调节pH至9~10,再稀释至500 mL。
步骤2:取10.00 mL稀释后的试液,滴加5%的双氧水,至不再产生气泡。
步骤3:加入饱和NaHCO3溶液20 mL,煮沸。
步骤4:冷却,加足量稀硫酸酸化。
步骤5:加入a mol·L-1FeSO4溶液V1 mL(过量),以如图所示装置煮沸。

步骤6:冷却,用c mol·L-1KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液V2mL。
①稀释时用到的玻璃仪器有烧杯、胶头滴管、 。
②步骤2用双氧水除去盐水中残留ClO-的离子方程式为 ,还原剂不用Na2SO3的原因为 。
③与步骤5中通N2目的相同的实验是 (填写步骤号)。
④该盐水试样中ClO3-的浓度为 mol·L-1(用含字母的代数式表示)。
⑤为提高实验结果的精确度,还需补充的实验是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在第3周期中,置换酸中氢的能力最强的元素的元素符号为 , 化学性质最稳定的元素符号是 , 最高价氧化物的水化物的酸性最强的化合物的化学式是 , 最高价氧化物的水化物的碱性最强的化合物的化学式是 , 显两性的氢氧化物的化学式是 , 该两性氢氧化物与盐酸、氢氧化钠溶液分别反应的离子方程式为、 , 原子半径最大的金属元素的名称是 , 离子半径最小的离子结构示意图是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com