
【题目】固体化合物CaFe(CO3)2在空气中加热反应生成CO2、Fe2O3和CaO.回答下列问题:
(1)CO2的电子式为_____。
(2)上述反应产物中的CaO加入燃煤中,其作用是_____。
A.降低温室效应B.减少SO2的排放C.避免光化学烟雾D.保护臭氧层
(3)设计实验证明上述固体产物中含有三价铁:取少量固体于试管中,_____。
(4)CaFe(CO3)2在空气中加热反应的化学方程式为_____。
【答案】![]() B 加盐酸溶解,再滴入少量KSCN溶液后变红色,证明含三价铁离子 4CaFe(CO3)2+O2
B 加盐酸溶解,再滴入少量KSCN溶液后变红色,证明含三价铁离子 4CaFe(CO3)2+O2![]() 8CO2+2Fe2O3+4CaO
8CO2+2Fe2O3+4CaO
【解析】
(1)二氧化碳为共价化合物,C、O之间存在两对共用电子对,由此书写电子式;
(2)煤炭含硫元素,燃烧生成二氧化硫污染空气,加入氧化钙可以除去硫元素,可减少SO2的排放;
(3)三价铁可与KSCN溶液结合生成红色物质,据此可检验三价铁;
(4)CaFe(CO3)2在空气中加热和氧气反应生成CO2、Fe2O3和CaO,据此书写方程式。
(1)二氧化碳为共价化合物,C、O之间存在两对共用电子对,因此二氧化碳的电子式为![]() ;
;
(2)煤炭含硫元素,燃烧生成二氧化硫污染空气,加入氧化钙可以除去硫元素,可减少SO2的排放;
A.温室效应是二氧化碳形成,A项错误;
B.加入氧化钙可以除去硫元素,生成硫酸钙,工业上为钙基固硫,减少SO2的排放,B项正确;
C.光化学烟雾形成是氮氧化物,氧化钙不能除去某些氮氧化物,不能避免光化学烟雾的形成,C项错误;
D.氧化钙不能保护臭氧层,D项错误;
答案选B;
(3)实验证明上述固体产物中含有三价铁:取少量固体于试管中,加盐酸溶解,再滴入少量KSCN溶液后变红色,证明含三价铁离子;
(4)CaFe(CO3)2在空气中加热和氧气反应生成CO2、Fe2O3和CaO,反应的化学方程式为:4CaFe(CO3)2+O2![]() 8CO2+2Fe2O3+4CaO。
8CO2+2Fe2O3+4CaO。


科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
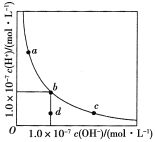
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,通入HCl可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《我不是药神》中的“格列宁”是一种抗癌药。同样是抗癌药物"6-Azulenol”的结构简式如图所示,下列有关叙述错误的是 ( )

A.分子式为C13H18O3
B.能发生加成、氧化、酯化反应
C.能使溴水、酸性高锰酸钾溶液褪色
D.1mol该物质与足量的Na反应可产生11.2LH2(已换算成标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将![]() 气体和2molB气体在2L的密闭容器中混合并在一定条件下发生如下反应:
气体和2molB气体在2L的密闭容器中混合并在一定条件下发生如下反应:![]() ,4s后反应达到平衡状态,此时测得C的浓度为
,4s后反应达到平衡状态,此时测得C的浓度为![]() ,下列说法中正确的是
,下列说法中正确的是
A.反应过程中,当A、B、C的物质的量浓度之比为2:1:2时,反应即达到平衡状态
B.4s内用物质B表示的反应速率为![]()
C.达平衡后若增大压强,A的转化率降低,平衡常数增大
D.达平衡后若升高温度,C的浓度将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容条件下,可逆反应:![]() ,在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是( )(Qc表示浓度熵)
,在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是( )(Qc表示浓度熵)
容器 | 体积 | 起始物质 | 平衡时C的物质的量 | 平衡时B的体积分数 | 平衡常数 |
甲 | 1L |
| 1mol |
|
|
乙 | 1L |
|
|
|
|
丙 | 2L |
|
|
|
|
A.在建立平衡的过程中,甲的Qc逐渐减小,乙和丙的Qc逐渐增大
B.![]()
C.升高甲的温度,可使![]()
D.![]() ,
,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片(锌片和铜片不接触),可观察到铜片上________(填“有”或“没有”)气泡产生。再用导线把锌片和铜片连接起来(见图A),组成一个原电池,负极为________,正极的电极反应式为________________________。
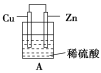

(2)如果烧杯中最初装入的是2 mol/L 500 mL的稀硫酸溶液,构成铜锌原电池(见图B,假设产生的气体没有损失),当在标准状况下收集到11.2 L的氢气时,则此时烧杯内溶液中硫酸的物质的量浓度为(溶液体积变化忽略不计)____________________。
(3)生活中利用原电池原理生产了各种各样的电池,废电池必须进行集中处理的问题已被提到议事日程,其主要原因是________________。
A.回收利用电池外壳的金属
B.防止电池中汞、镉和铅等重金属离子对土壤、水源的污染
C.防止电池中渗漏的电解液腐蚀其他物品
D.回收其中石墨电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温、恒容密闭容器中发生反应:Ni(s)+4CO(g)![]() Ni(CO)4(g),△H<0。利用该反应可以将粗镍转化为纯度达99.9%的高纯镍。对该反应的说法正确的是
Ni(CO)4(g),△H<0。利用该反应可以将粗镍转化为纯度达99.9%的高纯镍。对该反应的说法正确的是
A. 增加Ni的量可提高CO的转化率,Ni的转化率降低
B. 缩小容器容积,平衡右移,△H减小
C. 反应达到平衡后,充入CO再次达到平衡时,CO的体积分数降低
D. 当4v[Ni(CO)4]=v(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把蘸有浓盐酸的玻璃棒靠近装有氨水的试剂瓶口,为了使现象明显,可先往瓶中加入一种物质,该物质可以选用下列物质中的![]()
①浓硫酸 ②固体烧碱 ③固体碳酸钙 ④生石灰 ⑤固体![]() ⑥固体食盐
⑥固体食盐
A.①②B.②③④C.②④⑤D.①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸![]() 是一种具有强还原性的一元弱酸,工业上常利用
是一种具有强还原性的一元弱酸,工业上常利用![]() 和
和![]() 溶液反应进行化学镀银,已知该反应中氧化剂与还原剂的物质的量之比为4:1,则下列说法中正确的是
溶液反应进行化学镀银,已知该反应中氧化剂与还原剂的物质的量之比为4:1,则下列说法中正确的是![]()
A.![]() 中磷元素的化合价为
中磷元素的化合价为![]()
B.![]() 的电离方程式为
的电离方程式为![]()
C.![]() 被
被![]() 氧化成了
氧化成了![]()
D.![]() 、
、![]() 、
、![]() 均为酸式盐
均为酸式盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com