
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:推断题
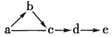 其中:a是单质,b是气体,c、d是氧化物,e是最高价氧化物对应的水化物.
其中:a是单质,b是气体,c、d是氧化物,e是最高价氧化物对应的水化物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
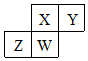 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 元素X、Y、Z、W的最高化合价分别与其主族序数相等 | |
| C. | 最简单气态氢化物的热稳定性:X>Z>W | |
| D. | 最高价氧化物对应水化物的酸性:X>Z>W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2 | B. | CH2=CHCH=CH2 | C. | CH4 | D. | CH≡C-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤 | B. | 蒸发 | C. | 结晶 | D. | 萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2溶液:K+、Na+、SO42-、AlO2- | |
| B. | 使紫色石蕊试液变红的溶液:Na+、Fe2+、NO3-、SO42- | |
| C. | 向存在大量Na+、Cl-的溶液中通入足量的NH3后:NH4+、Fe3+、SO42- | |
| D. | 在强酸性溶液中:K+、Fe2+、SO42-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
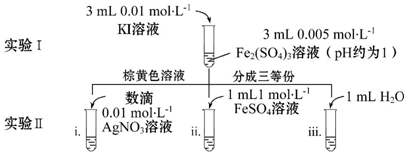
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定管装滴定液时不应先用滴定液润洗 | |
| B. | 锥形瓶用作反应容器时一定不能加热 | |
| C. | 蒸馏时温度计水银球可以高于蒸馏瓶支管口 | |
| D. | 振荡分液漏斗时应关闭其玻璃塞和活塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
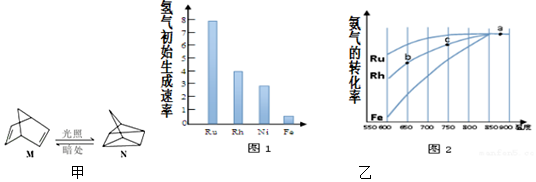
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com