
| A�� | ����AgBr��AgI���������Һ��c��Ag+����c��Br-��=c��I-�� | |
| B�� | 25��ʱ��0.1mol•L-1������ҺPH=a��0.01mol•L-1������ҺPH=b����b=a+1 | |
| C�� | 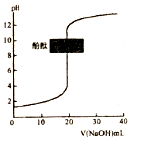 �����£�ͼ��ʾ�Է�̪��ָʾ������0.1mol•L-1NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ�ζ����յ�ʱ����Һһ�������� | |
| D�� | ��0.1mol•L-1�İ�ˮ�м�������粒��壬����Һ��c��OH-��/c��NH3•H2O����С |
���� A��AgBr��AgI�ܶȻ���ͬ��
B������Ϊ���ᣬŨ�Ȳ�ͬ�������̶Ȳ�ͬ��
C���ζ����յ�ʱ��pH����8-10֮�䣻
D����0.1mol•L-1�İ�ˮ�м�������粒��壬����һˮ�ϰ��ĵ��룮
��� �⣺A��AgBr��AgI�ܶȻ���ͬ��AgI�ܶȻ���С��ӦΪc��Br-����c��I-������A����
B������Ϊ���ᣬŨ��Խ�࣬����̶�ԽС��25��ʱ��0.1mol•L-1������ҺPH=a��0.01mol•L-1������ҺPH=b����b��a+1����B����
C���ζ����յ�ʱ��pH����8-10֮�䣬���Թ�������C����
D����0.1mol•L-1�İ�ˮ�м�������粒��壬����һˮ�ϰ��ĵ��룬��c��NH3•H2O������c��OH-����С������Һ��c��OH-��/c��NH3•H2O����С����D��ȷ��
��ѡD��
���� ���⿼���Ϊ�ۺϣ��漰���ܵ���ʵ��ܽ�ƽ�⣬������ʵĵ����Լ������ˮ���֪ʶ��Ϊ��Ƶ���㣬���ؿ���ѧ���ķ��������ͼ���������ע�����������ʵĵ����ص㣬�״���ΪB���Ѷ��еȣ�


 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
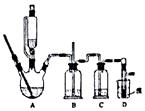 ʵ�����Ʊ�1��2-������ķ�Ӧԭ�����£�
ʵ�����Ʊ�1��2-������ķ�Ӧԭ�����£�| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶȣ�g/cm3�� | 0.79 | 2.2 | 0.71 |
| �е㣨�棩 | 78.5 | 132 | 34.6 |
| �۵㣨�棩 | -130 | 9 | -116 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
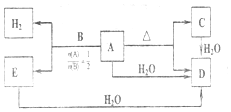
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��C��D��Ӧ���ɵĻ�����ĵ���ʽ��
��C��D��Ӧ���ɵĻ�����ĵ���ʽ�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£���1LpH=1�Ĵ�����Һ�м�ˮ��������Һ��H+��Ŀ����0.1NA | |
| B�� | 60g�����������Ҵ�����������Ӧ����ַ�Ӧ����ѵ�C-O����ĿΪNA | |
| C�� | ��ˮ�Ҵ������������Ʒ�Ӧ����5.6LH2�����Ҵ������й��ۼ�����Ϊ4NA | |
| D�� | ��֪C2H4��g��+H2��g���TC2H6��g����H=-137.0kJ/mol����ϩ��H2�ӳ�ʱ�ų�137.0kJ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ�� | ���� | ���� |
| A | ��KI��Һ�м���CCl4������ | Һ��ֲ㣬�²���Ϻ�ɫ | ��������CCl4��������ˮ |
| B | ������ǯ��סһС����ɰֽ��ϸ��ĥ���������ھƾ����ϼ��� | �ۻ����Һ̬���������� | ���������۵�ϵ� |
| C | ���з�̪��Na2CO3��Һ�м���������BaCl2���� | ��Һ��ɫ��dz | ֤��Na2CO3��Һ�д���ˮ��ƽ�� |
| D | ���������������е��������ữ��Ba��ClO��2��Һ | ������ɫ���� | �������������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȼ�������ȼ������SO3 | |
| B�� | �й��Ŵ�����������Һ���������ͭ��������ͭ�� | |
| C�� | ���ð�˾ƥ�ֳ���ˮ���ᷴӦʱ����NaOH��Һ�ⶾ | |
| D�� | ʹ�ú�������Ũ�Ƚϴ�ĵ���ˮϴ�·�������ȥ��������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȼ���е����ơ���Ԫ�ؾ���������̬��ʽ���� | |
| B�� | ����Ӧ��Ĺ�����������ˮ�����ã�ͨ��CO2�������� | |
| C�� | ���İ뾶��r��K+����r��Na+����r��O2-�� | |
| D�� | ����Ӧ��ת��6.02��1022���ӣ�������NaN3������Ϊ6.5g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ݻ�Ϊ2L���ܱ������У�Ͷ��2molA��3molB������Ӧ��A��s��+2B��g��?2C��g����B�����ʵ����ı仯��ͼ��ʾ����֪��2��t1ʱ�ε�����Ӧ���ʱ�t2��t3ʱ�ε�����Ӧ���ʿ죮
���ݻ�Ϊ2L���ܱ������У�Ͷ��2molA��3molB������Ӧ��A��s��+2B��g��?2C��g����B�����ʵ����ı仯��ͼ��ʾ����֪��2��t1ʱ�ε�����Ӧ���ʱ�t2��t3ʱ�ε�����Ӧ���ʿ죮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com