
甲、乙两种金属性质比较:①甲的单质熔、沸点比乙的低;②常温下,甲能与水反应放出氢气而乙不能;③最高价氧化物对应的水化物碱性比较,乙比甲的强;④甲、乙作电极,稀硫酸为电解质溶液组成原电池,乙电极表面产生气泡。上述项目中能够说明甲比乙的金属性强的是( )
A.①② B. ②④ C. ②③ D. ①③
科目:高中化学 来源:2014高考名师推荐化学--预测10 题型:填空题
一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。工业上依此用CO生产燃料甲醇。
CH3OH(g)。工业上依此用CO生产燃料甲醇。
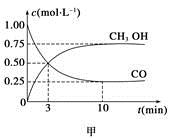

(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用H2浓度变化表示平均反应速率v(CO)=__________________。
(2)乙图表示该反应进行过程中能量的变化。曲线b下的反应条件为 。该反应的焓变是________(填“ΔH<0”或“ΔH>0”),写出反应的热化学方程式 ;选择适宜的催化剂______(填“能”或“不能”)改变该反应的反应热。
(3)该反应平衡常数K的表达式为______________________,温度升高,平衡常数K________(填“增大”、“不变”或“减小”)。
(4)恒容条件下,下列措施中能使 增大的有____________。
增大的有____________。
a.降低温度 b.充入He气
c.再充入1molCO和2molH2 d.使用催化剂
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测 题型:选择题
下列说法不正确的是
A.2013年0点钟声敲响后的几个小时,北京的污染指数从轻度污染上升为重度污染,主要污染为PM2.5污染,看来烟花爆竹的燃放,可加重PM2.5污染
B.催化剂之所以能加快反应速率,是因为催化剂能降低反应的活化能
C.氨气的水溶液氨水可以导电,因此氨气是电解质
D.大量燃烧含硫燃料是形成酸雨的主要原因
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--线索综合2 题型:简答题
CuCl2溶液中的铜主要以Cu(H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu(H2O)42+(蓝色)+4Cl- CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:

(1)甲电极的电极反应式为_________________。
(2)丙中溶液变蓝是乙电极产物与KI反应导致的,该反应的化学方程式为___。
(3)随电解的不断进行,U型管中溶液的颜色变化为__________;
A.由黄色变为浅蓝色 B.由蓝色变为浅黄色
溶液颜色变化的原因是_________________。
(4)当电解到一定程度,甲电极附近出现蓝色Cu(OH)2絮状物。经测甲电极附近溶液的pH=a,此时甲电极附近溶液中c(Cu2+)=______ mol·L-1。(已知:Cu(OH)2的Ksp=2.2×10-20)
(5)电解较长时间后,丙中溶液的蓝色又会褪去,这是因为乙电极产物进一步将I2氧化为IO3-,该反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源:2014福建安溪一中、养正中学、惠安一中高一下学期期末化学试卷(解析版) 题型:选择题
(15分) 现有A、B、C、D、E、F、G七种短周期元素,原子序数依次增大。已知A与E、D与F分别同主族, E、F、G同周期;A、C的最外层电子数之和与D的最外层电子数相等,A与D形成的化合物常温下为液态,A分别与F、G形成的气体分子电子总数相等、B有多种同素异形体,其中一种是原子晶体,是自然界中最硬的物质,可做首饰品或做切削工具。
请回答下列问题:
(1)元素C在周期表中的位置是_______________
元素E的原子结构示意图为
(2)C的气态氢化物的水化物与其最高价氧化物的水化物可发生反应,离子方程式为:
(3)在一定条件下,A、D的单质和A、D、E形成的离子化合物的水溶液可构成电池,该电池负极的电极反应式为 , 该电池在放电过程中,电解质溶液的pH将________(填“增大”、“减小”或“不变”)。
(4)化合物C2A4(g) 是一种高效清洁的火箭燃料,0.25 mol C2A4完全燃烧的生成物是一种气态单质和一种气态化合物,它们对环境无污染,同时放出热量133.5 kJ的热量。则该反应的热化学方程式为(用具体物质化学式表示) 。
查看答案和解析>>
科目:高中化学 来源:2014福建安溪一中、养正中学、惠安一中高一下学期期末化学试卷(解析版) 题型:选择题
下列叙述不正确的是( )
A.原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键
B.向煤中加入生石灰可减少对大气的污染
C.完全由非金属元素组成的化合物可以形成离子化合物
D.由氮气为原料合成氨是氮的固定
查看答案和解析>>
科目:高中化学 来源:2014福建安溪一中、养正中学、惠安一中高一下学期期末化学试卷(解析版) 题型:选择题
下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为 890.3 kJ·mol-1 ,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3 kJ·mol-1
B.500℃、30MPa 下,将 0.5mol N2(g)和 1.5molH2(g)置于密闭容器中充分反应生成 NH3(g)放热 19.3 kJ,其热化学方程式为:
N2(g)+3H2(g) 2NH3(g) △H = -38.6 kJ·mol-1
2NH3(g) △H = -38.6 kJ·mol-1
C.HCl 和 NaOH 反应的中和热△H = -57.3 kJ·mol-1 ,
则 H2SO4 和 Ca(OH)2 反应的中和热 △H = 2×(-57.3)kJ·mol -1
D.在 101 kPa 时,2gH2完全燃烧生成液态水,放出 285.8kJ 热量,氢气燃烧的热化学方程式表示为 2H2(g)+O2(g)=2H2O(1)△H = -571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014江苏常熟市高二化学期末模拟4(必修2、选修4、结构)试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.MgSO4溶液中加入Ba(OH)2溶液:Ba2++SO4 2-=BaSO4↓
B.FeCl3溶液中加入Cu粉:2Fe3++3Cu=2Fe+3Cu2+
C.酸性碘化钾溶液中滴加双氧水:2I-+2H+ +H2O2=I2+2H2O
D.氯化铝溶液中滴加氨水:Al3++4OH-=AlO2-+2H2O
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版3.4海水中的元素练习卷(解析版) 题型:填空题
空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:

(1)步骤③的离子方程式: 。
(2)步骤⑤中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是 。
(3)溴水混合物Ⅱ中溶有一定量的氯气,因此在步骤⑤中可将蒸馏产生的气体通过 (填试剂名称)溶液,以除去氯气。
(4)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因: 。
(5)步骤①中用硫酸酸化可提高Cl2的利用率,理由是 。
(6)提取溴单质,采用蒸馏“溴水混合物Ⅱ”而不是蒸馏“溴水混合物Ⅰ”,请说明原因: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com