
| A£® | MgŗĶZn | B£® | ZnŗĶFe”¢C | C£® | CuŗĶFe | D£® | ZnŗĶCu |
·ÖĪö ¼ŁÉč½šŹō¶¼ĪŖ+2¼Ū£¬øł¾Żµē×Ó×ŖŅĘŹŲŗć¼ĘĖć½šŹōĪļÖŹµÄĮ棬ŌŁøł¾ŻM=$\frac{m}{n}$¼ĘĖćĘ½¾łĻą¶ŌŌ×ÓÖŹĮæ£¬Ę½¾łĻą¶ŌŌ×ÓÖŹĮæÓ¦½éÓŚø÷×é·ÖÖ®¼ä£¬Čō½šŹō²»ÓėĻ”ŃĪĖį·“Ó¦£¬Óɵē×Ó×ŖŅĘŹŲŗć£¬æÉŅŌŹÓ×÷ĘäĻą¶ŌŌ×ÓÖŹĮæĪŖĪŽĒī“ó£¬Čō·“Ó¦ÖŠ½šŹō²»±ķĻÖ+2¼Ū£¬°“»ÆŗĻ¼ŪÓėĻą¶Ō·Ö×ÓÖŹĮæ³ÉÕż±Č¹ŲĻµÕŪĖć+2¼ŪŹ±Ļą¶Ō·Ö×ÓÖŹĮ森
½ā“š ½ā£ŗ±źæöĻĀ£¬11.2LĒāĘųµÄĪļÖŹµÄĮæĪŖ$\frac{11.2L}{22.4L/mol}$=0.5mol£¬
¼ŁÉč½šŹō¶¼ĪŖ+2¼Ū£¬øł¾Żµē×Ó×ŖŅĘŹŲŗć£¬½šŹōĪļÖŹµÄĮæĪŖ0.5mol£¬½šŹōĘ½¾łĻą¶ŌŌ×ÓÖŹĮæĪŖ$\frac{25}{0.5}$=50£¬
A£®Mg”¢Zn¾łÓėŃĪĖį·“Ӧɜ³ÉĒāĘų£¬¾ł±ķĻÖ+2¼Ū£¬MgĻą¶ŌŌ×ÓÖŹĮæĪŖ24£¬ZnĻą¶Ō·Ö×ÓÖŹĮæĪŖ65£¬Ę½¾łĻą¶Ō·Ö×ÓÖŹĮæ½éÓŚ24Óė65Ö®¼ä£¬·ūŗĻĢāŅā£¬¹ŹAÕżČ·£»
B£®Zn”¢Fe¾łÓėŃĪĖį·“Ӧɜ³ÉĒāĘų£¬¾ł±ķĻÖ+2¼Ū£¬Ļą¶Ō·Ö×ÓÖŹĮæ·Ö±šĪŖ65”¢56£¬C²»ÓėŃĪĖį·“Ó¦£¬Ļą¶ŌŌ×ÓÖŹĮæĪŖĪŽĒī“󣬾ł“óÓŚ50£¬²»·ūŗĻĢāŅā£¬¹ŹB“ķĪó£»
C£®Cu²»ÓėŃĪĖį·“Ó¦£¬FeÓėŃĪĖį·“Ó¦±ķĻÖ+2¼Ū£¬Ļą¶Ō·Ö×ÓÖŹĮæĪŖ56£¬¾ł“óÓŚ50£¬¹ŹC²»·ūŗĻ£»
D£®Fe¾łÓėŃĪĖį·“Ӧɜ³ÉĒāĘų£¬±ķĻÖ+2¼Ū£¬Ļą¶Ō·Ö×ÓÖŹĮæĪŖ65£¬Cu²»ÓėŃĪĖį·“Ó¦£¬Ļą¶ŌŌ×ÓÖŹĮæĪŖĪŽĒī“󣬾ł“óÓŚ50£¬²»·ūŗĻĢāŅā£¬¹ŹD“ķĪó£®
¹ŹŃ”£ŗA£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļ¼ĘĖć£¬²ąÖŲæ¼²éѧɜ·ÖĪöĖ¼Ī¬Óė½āĢā·½·Ø¼¼ĒɵÄ漲飬עŅāĄūÓĆĘ½¾łÖµ½ā“š£¬Ņ²æÉŅŌĄūÓĆ¼«Öµ·Ø¼ĘĖćŠčŅŖ½šŹōµÄÖŹĮæµČ½ųŠŠ½ā“š£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | N2O | B£® | NO2 | C£® | N2O5 | D£® | NaNO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2+H2OØTH2CO3»ÆŗĻ·“Ó¦ | |
| B£® | Cu£ØOH£©2$\frac{\underline{\;\;”÷\;\;}}{\;}$CuO+H2O ·Ö½ā·“Ó¦ | |
| C£® | Fe2O3+3CO$\frac{\underline{\;øßĪĀ\;}}{\;}$2Fe+3CO2ÖĆ»»·“Ó¦ | |
| D£® | NaCl+AgNO3ØTAgCl”ż+NaNO3ø“·Ö½ā·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.6a g | B£® | £Øa-1.6£©g | C£® | £Øa-3.2£©g | D£® | £Ø2a-3.2£©g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol¼×±½ŗ¬ÓŠ6nAøöC-H¼ü | |
| B£® | 18 g H2Oŗ¬ÓŠ10nAøöÖŹ×Ó | |
| C£® | ±ź×¼×“æöĻĀ£¬2.24 L CCl4ÖŠŗ¬ÓŠµÄC-Cl¼üŹżĪŖ0.4NA | |
| D£® | ³£ĪĀĻĀ£¬56 gĢśĘ¬Ķ¶Čė×ćĮæÅØH2SO4ÖŠÉś³ÉnAøöSO2·Ö×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
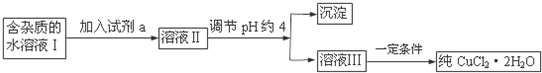
| ³ĮµķĪļ | Fe£ØOH£©3 | Fe£ØOH£©2 | Cu£ØOH£©2 |
| æŖŹ¼³ĮµķpH | 2.7 | 7.6 | 4.7 |
| Ķź³É³ĮµķpH | 3.2 | 9.7 | 6.7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K2SO4ČÜŅŗ | B£® | KNO3ČÜŅŗ | C£® | Na2SO4£Øs£© | D£® | Na2CO3£Øs£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com