
�����12�֣���Ⱦ�����Чȥ������Դ�ij�������ǻ�ѧ�츣�������Ҫ�о����⡣ij�о�С���������̿���Ҫ�ɷ�ΪMnO2������������������ͭ�Ƚ�����������������ͨ�����¼����̣����ѳ�ȼúβ���е�SO2�����Ƶõ�ز���MnO2����Ӧ������ʡ�ԣ���
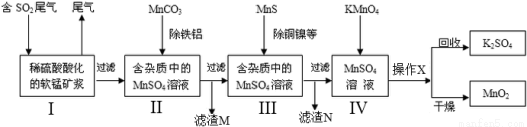
��ش��������⣺
38��������������ʵ���� ��ѡ���ţ���
a����������ۺ����� b����ɫ��Ⱦ�ļ���
c������ļ��� d��������ն��ļ���
39������I������ˮMnSO4�Ļ�ѧ����ʽ�� ��
����IV������ˮMnO2�Ļ�ѧ����ʽ�� ��
40������I�У���MnCO3�ܳ�ȥ��Һ��Al3����Fe3������ԭ���� ������M�ijɷ��� ��ͭԪ���� ��ʽ����������N�С���д��ѧʽ��
41����ƷMnO2�����������ݲ��ϡ��ö��Ե缫���MnSO4��Һ�����Ƶ�MnO2����MnO2�� ���ɣ���缫���ƣ���
42�������ѳ���SO2ֻ�����̿���MnO2��Ӧ������ͼʾ���̣���2.0 m3(��״��)��SO2���������Ϊ60%��β��ͨ�����SO2���ѳ���Ϊ89.6%�����յõ�MnO2������10.44 kg�����ڳ�ȥ��������ͭ���������ʵĹ����У����������Ԫ��Ϊ kg��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡμ���и�����ѧ������⣨һģ����ѧ�Ծ��������棩 ���ͣ������
(14��)(I)��֪X��Y��Z��WΪ���������ֳ���Ԫ�أ�����X��ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�ӵ��������������ڲ������������Z�ܺ�X�γ����ֳ�����Һ̬�����WԪ�صĵ��ʼ��������ᷴӦҲ����NaOH��Һ��Ӧ���Իش���������:
��1����д������Ԫ�ص�����:Y____________��W____________��
��2����д��X2Z2�ĵ���ʽ________________��
��3����д��WԪ�صĵ�����NaOH��Һ��Ӧ�����ӷ���ʽ____________��
(II)A����X�� Y�� Z��Cu����Ԫ����ɵ���ɫ���壬��������ͼ��ʾת������Ӧ���������ֲ�������ȥ)��
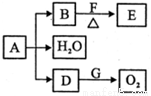
�����£�DΪ��ɫ��ζ���壬BΪ��ɫ��ĩ��75%��Fˮ��Һ����ҽ������������ش���������:
��4��D��G��Ӧ�Ļ�ѧ����ʽ____________________��
��5��E�к��й����ŵ�����__________����д������E�й����ŵĻ�ѧ����ʽ_ ______________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ��У�����ڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������������ȷ����
A��NH4Cl��Һ��ˮϡ�ͺָ���ԭ�¶ȣ�pH��KW������
B��0.1 mol/L CH3COONa��Һ�У�c(Na+)��c(CH3COO-)��c(OH-)��c(H+)
C��pH��4��CH3COOH��Һ��pH��4��NH4Cl��Һ�У�c��H+�����
D����NaHCO3��Һ�У�c��OH����+c��CO32������c��H+��+c��H2CO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ԭ�и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������Xn��������N����X��������ΪA����a g X���⻯���к����ӵ����ʵ�����
A��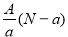 mol B��
mol B��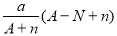 mol
mol
C��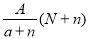 mol D��
mol D��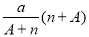 mo1
mo1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ԭ�и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������Ӧ��ѧ��������ۺ�������
ѡ�� | ��ѧ���� | ���� |
A |
| �������Ӻ�����89������ |
B | 2H2(g)+O2(g)= 2H2O(g)����H=��483.6kJmol | 1mol������ȫȼ�շų�����483.6kJ. |
C | 2NaCl+2H2O | NaCl�����Ա�Cl2ǿ |
D | FeO+4H++NO3�D= Fe3++NO2��+2H2O | ������������ϡ��������ӷ���ʽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ϻ��з����������ڶ�ѧ�ڵ��в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ��ѧ�кܶࡰ���ɡ����������÷�Χ�����и����йء����ɡ��Ƴ��Ľ�����ȷ����
ѡ�� | ���� | ���� |
A | �е�ߵ������Ʊ��е�͵����� | ���û���﨣���Ũ�����Ʊ�HI |
B | ��Ӧ��Ũ��Խ��Ӧ����Խ�� | �����£���ͬ����Ƭ�зֱ����������Ũ��ϡ���ᣬŨ��������Ƭ���ܽ��� |
C | �ṹ��������Ƶ����ʣ��е�����Է���������������� | BCl3�е����AlCl3��CO2�е����SiO2 |
D | �ܽ��С�ij��������ܽ�ȸ�С�ij���ת�� | ZnS�����еμ�CuSO4��Һ���Եõ�CuS���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ϻ��з����������ڶ�ѧ�ڵ��в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ʾ������Ԫ���У�W��X��Y��ZΪ������Ԫ�أ�������Ԫ�ص�ԭ������������֮��Ϊ22������˵����ȷ����

A��X��Y��Z����Ԫ����ͼ��⻯��ķе���������
B����X��Y��������Ԫ���γɵĻ�������ֻ�й��ۼ�
C��ԭ�ӵõ�������ǿ����W��X��Y��Z
D��TԪ�صĵ��ʿ��ܾ��а뵼������ԣ�T��ZԪ�ؿ��γɻ�����TZ4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ����������У������ѧ�����������ۻ�ѧ�Ծ��������棩 ���ͣ������
��14�֣�SiCl4��������Ϊ��ɫҺ�壬�ӷ�����ǿ�ҵĴ̼��ԣ���SiCl4��ת��ΪSiHCl3���پ�������ԭ���ɸߴ��裮
��1�����������£�SiHCl3��������Ӧ�ķ���ʽΪ�� ��
��2����֪��
������Si(S)+4HCl(g)=SiCl4(g)+2H2(g) ��H=-241KJ.mol-1
������Si(S)+3HCl(g)=SiHCl3(g)+H2(g) ��H=-210KJ.mol-1
��SiCl4ת��ΪSiHCl3�ķ�Ӧ��������3SiCl4(g)+2H2(g)+Si(S)==4SiHCl3(g) ��H=______��
��3�����о���Ӧ��iii���������˷�Ӧ�¶ȣ���ͼΪ���Ȼ�̼��ת�������¶ȵı仯���ߣ���ͼ��֪�÷�Ӧ�����˵��¶�Ϊ �����Ȼ�̼��ת�������¶����߶������ԭ��Ϊ____��
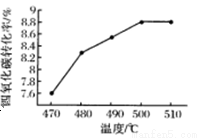
��4��һ�������£���2L�����ܱ������з�����Ӧ��������6h��ﵽƽ�⣬H2��SiHCl3�����ʵ���Ũ�ȷֱ�Ϊ1mol.L-1��0.2 mol.L-1
�ٴӷ�Ӧ��ʼ��ƽ�⣬v��SiCl4��=___________��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽΪK= ���¶����ߣ�Kֵ �������������С�����䡱����
��ԭ�����У�ͨ��H2���������״���£�Ϊ ��
����ƽ������������г�������ʼʱ������SiCl4��H2������Si������������Ӧ�ٴδﵽƽ��ʱ����ԭƽ����Ƚϣ�H2����������� �����������С�����䡱����
��ƽ������������ѹ��Ϊ1L���ٴδﵽƽ��ʱ��H2�����ʵ���Ũ�ȷ�ΧΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ݱ��������Ħ��������˾�з���һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ������ɴ�����ʹ�õ������ػ�﮵�ص�ʮ����������ʹ��һ���²ų�һ�ε硣���ط�ӦΪ�� 2CH3OH + 3O2 + 4OH- 2CO32-+6H2O��������˵����ȷ����
2CO32-+6H2O��������˵����ȷ����
A�����ɸõ�ص������������������ֻ��Բ�ͬ�Ľ���
B�����ʱ��CH3OH���ɵĵ缫Ϊ����
C���ŵ�ʱ�������Һ��pH������
D���ŵ�ʱ�����ĵ缫��ӦΪ��CH3OH��6e�� ��8OH�� �� CO32- + 6H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com