
| 离子 | Na+ | Mg2+ | Al3+ |
| 浓度/mol•L-1 | 0.5 | 1.0 | 0.5 |
分析 (1)根据n=cV计算Na+、Mg2+的物质的量,溶液中n(NaCl)=n(Na+),n(MgCl2)=n(Mg2+),再根据m=nM计算氯化镁的质量;
(2)根据镁离子、钠离子和铝离子浓度计算出氯离子浓度,然后根据n(AgNO3)=n(Cl-)、V=$\frac{n}{c}$计算AgNO3溶液的体积;
(3)稀释过程中钠离子的物质的量不变,根据稀释定律计算稀释后中Na+的物质的量浓度.
解答 解:(1)溶液中n(NaCl)=n(Na+)=0.2L×0.5mol/L=0.1mol;
n(MgCl2)=n(Mg2+)=0.2L×1mol/L=0.2mol,故氯化镁的质量为:0.2mol×95g/mol=19g,
故答案为:0.1mol;19g;
(2)c(Cl-)=c(Na+)+2c(Mg2+)+3c(Al3+)=0.5mol/L+1.0mol/L×2+0.5mol/L×3=4mol/L,
n(AgNO3)=n(Cl-)=0.2L×4mol/L=0.8mol,需要AgNO3溶液的体积为:$\frac{0.8mol}{0.1mol/L}$=8L,
故答案为:8L;
(3)稀释过程中钠离子的物质的量不变,则稀释后钠离子的浓度为:c(Na+)=$\frac{0.5mol/L×0.2L}{1L}$=0.1mol/L,
故答案为:0.1mol/L.
点评 本题考查物质的量浓度有关计算,题目难度中等,注意掌握物质的量浓度的概念及表达式,明确守恒思想在化学计算中的应用方法为解答关键,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | c(NH4+)>c(SO42-)>c(H+)>c(OH-) | B. | c(NH4+)=2c(SO42-) | ||
| C. | c(NH4+)+c(NH3•H2O)=2c(SO42-) | D. | c(NH4+)+c(H+)=c(OH-)+2c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
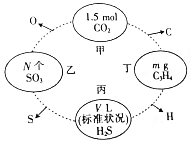 如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)
如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在和上面初始体积相同的恒温恒压密闭容器中,也充入0.5molN2和1.5molH2发生反应则达到平衡时,放出的热量大于46.2kJ | |
| B. | 在平衡时再充入1molNH3则平衡向左移动,则平衡时N2的百分含量减小 | |
| C. | 若向容器中充入一定量He气,则平衡向右移动 | |
| D. | 在平衡后再充入1molH2,则N2的转化率增大,且平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ①③⑤ | C. | ②④⑥ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使淀粉碘化钾试纸显蓝色的溶液:Na+、H+、I-、SO32- | |
| B. | 饱和CO2的溶液中:Ca2+、K+、NO3-、Cl- | |
| C. | 在pH=14的溶液中:Na+、K+、Cl-、SO2 | |
| D. | 无色透明溶液:Na+、Ba2+、MnO4-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH═CHCH2CH3 | B. | CH2═CHCH═CH2 | C. | CH2═CHCH3 | D. | CH3-CH═CH-CH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com